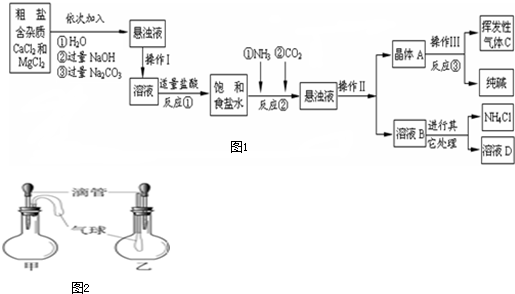
(2013?北京二模)化学小组对某品牌牙膏中摩擦剂成分及其含量产生兴趣,设计实验进行探究.
【提出问题】摩擦剂中有哪些主要成分,它们的含量是多少?
【查阅资料】①该牙膏摩擦剂由氢氧化铝、碳酸钙粉末组成.
②牙膏中其它成分遇到氢氧化钠不溶解,遇到稀硫酸时无气体生成.
③氢氧化铝[Al(OH)
3]和氢氧化钠溶液反应生成偏铝酸钠[NaAlO
2]和水,该反应的化学方程式为
Al(OH)3+NaOH═NaAlO2+2H2O
Al(OH)3+NaOH═NaAlO2+2H2O
.偏铝酸钠和稀硫酸反应生成氢氧化铝,氢氧化铝和稀硫酸反应生成硫酸铝.
相关物质的溶解性表
| 物质 |
Al(OH)3 |
NaAlO2 |
Al2(SO4)3 |
| 溶解性 |
不溶 |
溶 |
溶 |
④Ba(OH)
2+CO
2═BaCO
3↓+H
2O
【猜想与实验】
实验I:验证中摩擦剂中含有氢氧化铝.
同学们先在少量牙膏样品中加入过量的氢氧化钠溶液,静置一段时间,取上层清液,再滴加稀硫酸至过量,此实验过程中观察到的现象为
牙膏样品中部分固体溶解,向上层清液中滴加稀硫酸时先有固体产生,后固体溶解
牙膏样品中部分固体溶解,向上层清液中滴加稀硫酸时先有固体产生,后固体溶解
,根据该现象可以判断摩擦剂中含有氢氧化铝.
实验II:验证摩擦剂中含有碳酸钙,并测定其含量.同学们在老师的指导下设计了如图所示装置.
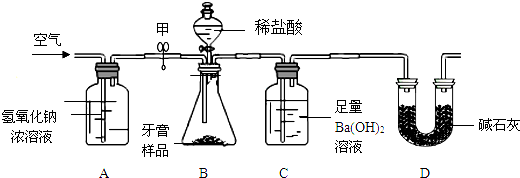
(1)实验步骤:
①如图所示连接好装置,并
检验装置的气密性
检验装置的气密性
;
②准确称取牙膏样品的质量8.00g,并在各仪器中加入相应试剂;
③打开弹簧夹甲,缓缓通入空气,然后接上C和D;
④打开B的分液漏斗滴加稀硫酸反应,同时再次持续缓缓通入空气;
⑤待B中不再产生气体后停止滴加稀硫酸;
⑥将C中沉淀过滤、洗涤、干燥,得BaCO
3固体.
(2)数据处理:
实验中准确称取8.00g样品三份,进行三次测定,测得BaCO
3平均质量为3.94g.则牙膏样品中碳酸钙的质量分数为
25%
25%
.
【实验反思】
(1)A中放NaOH溶液的作用是
吸收空气中的二氧化碳,防止干扰测定结果
吸收空气中的二氧化碳,防止干扰测定结果
.
(2)实验过程中需持续缓缓通入空气.其作用除了可搅拌B、C中的反应物外,还有
使样品与稀盐酸反应生成的二氧化碳都吹入C中,全部与氢氧化钡反应生成碳酸钡
使样品与稀盐酸反应生成的二氧化碳都吹入C中,全部与氢氧化钡反应生成碳酸钡
.
(3)有同学认为不必测定装置C中生成BaCO
3质量,只要测定装置C在吸收CO
2前后质量差,一样可以准确测定碳酸钙质量分数.请说明是否可以及理由
不可以;这样测得的结果会偏大,因为B中的水蒸气、HCl气体会进入装置C中,测得的二氧化碳的质量偏大,通过计算得到的碳酸钙的质量分数会偏大
不可以;这样测得的结果会偏大,因为B中的水蒸气、HCl气体会进入装置C中,测得的二氧化碳的质量偏大,通过计算得到的碳酸钙的质量分数会偏大
.


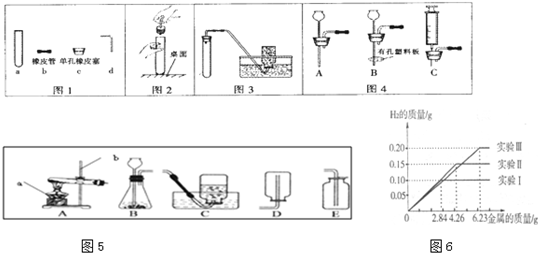
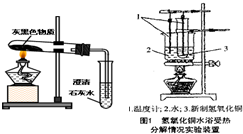 金属镁将成为二十一世纪大有前途的绿色金属材料.
金属镁将成为二十一世纪大有前途的绿色金属材料.