
加热分解高锰酸钾KMnO4也是实验室制氧气方法之一,其中锰元素的化合价为( )
|
科目:初中化学 来源: 题型:阅读理解

| ||
| ||
科目:初中化学 来源: 题型:解答题
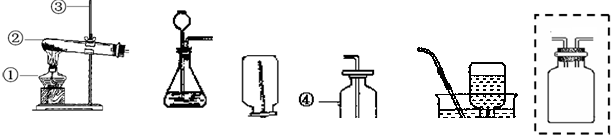
科目:初中化学 来源: 题型:
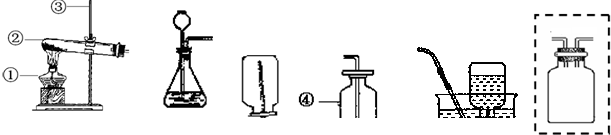
| ||
| ||
科目:初中化学 来源: 题型:
实验室既可用KMnO4(或KClO3和MnO2的混合物)在加热条件下使其分解制取氧气,也可用下图装置,通过分解过氧化氢(H2O2)来制取氧气。请你根据已学化学知识和经验回答下列问题:
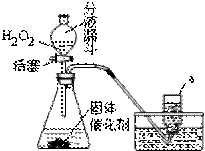
(1) 写出过氧化氢分解的化学方程式:
(2) 写出上图装置中仪器a的名称:
(3) 与高锰酸钾(或氯酸钾和二氧化锰的混合物)制取氧气相比,用过氧化氢制取氧气的优点是:
(4) 收集氧气的方法还可用 法,你选择此方法的理由是:
(5)上图发生装置还可以用于制取的气
体有 。
并写出制取该气体的化学方程式
科目:初中化学 来源:2013届湖南省长沙县开慧中学九年级12月月考化学试卷(带解析) 题型:填空题
实验室既可用KMnO4(或KClO3和MnO2的混合物)在加热条件下使其分解制取氧气,也可用下图装置,通过分解过氧化氢(H2O2)来制取氧气。请你根据已学化学知识和经验回答下列问题: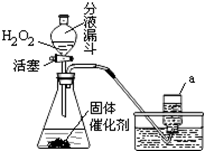
(1)写出过氧化氢分解的化学方程式:
(2)写出上图装置中仪器a的名称:
(3)与高锰酸钾(或氯酸钾和二氧化锰的混合物)制取氧气相比,用过氧化氢制取氧气的优点是:
(4)收集氧气的方法还可用 法,你选择此方法的理由是:
(5)上图发生装置还可以用于制取的气体有 。
并写出制取该气体的化学方程式
科目:初中化学 来源:2012-2013学年湖南省九年级12月月考化学试卷(解析版) 题型:填空题
实验室既可用KMnO4(或KClO3和MnO2的混合物)在加热条件下使其分解制取氧气,也可用下图装置,通过分解过氧化氢(H2O2)来制取氧气。请你根据已学化学知识和经验回答下列问题:
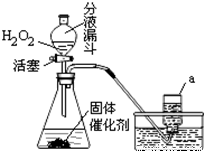
(1)写出过氧化氢分解的化学方程式:
(2)写出上图装置中仪器a的名称:
(3)与高锰酸钾(或氯酸钾和二氧化锰的混合物)制取氧气相比,用过氧化氢制取氧气的优点是:
(4)收集氧气的方法还可用 法,你选择此方法的理由是:
(5)上图发生装置还可以用于制取的气体有 。
并写出制取该气体的化学方程式
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com