
“NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl 2NaHCO3?Na2CO3+CO2↑+H2O”是著名的“侯氏制碱法”的重要反应.同学们对上述反应涉及的有关知识发表了下列见解.其中不正确的是( )
|
科目:初中化学 来源:六合区模拟 题型:单选题
| A.该条件下NaHCO3的溶解度较小 |
| B.副产品氯化铵是一种氮肥 |
| C.析出固体后的溶液为NaHCO3的不饱和溶液 |
| D.二氧化碳在制纯碱的过程中可循环使用 |
科目:初中化学 来源: 题型:
科目:初中化学 来源:2009年江苏省镇江市中考化学模拟试卷(解析版) 题型:选择题
科目:初中化学 来源:2009-2010学年江苏省南京市六合区九年级(下)调研测试化学试卷(解析版) 题型:选择题
科目:初中化学 来源: 题型:单选题
科目:初中化学 来源:北海 题型:问答题
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量滤液于试管中,滴加足量的NaOH浓溶液并加热. | 产生刺激性气味气体 | 证明滤液中含有NH4Cl,写出有关化学方程式:______. |
| ②另取少量滤液于试管中,滴加______. | 产生无色无味气体 | 证明滤液中含有______. |
| ③另取少量滤液于试管中,滴加稀HNO3酸化后,再滴加AgNO3溶液. | 产生白色沉淀 | ______(填“能”或“不能”)证明滤液中含有NaCl. |
| ||
| ||
科目:初中化学 来源: 题型:
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量滤液于试管中,滴加足量的NaOH浓溶液并加热. | 产生刺激性气味气体 | 证明滤液中含有NH4Cl,写出有关化学方程式: NaOH+NH4Cl═NaCl+NH3↑+H2O NaOH+NH4Cl═NaCl+NH3↑+H2O . |
| ②另取少量滤液于试管中,滴加 稀盐酸 稀盐酸 . |
产生无色无味气体 | 证明滤液中含有 碳酸氢钠 碳酸氢钠 . |
| ③另取少量滤液于试管中,滴加稀HNO3酸化后,再滴加AgNO3溶液. | 产生白色沉淀 | 不能 不能 (填“能”或“不能”)证明滤液中含有NaCl. |
| ||
| ||
科目:初中化学 来源: 题型:
| ||

科目:初中化学 来源: 题型:
我国科学家侯德榜创造了一种著名的纯碱生产方法——“联合制碱法”。“联合制碱法”生产过程用化学方程式可简要表示为:
①NH3+CO2+H2O==NH4HCO3 ②NH4HCO3+NaCl==NaHCO3+NH4Cl
③2NaHCO3 ===![]() ====Na2CO3+H2O+CO2 ↑
====Na2CO3+H2O+CO2 ↑
(1)从表中数据可以看出,温度对____________的溶解度影响不大。
(2)要使NH4Cl饱和溶液中的NH4Cl结晶析出,在__________(填“较高”或“较低”)温度下进行比较合适。
0℃ | 20℃ | 40℃ | 60℃ | |
NaHCO3 | 6.9 | 9.6 | 12.7 | 16.4 |
NaCl | 35.7 | 35.8 | 36.6 | 37.3 |
NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 |
(3)“侯氏制碱法”制NaHCO3的方程式也可表示为NaCl+CO2+NH3+H2O==NaHCO3+NH4Cl,该反应能进行的原因是:室温时_ ___________________
第②步中加入的是磨细食盐粉。食盐磨细的目的是________________________
(4)将第②步所得滤液(NH4Cl与剩余NaCl的混合溶液)降温,NH4Cl晶体大量析出,而NaCl却仍留在溶液中。你认为NH4Cl先结晶的原因可能是________________,所得NH4Cl属于化学肥料中的_____________肥。
科目:初中化学 来源: 题型:
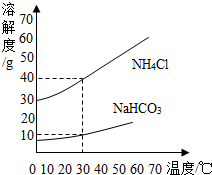 1926年,我国著名化学家侯德榜先生创立了一种高效环保的纯碱生产方法--“联合制碱法”,又称侯氏制碱法.其生产过程中有下列反应:
1926年,我国著名化学家侯德榜先生创立了一种高效环保的纯碱生产方法--“联合制碱法”,又称侯氏制碱法.其生产过程中有下列反应:
| ||
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com