
УОКЭбѕЦјЗДгІЩњГЩСЫ5gбѕЛЏУОЃЌдђЫљЯћКФЕФУОКЭбѕЦјЕФжЪСПЗжБ№ЮЊЃЈЁЁЁЁЃЉ
|
ПЦФПЃКГѕжаЛЏбЇ РДдДЃК ЬтаЭЃК
| AЁЂУО2gЁЂбѕЦј3g | BЁЂУО3gЁЂбѕЦј2g | CЁЂУО1gЁЂбѕЦј4g | DЁЂУО4gЁЂбѕЦј1g |
ПЦФПЃКГѕжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЕЅбЁЬт
| AЃЎУО2gЁЂбѕЦј3g | BЃЎУО3gЁЂбѕЦј2g |
| CЃЎУО1gЁЂбѕЦј4g | DЃЎУО4gЁЂбѕЦј1g |
ПЦФПЃКГѕжаЛЏбЇ РДдДЃКЁЖ4.2 ЖЈСПШЯЪЖЛЏбЇБфЛЏЁЗ2010ФъПЮЪБСЗЯАЃЈ5ЃЉЃЈНтЮіАцЃЉ ЬтаЭЃКбЁдёЬт
ПЦФПЃКГѕжаЛЏбЇ РДдДЃКЁЖ5.4 ЛЏбЇЗДгІжаЕФгаЙиМЦЫуЁЗ2010ФъЭЌВНСЗЯАЃЈНтЮіАцЃЉ ЬтаЭЃКбЁдёЬт
ПЦФПЃКГѕжаЛЏбЇ РДдДЃК ЬтаЭЃКЕЅбЁЬт
ПЦФПЃКГѕжаЛЏбЇ РДдДЃК ЬтаЭЃК
| AЃЎУО2gЁЂбѕЦј3g | BЃЎУО3gЁЂбѕЦј2g | CЃЎУО1gЁЂбѕЦј4g | DЃЎУО4gЁЂбѕЦј1g |
ПЦФПЃКГѕжаЛЏбЇ РДдДЃКЛІНЬАцГѕЖўЛЏбЇЖЈСПШЯЪЖЛЏбЇБфЛЏ3ЭЌВНСЗЯА ЬтаЭЃКЕЅбЁЬт
УОКЭбѕЦјЗДгІЩњГЩСЫ5gбѕЛЏУОЃЌдђЫљЯћКФЕФУОКЭбѕЦјЕФжЪСПЗжБ№ЮЊЃЈ ЃЉ
| AЃЎУО2gЁЂбѕЦј3g | BЃЎУО3gЁЂбѕЦј2g | CЃЎУО1gЁЂбѕЦј4g | DЃЎУО4gЁЂбѕЦј1g |
ПЦФПЃКГѕжаЛЏбЇ РДдДЃК ЬтаЭЃК
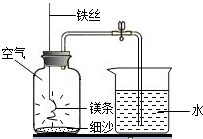 ЂёЁЂШчЭМЫљЪОЪЕбщжаЃЌШчЙћУОЬѕжЛгыПеЦјжаЕФбѕЦјЗДгІЃЌЛЏбЇЗНГЬЪНЮЊ
ЂёЁЂШчЭМЫљЪОЪЕбщжаЃЌШчЙћУОЬѕжЛгыПеЦјжаЕФбѕЦјЗДгІЃЌЛЏбЇЗНГЬЪНЮЊ| 3 |
| 5 |
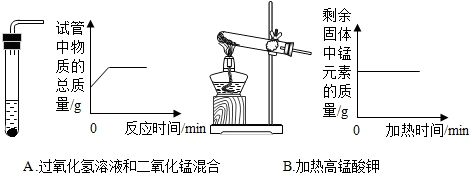
| ађКХ | KClO3ЕФжЪСП | ЦфЫћЮяжЪЕФжЪСП | ЮТЖШ | бѕЦјЕФЬхЛ§ | ЗДгІЫљашЪБМф |
| Ђй | 2.0g | 330Ёц | 100mL | t1 | |
| Ђк | 2.0g | CuO 0.5g | 330Ёц | 100mL | t2 |
| Ђл | 2.0g | MnO2 0.5g | 330Ёц | 100mL | t3 |
| Ђм | 2.0g | MnO2 |
380Ёц | 100mL | t4 |
ПЦФПЃКГѕжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЂёЁЂШчЭМЫљЪОЪЕбщжаЃЌШчЙћУОЬѕжЛгыПеЦјжаЕФбѕЦјЗДгІЃЌЛЏбЇЗНГЬЪНЮЊ ЃЌдђНјШыМЏЦјЦПжаЫЎЕФЬхЛ§зюЖрВЛГЌЙ§ЦфШнЛ§ЕФ ЁЃБОЪЕбщжаЪЕМЪНјШыМЏЦјЦПжаЫЎЕФЬхЛ§дМЮЊЦфШнЛ§ЕФ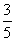 ЃЌдђМЏЦјЦПжаМѕЩйЕФЦјЬхжаГ§O2ЭтЃЌвЛЖЈЛЙга ЁЃ
ЃЌдђМЏЦјЦПжаМѕЩйЕФЦјЬхжаГ§O2ЭтЃЌвЛЖЈЛЙга ЁЃ

ЂђЁЂЯТСаAЁЂBЪЕбщжаЪ§ОнБфЛЏЙиЯЕгыЖдгІЭМЯёЯрЗћЕФЪЧ ЁЁЃЈЬюзжФИађКХЃЉЁЃ

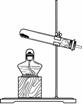
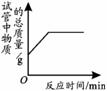

AЃЎЙ§бѕЛЏЧтШмвККЭЖўбѕЛЏУЬЛьКЯ BЃЎМгШШИпУЬЫсМи
ЂѓЁЂаЁгъдФЖСПЮЭтзЪСЯЕУжЊЃКТШЫсМиЗжНтГ§СЫгУЖўбѕЛЏУЬЭтЃЌЛЙПЩгУбѕЛЏЭЕШЮяжЪзїДпЛЏМСЃЌгкЪЧЫћЖдбѕЛЏЭВњЩњСЫЬНОПаЫШЄЁЃ
ЁОЬсГіЮЪЬтЁПбѕЛЏЭЪЧЗёБШЖўбѕЛЏУЬДпЛЏаЇЙћИќКУЃПгАЯьТШЫсМиЗжНтЫйТЪЕФвђЫигаФФаЉФиЃП
ЁОЩшМЦЪЕбщЁПаЁгъвдЩњГЩЕШЬхЛ§ЕФбѕЦјЮЊБъзМЃЌЩшМЦСЫЯТСаМИзщЪЕбщЃЈЦфЫќПЩФмгАЯьЪЕбщЕФвђЫиОљКіТдЃЉЁЃ
| ађКХ | KClO3ЕФжЪСП | ЦфЫћЮяжЪЕФжЪСП | ЮТЖШ | бѕЦјЕФЬхЛ§ | ЗДгІЫљашЪБМф |
| Ђй | 2.0g | 330Ёц | 100mL | t1 | |
| Ђк | 2.0g | CuO 0.5g | 330Ёц | 100mL | t2 |
| Ђл | 2.0g | MnO2 0.5g | 330Ёц | 100mL | t3 |
| Ђм | 2.0g | MnO2 g | 380Ёц | 100mL | t4 |
ЃЈ1ЃЉШєt1 t2ЃЈЬюЁАДѓгкЁБЁЂЁАЕШгкЁБЁЂЁАаЁгкЁБЃЉЃЌЫЕУїбѕЛЏЭФмМгПьТШЫсМиЕФЗжНтЫйТЪЁЃ
ЃЈ2ЃЉФуШЯЮЊаЁгъЩшМЦЪЕбщЂлКЭЪЕбщЂкЖдБШЕФФПЕФЪЧ ЁЃ
ЃЈ3ЃЉЪЕбщЂмжаПижЦMnO2ЕФжЪСПЮЊ gЃЌШєt3>t4ЃЌдђЛЏбЇЗДгІПьТ§гыЮТЖШЕФЙиЯЕЪЧ ЁЃ
ЃЈ4ЃЉаДГіЪЕбщЂмЫљЩцМАЕФЛЏбЇЗНГЬЪН ЁЃ
ПЦФПЃКГѕжаЛЏбЇ РДдДЃК ЬтаЭЃКдФЖСРэНт
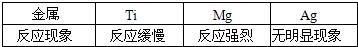
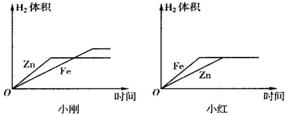
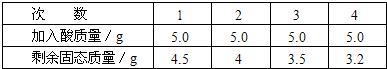
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com