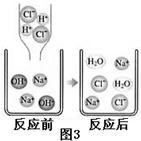
ªØ—ߌÔ÷ ÷ƺ‰µƒ∑¥”¶∞¬√ӌޫӣƑ⁄“ª¥ŒªØ—ßÃΩæøªÓ∂Ø÷–£¨Õ¨—ß√«¥”≤ªÕ¨Ω«∂»∂‘œ°¡ÚÀ·”Ϋ‚—ıªØƒ∆»Ð“∫µƒ∑¥”¶Ω¯––¡ÀÃΩæø£¨«Îƒ„≤Œ”Î≤¢ÃÓ–¥“‘œ¬ø’∞◊£Æ
£®1£©»Á∫Œ”√ µ—È—È÷§œ°¡ÚÀ·”Ϋ‚—ıªØƒ∆»Ð“∫∑¢…˙¡À∑¥”¶
µ⁄“ª◊ÈÕ¨—߅˺∆¡À µ—È∑Ω∞∏“ª£∫
| µ—È≤Ω÷Ë | µ—Èœ÷œÛ | Ω·¬€ |
| œ»”√PH ‘÷Ω≤‚∂®œ°¡ÚÀ·µƒPH£¨‘Ÿ÷Ω•µŒº”«‚—ıªØƒ∆»Ð“∫£¨≤¢≤ª∂œ’Òµ¥£¨Õ¨ ±≤‚∂®ªÏ∫œ“∫µƒPH£Æ | PH÷Ω•±‰¥Û£¨
◊Ó∫Û PH°ð7 | œ°¡ÚÀ·”Ϋ‚—ıªØƒ∆»Ð“∫ƒÐ∑¢…˙∑¥”¶ |
¢Ÿ«Îƒ„∑÷Œˆ…œ ˆ∑Ω∞∏÷–Œ™ ≤√¥«øµ˜÷ª”–≤‚µ√µƒPH°ð7≤≈ƒÐ÷§√˜∑¥”¶∑¢…˙¡À£ø______
______£Æ
¢⁄–¥≥ˆœ°¡ÚÀ·”Ϋ‚—ıªØƒ∆»Ð“∫∑¥”¶µƒªØ—ß∑Ω≥à Ω______£Æ
£®2£©…˺∆ µ—È£¨ÃΩæøœ°¡ÚÀ·”Ϋ‚—ıªØƒ∆»Ð“∫µƒ∑¥”¶ «∑Ò∑≈»»
µ—È“«∆˜”Γ©∆∑£∫10%µƒ¡ÚÀ·°¢10%µƒ«‚—ıªØƒ∆»Ð“∫°¢…’±≠°¢Œ¬∂»º∆°¢≤£¡ß∞Ù°¢Ω∫Õ∑µŒπУÆ
«Îƒ„ÕÍ≥… µ—È∑Ω∞∏…˺∆£∫
| µ —È ≤Ω ÷Ë | µ—Èœ÷œÛ | Ω·¬€ |
| | œ°¡ÚÀ·”Ϋ‚—ıªØƒ∆»Ð“∫∑¥”¶∑≈»» |
£®3£©ÃΩæøœ°¡ÚÀ·”Ϋ‚—ıªØƒ∆»Ð“∫ «∑Ò«°∫√ÕÍ»´∑¥”¶
µ⁄∂˛◊ÈÕ¨—ß‘⁄◊ˆÕÍœ°¡ÚÀ·”Ϋ‚—ıªØƒ∆»Ð“∫∑¥”¶µƒ µ—È∫Û£¨Œ™ÃΩæøœ°¡ÚÀ·”Ϋ‚—ıªØƒ∆»Ð“∫ «∑Ò«°∫√ÕÍ»´∑¥”¶£Æ
…˺∆¡À µ—È∑Ω∞∏∂˛£∫
| µ—È≤Ω÷Ë | µ—Èœ÷œÛ | Ω·¬€ |
| »°…Ÿ¡ø…œ ˆ∑¥”¶∫Ûµƒ»Ð“∫”⁄ ‘πÐ÷–£¨µŒº”¡ÚÀ·Õ≠»Ð“∫£Æ | »Ù______ | «‚—ıªØƒ∆»Ð“∫π˝¡ø |
| »Ù√ª”–√˜œ‘œ÷œÛ | œ°¡ÚÀ·”Ϋ‚—ıªØƒ∆»Ð“∫«°∫√ÕÍ»´∑¥”¶ |
¥À ±”–Õ¨—ß÷≥ˆ∑Ω∞∏∂˛≤ªƒÐ÷§√˜œ°¡ÚÀ·”Ϋ‚—ıªØƒ∆»Ð“∫«°∫√ÕÍ»´∑¥”¶£¨∆‰‘≠“Ú «______£ÆŒ™¥À£¨ªπ–Ë“™—°‘Ò______£®ÃÓ“ª÷÷ ‘º¡£©£¨‘ŸΩ¯–– µ—Ⱥ¥ø…£Æ
ƒÐ¡¶Ã·…˝£∫
ƒ≥µÿ–¬Ω®“ªªØπ§≥ß”–“ª÷÷≤˙∆∑ Ù”⁄°∞∏¥—Œ°±£¨∏√≤˙∆∑ø…”√◊˜Ã˙ ˜°¢◊ÿȵµ»ª®ƒæµƒ∑ ¡œ£Æƒ≥ªØ—ßøŒÕ‚–À»§–°◊ÈÃΩæø∏√≤˙∆∑µƒ◊È≥…£¨Ω¯––¡À»Áœ¬µƒ µ—È£∫£©£Æ
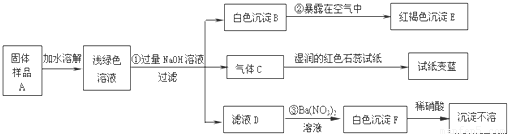
‘ªÿ¥œ¬¡–Œ £∫
£®1£©–¥≥ˆœ¬¡–ŒÔ÷ µƒªØ—ß Ω£∫C______°¢E______°¢F______
£®2£©–¥≥ˆœ¬¡–±‰ªØµƒªØ—ß∑Ω≥Ã Ω£∫
¢⁄______ ¢€______
£®3£©…œ ˆÃΩæøΩ·π˚Àµ√˜—˘∆∑A÷–∫¨”–µƒ¿Î◊””–______£Æ


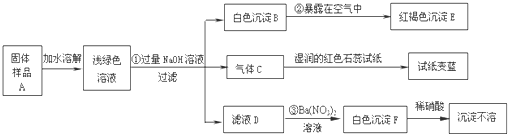

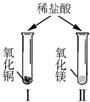 £®2009?ô‘≠£©Œ™¡ÀΩ‚Ω Ù—ıªØŒÔµƒ–‘÷ £¨ µ—È–°◊ȵƒÕ¨—ß√«◊ˆ¡À»ÁÕºÀ˘ æ¡Ω∏ˆ µ—È£¨«Îƒ„∫ÕÀ˚√«“ª∆Ω¯––ÃΩæø£Æ
£®2009?ô‘≠£©Œ™¡ÀΩ‚Ω Ù—ıªØŒÔµƒ–‘÷ £¨ µ—È–°◊ȵƒÕ¨—ß√«◊ˆ¡À»ÁÕºÀ˘ æ¡Ω∏ˆ µ—È£¨«Îƒ„∫ÕÀ˚√«“ª∆Ω¯––ÃΩæø£Æ