ÃΩæø“ª£∫𧓵Ã˙∫ϵƒ÷˜“™≥…∑÷ «Fe
2O
3£¨ªπ∫¨”–…Ÿ¡øµƒFeO°¢Fe
3O
4£Æƒ≥–À»§–°◊È”√≤ðÀ·æßÃÂ÷∆»°CO£¨≤¢Ω¯––¡À»Áœ¬ÕºÀ˘ æ µ—È£Æ

‘ªÿ¥£∫
°æ≤È‘ƒ◊ ¡œ°ø≤ðÀ·æßã®H
2C
2O
4?3H
2O£©‘⁄≈®H
2SO
4◊˜”√œ¬ л»∑÷Ω‚…˙≥…CO
2∫ÕCO£Æ
£®1£© µ—È«∞”¶œ»
ºÏ≤È◊∞÷√µƒ∆¯√Ж‘
ºÏ≤È◊∞÷√µƒ∆¯√Ж‘
£Æ
£®2£©Ω¯»ÎD÷–µƒ∆¯Ã «¥ø檰¢∏…‘ÔµƒCO£¨‘ÚA÷– ‘º¡ «
c
c
°¢C÷–µƒ ‘º¡ «
a
a
£®ÃÓ◊÷ƒ∏±ý∫≈£©£Æ
a£Æ≈®¡ÚÀ· b£Æ≥Œ«Âµƒ ت“ÀÆ c£Æ«‚—ıªØƒ∆»Ð“∫
£®3£©F◊∞÷√µƒ◊˜”√ «
∑¿÷πø’∆¯÷–∂˛—ıªØú°¢ÀÆ’Ù∆¯Ω¯»ÎE◊∞÷√÷–
∑¿÷πø’∆¯÷–∂˛—ıªØú°¢ÀÆ’Ù∆¯Ω¯»ÎE◊∞÷√÷–
£Æ
£®4£©ƒ≥Õ¨—ß»œŒ™Õº æ◊∞÷√”–≤ª◊„÷Æ¥¶£¨∏ƒΩ¯µƒ∑Ω∑® «
‘⁄F∫Û”√æ∆æ´µ∆µ„»º
‘⁄F∫Û”√æ∆æ´µ∆µ„»º
£Æ
ÃΩæø∂˛£∫æ´ªπ‘≠Ã˙∑€ «“ª÷÷÷ÿ“™µƒªØπ§‘≠¡œ£¨ƒ≥–À»§–°◊È∂‘∆‰Ω¯––œ¬¡–—–æø£∫
°æŒÔ÷ ÷∆±∏°ø¿˚”√¬Ã∑Ø÷∆±∏æ´ªπ‘≠Ã˙∑€µƒπ§“’¡˜≥ûÁœ¬£∫

¥÷ªπ‘≠Ã˙∑€÷–ªπ∫¨”–…Ÿ¡øÃ˙µƒ—ıªØŒÔ∫ÕFe
3C‘”÷ £¨ø…”√«‚∆¯‘⁄∏þŒ¬œ¬Ω¯“ª≤Ωªπ‘≠£¨∆‰∑¥”¶∑Ω≥Ã ΩŒ™Fe
xO
y+y H
2x Fe+y H
2O£¨Fe
3C+2H
23Fe+CH
4£Æ
£®1£©–¥≥ˆ±∫…’÷–—ıªØÃ˙”ÎCO∑¥”¶µƒªØ—ß∑Ω≥Ã Ω£∫
£Æ
£®2£©±∫…’÷–º”ΩπÃøµƒ◊˜”√≥˝¡Àø…“‘…˙≥…COÕ‚£¨ªπƒÐ
Ã·π©»»¡ø
Ã·π©»»¡ø
£Æ
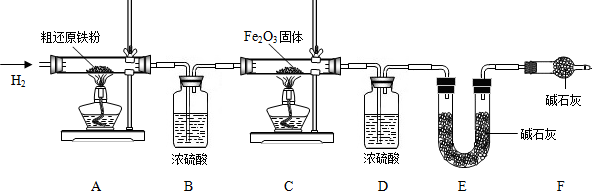
°æ∫¨¡ø≤‚∂®°øŒ™µ√µΩæ´ªπ‘≠Ã˙∑€≤¢≤‚∂®¥÷ªπ‘≠Ã˙∑€÷–—ı∫Õú‘™Àÿµƒ÷ ¡ø∑÷ ˝£¨∞¥»Áœ¬◊∞÷√Ω¯–– µ—È£Æ
“—÷™3CH
4+4Fe
2O
33CO
2+6H
2O+8Fe£®ºŸ…Ë√ø≤Ω∑¥”¶∂ºÕÍ»´£¨«“≤ªøº¬«◊∞÷√ƒ⁄‘≠”–ø’∆¯∂‘≤‚∂®Ω·π˚µƒ”∞œÏ£©£Æ
£®3£©÷˜“™ µ—È≤Ω÷Ë»Áœ¬£∫
¢Ÿ∞¥À≥–Ú◊È◊∞“«∆˜£¨ºÏ≤È◊∞÷√µƒ∆¯√Ж‘£¨≥∆¡ø—˘∆∑∫Õ±ÿ“™◊∞÷√µƒ÷ ¡ø£ª
¢⁄µ„»ºA¥¶æ∆æ´µ∆£ª
¢€ª∫ª∫Õ®»Î¥øæª∏…‘ÔµƒH
2£ª
¢Ðµ„»ºC¥¶æ∆æ´µ∆£ª
¢ð∑÷±œ®√A¥¶°¢C¥¶æ∆æ´µ∆£ª
¢Þ‘Ÿª∫ª∫Õ®»Î…Ÿ¡øH
2£ª
¢þ‘Ÿ¥Œ≥∆¡ø±ÿ“™◊∞÷√µƒ÷ ¡ø£Æ
≤Ÿ◊˜µƒœ»∫ÛÀ≥–Ú «¢Ÿ°˙¢€°˙
B
B
°˙¢ð°˙¢Þ°˙¢þ£®ÃÓ◊÷ƒ∏£©
A£Æ¢⁄°˙¢ÐB£Æ¢Ð°˙¢⁄
£®4£©≤Ω÷Ë¢€µƒƒøµƒ «
≥˝»•◊∞÷√ƒ⁄µƒ—ı∆¯£¨∑¿÷π∑¢…˙±¨’®
≥˝»•◊∞÷√ƒ⁄µƒ—ı∆¯£¨∑¿÷π∑¢…˙±¨’®
£¨—È÷§∏√≤Ω÷˃øµƒ¥ÔµΩµƒ µ—È∑Ω∑® «
’ºØŒ≤∆¯øøΩ¸»º◊≈µƒæ∆æ´µ∆£¨Ã˝…˘“Ù
’ºØŒ≤∆¯øøΩ¸»º◊≈µƒæ∆æ´µ∆£¨Ã˝…˘“Ù
£ª
£®5£©»Ù»±…Ÿ◊∞÷√D£¨‘ÚÀ˘≤‚—ı‘™Àÿµƒ÷ ¡ø∑÷ ˝Ω´
≤ª±‰
≤ª±‰
£®ÃÓ°∞∆´¥Û°Ø°Ø°∞∆´–°°∞ªÚ°∞≤ª±‰°∞£¨œ¬Õ¨£©£Æ
£®6£©¥÷ªπ‘≠Ã˙∑€—˘∆∑µƒ÷ ¡øŒ™20.000g£¨◊∞÷√B°¢E∑÷±‘ˆ÷ÿ0.360g∫Õ0.440g£¨‘Úº∆À„—˘∆∑≥ˆ÷–ú‘™Àÿµƒ÷ ¡ø∑÷ ˝ «
0.6%
0.6%
£¨—ı‘™Àÿµƒ÷ ¡ø∑÷ ˝ «
1.6%
1.6%
£Æ£®ŒÞ–˺∆À„π˝≥ã©£Æ



 x Fe+y H2O£¨Fe3C+2H2
x Fe+y H2O£¨Fe3C+2H2 3Fe+CH4£Æ
3Fe+CH4£Æ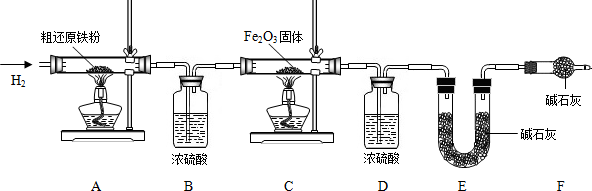
 3CO2+6H2O+8Fe£®ºŸ…Ë√ø≤Ω∑¥”¶∂ºÕÍ»´£¨«“≤ªøº¬«◊∞÷√ƒ⁄‘≠”–ø’∆¯∂‘≤‚∂®Ω·π˚µƒ”∞œÏ£©£Æ
3CO2+6H2O+8Fe£®ºŸ…Ë√ø≤Ω∑¥”¶∂ºÕÍ»´£¨«“≤ªøº¬«◊∞÷√ƒ⁄‘≠”–ø’∆¯∂‘≤‚∂®Ω·π˚µƒ”∞œÏ£©£Æ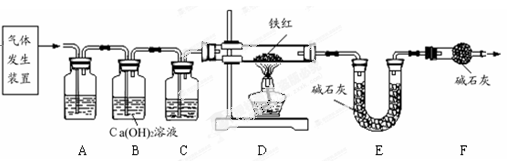

 x Fe + y H2O£¨Fe3C + 2H2
x Fe + y H2O£¨Fe3C + 2H2 3 Fe + CH4°£
3 Fe + CH4°£
 3 CO2 + 6H2O + 8 Fe£®ºŸ…Ë√ø≤Ω∑¥”¶∂ºÕÍ»´£¨«“≤ªøº¬«◊∞÷√ƒ⁄‘≠”–ø’∆¯∂‘≤‚∂®Ω·π˚µƒ”∞œÏ£©°£
3 CO2 + 6H2O + 8 Fe£®ºŸ…Ë√ø≤Ω∑¥”¶∂ºÕÍ»´£¨«“≤ªøº¬«◊∞÷√ƒ⁄‘≠”–ø’∆¯∂‘≤‚∂®Ω·π˚µƒ”∞œÏ£©°£



