
a gСђдкb gбѕЦјжаЧЁКУЭъШЋШМЩеЃЌЩњГЩc gЖўбѕЛЏСђЃЌЯТСаа№ЪіВЛе§ШЗЕФЪЧЃЈЁЁЁЁЃЉ
|
ПЦФПЃКГѕжаЛЏбЇ РДдДЃК ЬтаЭЃК
ПЦФПЃКГѕжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЕЅбЁЬт
| AЃЎaгы bжЎКЭЕШгк c |
| BЃЎЗДгІЧАКѓСђдзгзмЪ§ЁЂбѕдзгзмЪ§ВЛБф |
| CЃЎЗДгІЧАКѓЗжзгзмЪ§ВЛБф |
| DЃЎЗДгІЧАКѓСђдЊЫиКЭбѕдЊЫиВЛБф |
ПЦФПЃКГѕжаЛЏбЇ РДдДЃКЁЖЕк5ЕЅдЊ ЛЏбЇЗНГЬЪНЁЗ2012ФъЕЅдЊВтЪдОэЃЈЪЏСњжабЇЃЉЃЈНтЮіАцЃЉ ЬтаЭЃКбЁдёЬт
ПЦФПЃКГѕжаЛЏбЇ РДдДЃК ЬтаЭЃКЕЅбЁЬт
ПЦФПЃКГѕжаЛЏбЇ РДдДЃКЭЌВНЬт ЬтаЭЃКЬюПеЬт
ПЦФПЃКГѕжаЛЏбЇ РДдДЃК ЬтаЭЃКдФЖСРэНт
ПЦФПЃКГѕжаЛЏбЇ РДдДЃК ЬтаЭЃКНтД№Ьт
ПЦФПЃКГѕжаЛЏбЇ РДдДЃК ЬтаЭЃКдФЖСРэНт

| зщБ№ | вЛ | Жў | Ш§ | ||||||||
| МЏЦјЦПБрКХ | Ђй | Ђк | Ђл | Ђм | Ђн | Ђй | Ђк | Ђл | Ђм | Ђн | Ђй |
| ЦПжаO2еМШнЛ§ЕФЬхЛ§ЗжЪ§ЃЈ%ЃЉ | l0 | 20 | 30 | 40 | 50 | 3l | 33 | 35 | 37 | 39 | 34 |
| ДјЛ№аЧФОЬѕЕФзДПі | ЮЂСС | СС | КмСС | ИДШМ | ИДШМ | КмСС | КмСС | ИДШМ | ИДШМ | ИДШМ | КмСС |

ПЦФПЃКГѕжаЛЏбЇ РДдДЃК ЬтаЭЃКдФЖСРэНт
зЂЩфЦїЪЧвЛжжЦеЭЈЕФвНСЦЦїаЕЃЌЕЋЫќдкЛЏбЇЪЕбщзАжУжаГіЯжЕФдНРДдНЖрЃЌЫќЖдФГаЉЪЕбщЯжЯѓЕФЙлВьЛђЪЕбщЙ§ГЬЕФИФНјЃЌЦ№ЕНСЫвтЯыВЛЕНЕФаЇЙћЁЃ
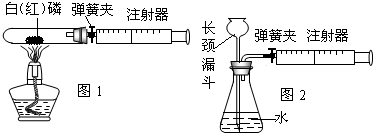
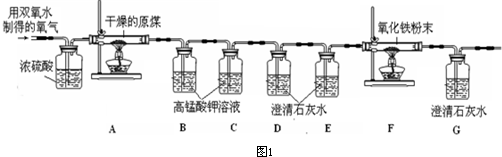
ЃЈ1ЃЉЭМ1гУ50mLЪдЙмзїЗДгІШнЦїЃЌСзЕФШМЩеОљдкУмБеШнЦїРяНјааЃЌПЩЗРжЙАзбЬЮлШОПеЦјЁЃгУ50mLзЂЩфЦїЃЈЛюШћЪТЯШДІдк20mLПЬЖШДІЃЉВтСПСзШМЩеЯћКФЕФбѕЦјЬхЛ§ЁЃ
ВйзїЃКЂйМьВщзАжУЕФЦјУмадЁЃЂкзАШывЉЦЗЃЌСЌКУвЧЦїЁЃЂлМаНєЕЏЛЩМаЃЌМгШШАзСзЃЌЙлВьЪдЙмжаЫљЗЂЩњЕФЯжЯѓЮЊ
ЁЃЂмШМЩеНсЪјЃЌЪдЙмРфШДКѓДђПЊЕЏЛЩМаЃЌПЩвдПДЕНЛюШћТ§Т§зѓвЦЕНдМ mLПЬЖШДІЃЈШЁећЪ§жЕЃЉЁЃЫЕУїПеЦјжабѕЦјЕФЬхЛ§ЗжЪ§дМЮЊ ЁЃ
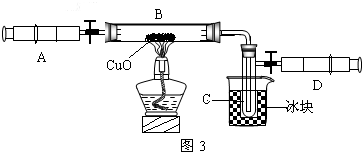
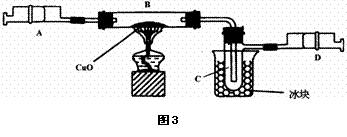
ЃЈ2ЃЉЭМ2гУЭЦРзЂЩфЦїЛюШћЕФЗНЗЈПЩвдМьВщзАжУЕФЦјУмадЁЃЕБЛКЛКЯђЭтРЖЏЛюШћЪБЃЌШчЙћФмЙлВьЕН (бЁЬюађКХ)ЃЌдђЫЕУїзАжУЦјУмадСМКУЁЃ
AЃЎзЂЩфЦїФкгавКЬх BЃЎЦПжавКУцЩЯЩ§
CЃЎГЄОБТЉЖЗФквКУцЩЯЩ§ DЃЎГЄОБТЉЖЗЯТЖЫЙмПкВњЩњЦјХн
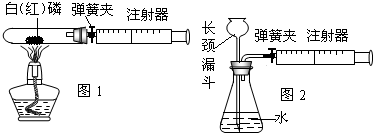
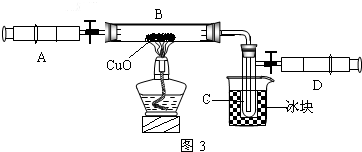
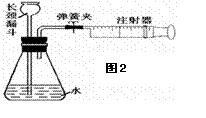
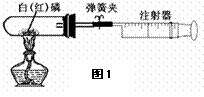
ЃЈ3ЃЉФГбЇЩњЮЊСЫВтЖЈгЩСНжждЊЫиаЮГЩЕФЦјЬЌЛЏКЯЮяXЕФзщГЩЃЌзіСЫШчЭМ3ЫљЪОЕФЪЕбщЁЃЫћАбзЂЩфЦїAжаЕФЦјЬхXЛКТ§ЫЭШызАгаCuOЕФBзАжУЃЌЪЙжЎЭъШЋЗДгІЃЌЕУЕНШчЯТНсЙћЃК
ЂйЪЕбщЧАBЙмМАвЉЦЗЕФжЪСПЮЊ21.32gЃЌЪЕбщКѓЮЊ21.16gЁЃ
ЂкCЙмжаЪеМЏЕНЕФЮяжЪЕчНтКѓЕУЕНH2КЭO2ЃЌдкDжаЪеМЏЕНЕФЪЧN2ЁЃ
ЂлXжаСНдЊЫиЕФжЪСПБШЪЧ14︰3ЃЌЮЪЃК
ⅰЃЎCжаЪеМЏЕНЕФвКЬхЃЌжЪСПЪЧ ЁЁ gЁЃ
ⅱЃЎдкЪЕбщжаПДЕНЕФЯжЯѓЪЧ ЁЃ
ⅲЃЎBжаЗДгІЕФЛЏбЇЗНГЬЪНЪЧ ЁЃ
ЃЈ4ЃЉШЁ8gCuOЗлЮДЃЌашвЊМгШыЖрЩйжЪСП20%ЕФСђЫсШмвКЃЌЧЁКУЭъШЋЗДгІЃП
ЃЈЧыаДГіМЦЫуЙ§ГЬЃЉ
ПЦФПЃКГѕжаЛЏбЇ РДдДЃК ЬтаЭЃКдФЖСРэНт
вбжЊФГЛьКЯН№ЪєЗлФЉжаГ§ТСЭтЛЙКЌгаЬњЁЂЭжаЕФвЛжжЛђСНжжЃЌЫљКЌН№ЪєЕФСПЖМдк5ЃЅвдЩЯЁЃЧыЩшМЦЪЕбщЬНОПИУЗлФЉжаЬњЁЂЭЕФДцдкЁЃ
зЪСЯдкЯпЃКТСгыЧтбѕЛЏФЦШмвКЗДгІЩњГЩШмгкЫЎЕФЦЋТСЫсФЦКЭЧтЦј
ЃЈ2Al+2H2O+2NaOH=2NaAlO2+3H2Ёќ)ЃЌЬњКЭЭВЛгыЧтбѕЛЏФЦШмвКЗДгІЁЃ
ПЩЙЉбЁдёЕФЪЕбщгУЦЗЃКЩеБЁЂДѓЪдЙмЁЂСПЭВЁЂЕЮЙмЁЂШМЩеГзЁЂвЉГзЁЂДХЬњЃЛЯЁСђЫсЁЂЯЁбЮЫсЁЂNa0HШмвКЁЂАБЫЎЁЃ
ЧыФуВЮгыВЂЭъГЩвдЯТЪЕбщЬНОПЙ§ГЬЃК
ЂёЁЂЬсГіМйЩшЁЁЁЁ МйЩш1ЃКИУЛьКЯН№ЪєЗлФЉжаГ§ТСЭтЛЙКЌгаFeЁЃ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ МйЩш2ЃКИУЛьКЯН№ЪєЗлФЉжаГ§ТСЭтЛЙКЌга _________ЁЃ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ МйЩш3ЃКИУЛьКЯН№ЪєЗлФЉжаГ§ТСЭтЛЙКЌгаFeЁЂCuЁЃ
ЂђЁЂЩшМЦВЂЪЕЪЉЪЕбщЗНАИ
(1)ЛљгкМйЩш1ЃЌВЛгУЛЏбЇЪдМСЃЌжЄУїН№ЪєЬњЕФДцдкПЩгУ ____________ ЁЃ
(2)ЛљгкМйЩш2ЃЌНЋЛьКЯН№ЪєЗлФЉМгШызуСПЯЁбЮЫсЃЌФуЙлВьЕНЕФЯжЯѓЪЧ
_____________ЃЌЗДгІЕФЛЏбЇЗНГЬЪНЮЊ ___________ЁЃ
(3)ЛљгкМйЩш3ЃЌЧыФуЭъГЩЪЕбщВйзїЃЌУшЪіЪЕбщЯжЯѓЁЃ
| ЪЕбщВНжш | ЪЕбщВйзїЃЈЫЕУївЧЦїКЭЪдМСЃЉ | ЪЕбщЯжЯѓ | НсТл |
| Ђй | ШЁЩйаэЗлФЉЗХШыДѓЪдЙмжаЃЌдйгУЕЮЙмЕЮМг ЃЌГфЗжЗДгІКѓЃЌОВжУЃЌЦњШЅЧхвКЕУЕН ЙЬЬхЁЃ | ЙЬЬхЗлФЉ ЃЌ ВЂга ЁЃ | НіГ§ШЅТС |
| Ђк | дйЭљДѓЪдЙмжаМг ЃЌГфЗжЗДгІЁЃ | ЙЬЬх ЃЌ ШмвК ЁЃ | жЄУїКЌгаЬњ |
| Ђл | НЋДѓЪдЙмОВжУЃЌЦњШЅЩЯВуЧхвКЃЌМгЫЎЃЌЖрДЮЯДЕгЪЃгрЙЬЬх | ЪЃгрЙЬЬхГЪзЯКьЩЋ | жЄУїКЌгаЭ |
ЂѓЁЂвбжЊИУН№ЪєЗлФЉЕФзщГЩЮЊТСКЭЬњЁЂТСКЭЭСНжжЧщПіЁЃ
ЃЈ1ЃЉЮЊВтЖЈЛьКЯН№ЪєЗлФЉжаТСЕФжЪСПЗжЪ§ЃЌНЋ5.6 gЕФН№ЪєЗлФЉжаМгШы100 gФГШмжЪжЪСПЗжЪ§ЕФЯЁСђЫсЃЌЧЁКУЭъШЋЗДгІЃЌВЂВњЩњa gЧтЦјЃЌдђЯТСаЫЕЗЈе§ШЗЕФЪЧ ( ЁЁ )
AЃЎЕБЗлФЉЮЊAl ЁЂFeЪБЃЌaПЩФмЮЊ0.2 g
BЃЎЕБЗлФЉЮЊAlЁЂCuЪБЃЌЗДгІЭъШЋКѓЃЌЩњГЩЮяЕФШмвКРявЛЖЈКЌгаAl2(SO4)3КЭCuSO4
CЃЎЕБЗлФЉЮЊAlЁЂCuЪБЃЌШєaЮЊ0.3gЃЌдђИУжжЗлФЉжаКЌТСЕФжЪСПЗжЪ§аЁгк50ЃЅ
DЃЎЕБЗлФЉЮЊAlЁЂFeЪБЃЌЫљашЯЁСђЫсШмжЪжЪСПЗжЪ§вЛЖЈДѓгк9.8ЃЅ
ЃЈ2ЃЉШє5.6 gЗлФЉЮЊТСКЭЭЃЌМгШы97.6 gзуСПЕФЯЁСђЫсЃЌЭъШЋЗДгІЩњГЩЧтЦј0.3 gЃЌЧѓЫљЕУAl2(SO4)3ШмвКжЪСПЗжЪ§ЃЈAl2(SO4)3ЯрЖдЗжзгжЪСПЮЊ342ЃЌвЊЧѓгаМЦЫуЙ§ГЬЁЃ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com