
在Cu+2H2SO4=CuSO4+SO2↑+2H2O反应中,反应物和生成物中不存在的物质种类是( )
|
科目:初中化学 来源: 题型:
| ||
| ||
科目:初中化学 来源: 题型:
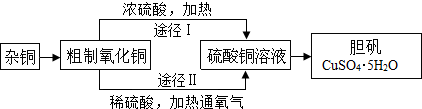
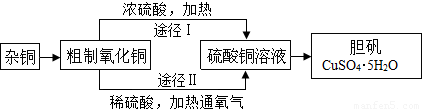
某课外研究小组,用含有较多杂质的铜粉,通过不同的化学反应制取胆矾。其设计的实验过程为:

(1)将杂铜灼烧以除去其中的杂质,此过程中可能产生大量二氧化碳和少量一氧化碳。灼烧后得到的产物是氧化铜及少量铜的混合物,用以制取胆矾。灼烧后含有少量铜的可能原因是 。
a. 灼烧过程中部分氧化铜被还原
b. 灼烧不充分铜未被完全氧化
c. 氧化铜在加热过程中分解生成铜
d. 该条件下铜无法被氧气氧化
(2)由粗制氧化铜制取胆矾可以通过两种途径先得到硫酸铜溶液,进而得到胆矾。
途径Ⅰ的反应:Cu+2H2SO4(浓)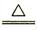 CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
途径Ⅱ的反应:2Cu+O2+2H2SO4(稀) 2CuSO4+2H2O
2CuSO4+2H2O
与途径Ⅰ相比,途径Ⅱ有明显的两个优点是: 、 。
(3)胆矾从物质类别上来说属于 (填“氧化物”“单质”“盐”“混合物”之一)
科目:初中化学 来源:2011-2012学年山东省济南市槐荫区九年级(上)月考化学试卷(12月份)(解析版) 题型:解答题
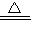 CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O 2CuSO4+2H2O
2CuSO4+2H2O科目:初中化学 来源: 题型:解答题

 CuSO4+SO2↑+2H2O从环保和经济的角度分析,利用途径______
CuSO4+SO2↑+2H2O从环保和经济的角度分析,利用途径______科目:初中化学 来源:2013年贵州省遵义市中考化学试卷(解析版) 题型:填空题
 CuSO4+SO2↑+2H2O从环保和经济的角度分析,利用途径
CuSO4+SO2↑+2H2O从环保和经济的角度分析,利用途径 科目:初中化学 来源: 题型:
 学过金属的活动性顺序以后,东东对其一系列知识进行了研究.
学过金属的活动性顺序以后,东东对其一系列知识进行了研究.
| ||
科目:初中化学 来源: 题型:问答题
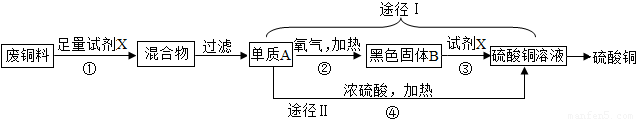
硫酸铜常用作农业杀虫剂,如图是利用含铁废铜料生产硫酸铜的工艺,回答下列问题.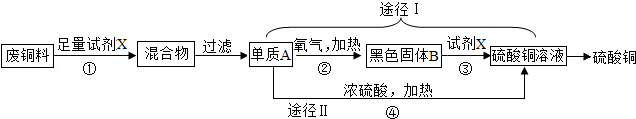
(1)试剂X的化学式是 。
(2)途径Ⅰ中,Cu+2H2SO4 (浓) 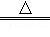 CuSO4+SO2↑+2H2O从环保和经济的角度分析,利用途径 。
CuSO4+SO2↑+2H2O从环保和经济的角度分析,利用途径 。
(填“Ⅰ”或“Ⅱ”)制取硫酸铜更合理;
(3)通常情况下不反应的两种物质,在改变温度和 后,也可能发生反应,如果用足量的铜与20.0溶质质量分数为98.0%的浓硫酸在加热条件下充分反应,实际生成二氧化硫的质量是 (选填字母)。
A.小于6.4g B.等于6.4g C.大于6.4g
科目:初中化学 来源:2013年初中毕业升学考试(贵州遵义卷)化学(解析版) 题型:简答题
硫酸铜常用作农业杀虫剂,如图是利用含铁废铜料生产硫酸铜的工艺,回答下列问题.
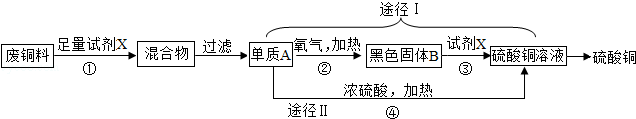
(1)试剂X的化学式是 。
(2)途径Ⅰ中,Cu+2H2SO4 (浓)
 CuSO4+SO2↑+2H2O从环保和经济的角度分析,利用途径 。
CuSO4+SO2↑+2H2O从环保和经济的角度分析,利用途径 。
(填“Ⅰ”或“Ⅱ”)制取硫酸铜更合理;
(3)通常情况下不反应的两种物质,在改变温度和 后,也可能发生反应,如果用足量的铜与20.0溶质质量分数为98.0%的浓硫酸在加热条件下充分反应,实际生成二氧化硫的质量是 (选填字母)。
A.小于6.4g B.等于6.4g C.大于6.4g
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com