
| 以下是关于过滤操作的说法: ①液体缓慢倒入过滤器;②漏斗里的液面要略低于滤纸边缘 ③为了加速过滤,可用玻璃棒搅动漏斗里的液体;④滤纸边缘要稍高于漏斗口 ⑤液体沿着玻璃棒流进过滤器 其中正确的过滤操作是( )
|
科目:初中化学 来源:番禺区二模 题型:单选题
| A.①和④ | B.③和④ | C.①和③ | D.②和⑤ |
科目:初中化学 来源: 题型:单选题
科目:初中化学 来源: 题型:
科目:初中化学 来源:2009年广东省广州市番禺区中考化学二模试卷(解析版) 题型:选择题
科目:初中化学 来源: 题型:阅读理解
烧碱(NaOH)是一种重要的化工原料,广泛应用于肥皂、造纸等工业。下面有一些关于烧碱的问题,请按要求解答:
(1)烧碱在工业上通常用电解饱和NaCl水溶液的方法制取,产物除烧碱外,还有H2和Cl2,请写出电解饱和NaCl水溶液的化学方程式 。(2)烧碱放在空气中会变质生成碳酸钠。现有14.6 g暴露在空气中的烧碱样品,全部溶于水,然后滴加足量Ca(OH)2溶液,充分反应后,过滤,烘干得10 g沉淀,则样品的组成为
A.全部为Na2CO3
B.4 g NaCO3和10.6 g NaOH
C.全部为NaOH
D.4 g NaOH和10.6 g Na2CO3
(3)酸碱中和反应在工农业生产和科研上具有很大用途,但氢氧化钠溶液和盐酸反应时看不到明显现象,请你设计一个实验,通过观察到的明显现象,说明氢氧化钠溶液与盐酸发生了反应。
(4)若中和反应需要60 g 10%的NaOH溶液,现提供50g 20%的NaOH溶液、40 g 5%的NaOH溶液以及足够的NaOH固体和水,请选用以上提供的药品设计两种配制方案(只要说明配制所需的各种药品用量)填入下表中。
| 序号 | 配制方案 |
| 举例 | 6 g NaOH固体和54 g水 |
| 方案1 | |
| 方案2 |
(5)下图是某学生用氢氧化钠固体和水配制60 g10%NaOH溶液的部分操作过程,该同学在称量氢氧化钠时,先在两个托盘上各放一张质量相同的纸,然后把药品直接放在纸上称量。
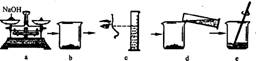
①a操作中的错误是 。
②下列操作中导致溶质质量分数偏低的是 (填字母)。
A.a操作中砝码和氢氧化钠放错盘
B.b中烧杯用水洗涤后未干燥就使用
C.c操作中平视量筒凹液面最低处读数为50 mL
D.d操作中有少量水溅出
科目:初中化学 来源:决胜2005 中考必备化学 题型:043
烧碱
(NaOH)是一种重要的化工原料,广泛应用于肥皂、造纸等工业.下面有一些关于烧碱的问题,请按要求解答:(1)烧碱在工业上通常用电解饱和NaCl水溶液的方法制取,产物除烧碱外,还有H2和Cl2,请写出电解饱和NaCl水溶液的化学方程式_____________________.
(2)烧碱放在空气中会变质生成碳酸钠.现有14.6g暴露在空气中的烧碱样品,全部溶于水,然后滴加足量Ca(OH)2溶液,充分反应后,过滤,烘干得10g沉淀,则样品的组成为
A.全部为Na2CO3
B.4g Na2CO3和10.6g NaOH
C.全部为NaOH
D.4g NaOH和10.6g Na2CO3
(3)酸碱中和反应在工农业生产和科研上具有很大用途,但氢氧化钠溶液和盐酸反应时看不到明显现象,请你设计一个实验,通过观察到的明显现象,说明氢氧化钠溶液与盐酸发生了反应.
________________________________________________.
(4)若中和反应需要60g 10%的NaOH溶液,现提供50g 20%的NaOH溶液、40g 5%的NaOH溶液以及足够的NaOH固体和水,请选用以上提供的药品设计两种配制方案(只要说明配制所需的各种药品用量)填入下表中:
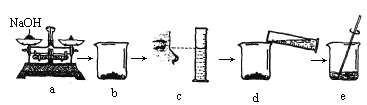
(5)下图是某学生用氢氧化钠固体和水配制60g 10%NaOH溶液的部分操作过程,该同学在称量氢氧化钠时,先在两个托盘上各放一张质量相同的纸,然后把药品直接放在纸上称量.
①
a操作中的错误是________________________________________.②下列操作中导致溶质质量分数偏低的是
________(填字母).A.a操作中砝码和氢氧化钠放错盘
B.b中烧杯用水洗涤后未干燥就使用
C.c操作中平视量筒凹液面最低处读数为50mL
D.d操作中有少量水溅出
科目:初中化学 来源: 题型:阅读理解
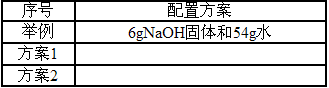
| 序号 | 配置方案 |
| 举例 | 6gNaOH固体和54g水 |
| 方案1 | |
| 方案2 |
科目:初中化学 来源: 题型:解答题
| 序号 | 配置方案 |
| 举例 | 6gNaOH固体和54g水 |
| 方案1 | |
| 方案2 |

科目:初中化学 来源:同步题 题型:实验题
科目:初中化学 来源:化学教研室 题型:058
(1)烧碱在工业上通常用电解饱和NaCl水溶液的方法制取,产物除烧碱外,还有H2和Cl2,请写出电解他和NaCl水溶液的化学方程式:________
(2)烧碱放在空气中会变质生成碳酸钠。现有14.6 g暴露在空气中的烧碱样品,全部溶于水,然后滴加足量Ca(OH)2溶液,充分反应后,过滤,烘干得10 g沉淀,则样品的组成为 ( )
A.全部为Na2CO3 B.4gNa2CO3和10.6gNaOH
C.全部为NaOH D.4g NaOH和10.6g Na2CO3
(3)酸碱中和反应在工农业生产和科研上具有很大用途,但氢氧化钠溶液和盐酸反应时看不到现象,请你设计一个实验,通过观察到的明显现象,说明氢氧化钠溶液与盐酸发生了反应。
______ __
(4)若中和反应需要60g 10%的NaOH溶液,现提供50g 20%的NaOH溶液、40g 5%的NaOH溶液以及足够的NaOH固体和水,请选用以上提供的药品涉及两种配制方案(只要说明配制所需的各种药品的用量)填入下表中
|
序号 |
配制方案 |
|
举例 |
6gNaOH固体和54g水 |
|
方案1 |
|
|
方案2 |
|
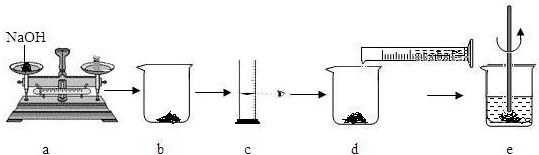
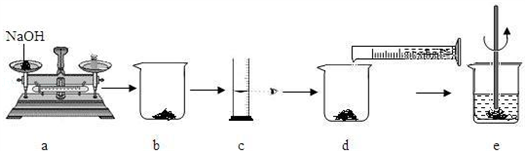
(5)下图是某学生用氢氧化钠固体和水配制60g10%的NaOH溶液的部分操作过程,该同学在称量氢氧化钠时,先在两个托盘上各放一张质量相同的纸,然后把药品直接放在纸上称量。

①操作中的错误是_______;
②下列操作中导致溶质质量分数偏低的是_______。(填字母)
A.a操作中砝码和氢氧化钠放错盘
B.b中烧杯用水洗涤后未干燥就使用
C.c操作中平视量筒凹液面最低处读数为50mL
D.d操作中有少量水溅出
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com