
【题目】下列四个图象分别对应四种操作过程,其中正确的是( )
A. 稀释稀硫酸时pH的变化情况
稀释稀硫酸时pH的变化情况
B.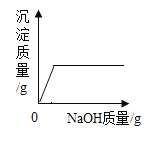 向氯化铁溶液中加入氢氧化钠溶液直至过量
向氯化铁溶液中加入氢氧化钠溶液直至过量
C.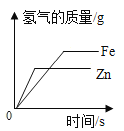 过量锌和铁分别与等量的溶质质量分数相同的稀硫酸反应
过量锌和铁分别与等量的溶质质量分数相同的稀硫酸反应
D.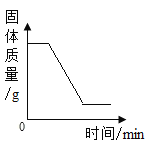 加热一定质量的高锰酸钾固体
加热一定质量的高锰酸钾固体
科目:初中化学 来源: 题型:
【题目】水是地球上最常见的物质之一,下图所示实验中都用到水。下列有关说法错误的是
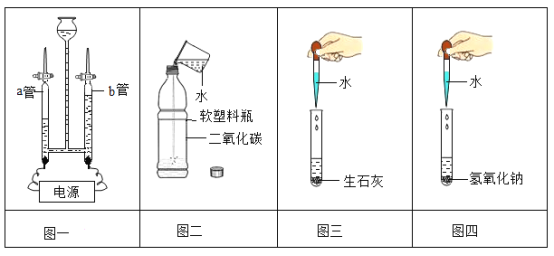
A.图一实验中 b 管内产生的气体有助燃性
B.图二实验加入少量水后,软塑料瓶会变瘪
C.图三实验加入适量水后所得液体可使酚酞溶液变红
D.图四实验中的水参加了化学反应,并放出热量
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有一包金属粉末,可能是由Mg、Al、Zn、Fe中的一种或几种组成。取该金属粉末2.4g与100g稀硫酸充分反应,金属无剩余,生成0.2gH2,得无色溶液。下列说法正确的是( )
A.金属粉末不可能是纯净物B.金属粉末中可能含四种金属
C.稀硫酸的质量分数为9.8%D.若金属粉末中含Al,则一定含Zn
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为测定锌铜合金中锌的含量,取该合金放入如图 14 盛有稀硫酸的锥形瓶中,发生反应: Zn+H2SO4=ZnSO4+H2↑ 。多次实验后,取平均值所得数据如下表:

反应前 | 充分反应后装置及反应剩余物质质量 | |
装置和足量的稀硫酸质量 | 锌铜合金质量 | |
342.10g | 16.00g | 357.70g |
若不考虑干燥剂吸收空气中的水蒸气,计算:
(1)根据质量守恒定律求生成氢气的质量。
(2)该合金中锌的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A-H是中学化学常见的物质,如图是这些物质的相互转化关系图。(其中部分反应条件和部分反应物、生成物已省略)已知:①A是一种氧化物,常用作干燥剂。②D是一种盐,广泛应用于玻璃、造纸、纺织和洗涤剂的生产。根据以下转化关系,请回答:

(1)贝壳的主要成分是_________(填名称)。
(2)写出D的化学式:___________。
(3)写出反应②的化学方程式__________,有关的实验现象为____________。
(4)写出反应③的化学方程式__________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
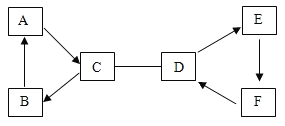
【题目】用A~F六种常见物质,其中A是食品包装中的常用的干燥剂,C与D混合可用来配制农药波尔多液,E是红色固体,它们之间的反应及转化关系如图,(“﹣”表示相连的物质两两之间可以发生反应,“→”表示由某一物质可制得另一物质);
(1)F的化学式为__;
(2)写出下列变化的化学方程式:C与D反应:__;B转化为A:__。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小亮同学对甲烷在氧气中燃烧后的气体产物的成分进行了相关探究(假定燃烧后产物均为氧化物)。
(知识回顾)
写出甲烷在足量的氧气中充分燃烧的化学方程式________________________________。
(实验探究)
小亮设计了下图装置进行实验探究(假定每步均完全反应)。
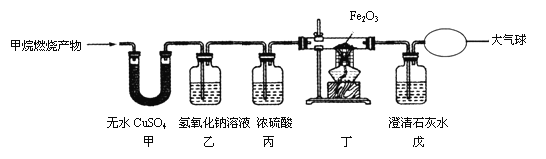
(1)完成实验报告:
实验操作 | 实验现象 | 实验结论 |
将燃烧后的气体 产物进行验证 | 甲中的白色固体变蓝 | 燃烧产物中有_______ |
乙装置质量增加 | 燃烧产物中有CO2 | |
丁中玻璃管内________; 戊中________ | 燃烧产物中有CO |
(2)写出丁中玻璃管内发生反应的化学方程式______________。
(拓展延伸)
实验结束,对相关装置进行称量(忽略空气成分对实验的干扰):甲装置增重5.4g,乙装置增重4.4g。
(1)根据以上数据,写出该实验中甲烷燃烧的化学方程式______________。
(2)若使上述实验中的甲烷充分燃烧,则理论上至少还需要氧气的质量为______________。
(交流与反思)
下列有关家庭使用天然气(主要成分为甲烷)的说法,正确的是___________。
A 天然气无毒,但是燃烧不充分产生CO会使人中毒,因此使用时需要良好的通风
B 天然气如果燃烧不充分,产生的热量会减少,从而浪费了资源
C 天然气泄漏报警器应安装在距地面约0.3米处
D 夜间若发现天然气泄漏,应立即开灯关闭阀门,并打开排气扇
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水和溶液对人类的生产、生活具有重要意义。
(1)鉴别硬水和软水常用的试剂是___。
(2)如图是“水中起火”的实验,实验中白磷能在热水中燃烧,热水的作用是:___。写出白磷燃烧的化学方程式___。
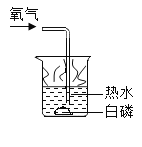
(3)将100g溶质质量分数为30%的过氧化氢溶液,稀释为适用于消毒杀菌的3%溶液,需要加水___g。
(4)下表是碳酸钠在不同温度时的溶解度,根据此表回答:
温度/℃ | 10 | 20 | 30 | 40 |
溶解度/g | 12.2 | 21.8 | 39.7 | 53.2 |
①碳酸钠的溶液随温度的变化趋势是____。
②10℃时将112.2g碳酸钠饱和溶液升温到40℃,至少需要加入质量为_____g的碳酸钠,溶液才能达到饱和。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小惠在帮助学校整理实验的志愿者服务中,发现有一瓶标签破损的硫酸铜溶液,在征得老师的同意后,她对该溶液的溶质质量分数进行了下列探究活动:
取出该溶液50g,向其中逐滴加入溶质质量分数为20%的氢氧化钠溶液,反应过程中生成沉淀的质量与所用氢氧化钠溶液质量的关系如图所示。请回答:
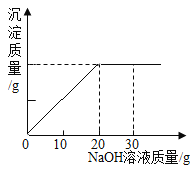
(1)硫酸铜与氢氧化钠恰好完全反应时,用去氢氧化钠溶液_____g;
(2)该硫酸铜溶液中溶质的质量分数是多少?(写出计算过程)
(3)当滴加氢氧化钠溶液质量为21g时,溶液中所含的溶质是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com