
����Ŀ�����ೣ�ӿ�ʯ�л�ȡ�������ϡ�
��1������ұ�����Ľ�������ҵ������Ҫ��Ӧ�Ļ�ѧ����ʽ�ǣ�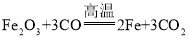 ����Ӧ�е���������_____________���÷�Ӧ�����漰�������У����ڵ��ʵ���________.������������___________.
����Ӧ�е���������_____________���÷�Ӧ�����漰�������У����ڵ��ʵ���________.������������___________.
��2��ͭ���������ý���Ľ�����ľ̿������ͭ��Ӧ���ɶ�����̼�Ļ�ѧ����ʽ��______________________����Ӧ����������_____________(����������������С������������)
��3�������ִ������еõ��㷺��Ӧ�á�����ԭ��ˮ��ʯ����Ҫ�ɷ���Al(OH)3��Al(OH)3��________��Ԫ����ɣ�2mol Al(OH)3�к���_____g��Ԫ�ء�
��4������ұ��ͨ��ʹ��ʯ�н���Ԫ��ת��Ϊ_______(��������������������)̬��
���𰸡�Fe2O3�������� Fe���� CO2�������̼ 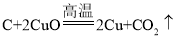 ���� 3���� 96 ����
���� 3���� 96 ����
��������
��1���������Ӧ�У����ǿ��Ը��ݵ�����ʧ�����ж���������������ԭ������������ָ��������ԭ��Ӧ��ʧȥ��Ԫ�ص����ʡ���ԭ����ָ��������ԭ��Ӧ�еõ���Ԫ�ص����ʡ�
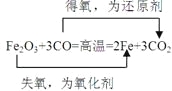
��2���÷�Ӧ�����ڵ��ʵ��ǽ�������Fe����
��3�������������Ƕ�����̼��CO2�����壬���ö�����̼��ȼ��Ҳ��֧��ȼ�յ����ʡ�
��4��ľ̿������ͭ�����ڼ��ȵ������·�Ӧ���ɶ�����̼��ͭ����������ľ̿�Ļ�ԭ�ԣ�
���Է�Ӧ�Ļ�ѧ����ʽΪ��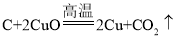 ��
��
��5����Ӧǰ�Ĺ�����CuO����Ӧ�����ɵĹ�����Cu���൱��CuO�Ļ�����ȥ������Ԫ�ص����������Է�Ӧ�������������١�
��6������Al(OH)3�Ļ�ѧʽ��֪�����к���Al��O��H������Ԫ�ء�
��7�����ݻ�ѧʽ��֪��2mol Al(OH)3�к�����Ԫ�ص����ʵ���Ϊ6 mol��������Ϊ16g/ mol��6 mol=96g��
��8������ұ��Ŀ���ǰѽ����Ļ�����ͨ����Ӧת��Ϊ�������ʣ�������Ԫ���ɻ���̬ת��Ϊ����̬��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼװ���о�CO2��������ʡ�

(1)ʵ��1������ƿ�Ǻ����۲쵽��������___________________��
(2)ʵ��2��a��cΪ�������ɫʯ����ֽ��b��dΪʪ�����ɫʯ����ֽ��
ʵ��2˵��������̼�ܶȱȿ�����������ˮ��Ӧ��������__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��һ����ʵ��Ϊ�����Ŀ�ѧ�����ÿ�ѧ��ʵ�鷽�������ǿ��ԴӲ�ͬ�Ƕ���ȷ����ʶ���ʡ�
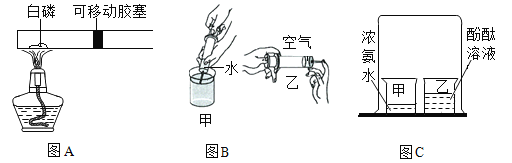
ʵ��һ��̽�����ʵ������ͼA��ʾʵ�飬�����ڲⶨ��������ɡ�
��1��д������ȼ�յ����ֱ���ʽ _____________�÷�Ӧ����__________���Ӧ�������ͣ�
��2����˵�������ǻ���������Ϊ������ȼ�ս�������ȴ�����£�________________��
ʵ�����̽����������
��1��ͼB��ʾʵ�飬�üס�����֧��С��ͬ��ע�������ֱ���ȡ������Ŀ�����ˮ������ָ��סע����ĩ�˵�С�ף�����ͬ��С��������˨���������롣ͨ���Ա���������ʵ�飬���Եó�������ͬ�����£�����������Ŀ�϶��ˮ��__________�����С������
��2��ͼC��ʾʵ�飬�����ձ����м���20mL����ˮ���ٵ��뼸�η�̪��Һ����̪����ɫ��Ȼ�����ձ����м���5mLŨ��ˮ����һ�����ձ���סA��B����С�ձ��������Ӻ۲쵽�ձ�������Һ���ɫ�����۽ǶȽ��Ͳ������������ԭ��_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧС��ͬѧ�ڼ��ȶ���������Ʒʱ�����������ݲ�������ͼһ��ʾ�����������Ƕ�����쳣���������̽����
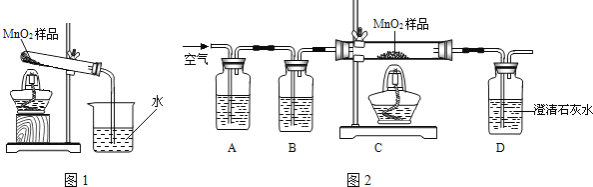
��1��������ɷֵ�̽�������ȶ���������Ʒ����ȼ�ŵ�ľ�������Թܿڣ�ľ��Ϩ�𣮽�����ͨ������ʯ��ˮ������ʯ��ˮ����ǣ������������� ��
��2����������Դ��̽����
��ͬѧ��Ϊ���������������Թ��еĿ������������ʵ��֤���ü��費����
ʵ�鲽�輰���� | ���� |
���ȿյ��Թܣ���һ�˵ij���ʯ��ˮû�б���� | ���� ��������������������� |
��ͬѧ��Ϊ������������Ʒ�п��ܻ���̿�ۣ�̿�۷�����Ӧ�����˸����壮���������ͼ����ʾ��ʵ������о�������Bװ�õ������Ǽ���A�з�Ӧ�Ƿ���ȫ��B�е��Լ��� ��ʵ���й۲쵽D������ʯ��ˮ����ǣ������õ�����������������������ʵ���е��κη�Ӧ�����ظ�����ʵ�飬����D�������ʯ��ˮҲ����ǣ�
ͨ����ͬѧ��ʵ��֤�������������л���̿�ۣ�̿���� ��Ӧ�������������壮
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ��̽������Ʒ��ʴ��������С������ͨ������������ͬʱ�������������ʵ�飬һ��ʱ���ֻ��ʵ��I�й۲쵽�˺��ɫ����ߣ������������Ա仯������˵��������ǣ�������
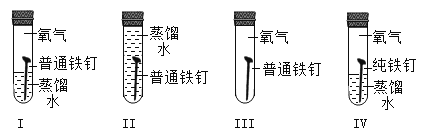
A. I�͢�˵������Ʒ��ʴ��ҪO2
B. I�͢�˵������Ʒ��ʴ��ҪH2O
C. I�͢�˵��H2O��O2ͬʱ���ڣ�����Ʒ��һ��������ʴ
D. ��͢�˵������Ʒ����ʴ������Ʒ�ڲ��ṹ�й�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ݱ�������ѧ���Ѿ����Ƴ���������IJ��ϩ���̼ĤƬ������ֻ��һ��ͷ���Ķ�ʮ���֮һ����ͼ��ʾ������̼ĤƬ��״��䳲������̼ԭ�ӹ��ɵ������ε�Ԫ������չ���ɣ������й�̼ĤƬ��˵���У���ȷ���ǣ�������
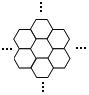
A.̼ĤƬ���ڵ���
B.̼ĤƬ��C60��ͬһ������
C.̼ĤƬ�����˹��ϳɵĻ�����
D.̼ĤƬ����������ȫȼ�յIJ����̼����������ȫȼ�յIJ��ﲻͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ��ʯ��ʯ��Ʒ����Ҫ�ɷ���CaCO3��SiO2��������С��ͬѧ��100g������뵽30gʯ��ʯ��Ʒ�У���֪SiO2�������ᷴӦ��Ҳ������ˮ��ʵ���������Һ��ʧ���Բ��ƣ�����ȫ��Ӧ�����ձ���ʣ������������121.2g������㡣
(1)��Ӧ�����ɵĶ�����̼��������___________��
(2)��ʯ��ʯ��Ʒ��CaCO3����������________________����д��������̣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ��ij��ѧ��ȤС�����A��B����ʵ�飬�۲쵽�˲�ͬ��ʵ������

��1����Aʵ���й۲쵽����ȼ�ո����������Һ����׳���_____________��
��2��ʵ��B������Ϩ���ԭ���Ǽ����Լ�������˴����Ķ�����̼��ͨ����ʵ����Եó�������̼�Ļ�ѧ������__________��
��3��ͨ��A��B����ʵ�飬���Եó���ȼ���ȼ��������_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС��ѧϰ���ᡢ��ε�֪ʶ��ijЩ�ε����ʿ�չ��̽�����
�о����⣻̽��FeCl3��Һ���ȣ����յı仯
�����Ϣ���ƾ�(C2H5OH)���л�ԭ�ԣ���������������Fe3O4��Ӧ��Fe��Fe3O4�ױ�����������FeO��һ�ֺ�ɫ���壬���ܱ�����������Fe3O4�������ᷴӦ�������κ�ˮ��
(1)ʵ��һ������Լ20mL����FeCl3��Һ���������м������������ں�����Һ���������ɫ���ǡ�
��FeCl3��Һ�ʻ�ɫ��Ҫ����Ϊ��Һ�к��������ӣ������ӷ���Ϊ_______��
������ʱ��FeCl3����ˮ��Ӧ���ɺ��ɫ���ʺ����ᣬ��Ӧ�Ļ�ѧ����ʽ��________��
����ʵ����ʾ��FeCl3��Һͨ�������ᾧ�ķ�ʽ______(������������������)���FeCl3���塣
(2)ʵ�������ʵ��һ������õĺ��ɫ����ת�Ƶ����������գ���ɫ�ɺ��ɫ��Ϊ����ɫ��
���˹��̷����ֽⷴӦ�������ɺ���ɫ�����⣬������ˮ����Ӧ�Ļ�ѧ����ʽ��_____��
��������þ��������ͭ�ȼ��ȷֽ�Ҳ�ܵõ���Ӧ�Ľ�����������ʵ�飬������������ܽ����ƶϣ�ͨ�����ȷֽ�_____________�����ɶ�Ӧ�Ľ��������
(3)ʵ������С��ͬѧ�ö��������պȡ����FeCl3��Һ�ھƾ��ƻ��������գ����ż���ʱ��ij�������1�����ڹ۲쵽������������ɫ�ı仯����Ϊ����ɫ�����ɫ������ɫ����ɫ��
��ʵ���������ʵ��һ�Ͷ����ŵ���______(��1�㼴��)
��ͬѧ�ǶԺ�ɫ���ʵijɷֲ��������ʡ���ϵ�ƾ��Ŀ�ȼ�ԡ���ԭ�Ե�������ʣ��Ժ�ɫ���ʵijɷ�����˲��룬��������Ϊ��������____________������Ҳ�ɣ���Fe3O4���������е�һ�ֻ��֡�
��Ϊ��ȷ����ɫ���ʵijɷ֣��ռ���ɫ���ʣ�����������ʵ�飺
ʵ�鲽�� | ʵ������ | ʵ����� |
ȡ��ɫ��ĩ�ô����������۲����� | ��ɫ��ĩȫ������������ | �ۺ�ʵ�������жϣ��˺�ɫ���ʳɷ���____________ |
��װ�к�ɫ��ĩ���Թ��м������������ᣬ��ַ�Ӧ���۲����� | �������ܽ⣬�������ݲ��� |
(4)��չ����
������FeCl3��Һʱ��Ϊ��ֹ���ֺ��ɫ���ʣ��������еμ�������______________����ѧʽҲ�ɣ���Һ��
�������ѧ֪ʶ����Ԫ�ػ��ϼ۱仯�ĽǶȷ�����Fe2O3������ԭ��Ӧʱ����Ӧǰ����Ԫ�ػ��ϼ�һ���_________(���������������½���)�ı仯��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com