
【题目】金属是一种重要的资源。
(1)为减少污染并变废为宝,某化学小组实验探究工业废水的综合利用,设计了以下流程 图并完成了回收金属铜和硫酸锌的实验。
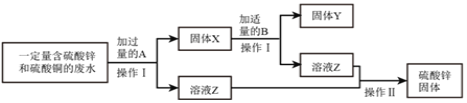
①固体 X 的成分是______;操作Ⅰ需用的玻璃仪器有烧杯、玻璃棒和______。
②上述流程中,在加入适量 B 时反应的化学方程式为______。
③操作Ⅱ中玻璃棒的作用是______。
(2)某同学为探究 Mg、Fe、Cu 三种金属的有关性质,进行了 如图甲所示的实验,实验后把两试管中的物质倒入烧杯中(如 图乙),
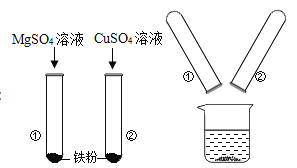
甲 乙
发现烧杯内的红色固体明显增多,充分反应后过滤,滤 液中含有的金属离子的可能组合有______(填字母)。
AMg2+ BMg2+和 Fe2+ CMg2+和 Fe3+ DMg2+和 Cu2+ EMg2+、Fe2+和 Cu2+
【答案】铜、锌 漏斗 Zn+H2SO4=ZnSO4+H2↑ 搅拌使液体均匀受热,防止液体飞溅 BE
【解析】
(1)①锌和硫酸铜反应生成硫酸锌和铜,所以加入的A是锌,所以X的成分为锌、铜,操作Ⅰ分离出了固体和溶液,所以操作I是过滤,需用的玻璃仪器有烧杯、玻璃棒和漏斗;
②由于固体X中含有过量的锌,要得到硫酸锌应除去,应加入稀硫酸,据此写出反应的花絮方程式;
③根据蒸发时分析玻璃棒的应用。
(2)在金属活动性顺序中,氢前的金属能与酸反应生成氢气,金属的位置越靠前,与酸反应生成氢气的速率越大,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,据此分析判断。
(1)①锌和硫酸铜反应生成硫酸锌和铜,所以加入的A是锌,所以X的成分为锌、铜,操作Ⅰ分离出了固体和溶液,所以操作I是过滤,需用的玻璃仪器有烧杯、玻璃棒和漏斗;
②由于固体X中含有过量的锌,要得到硫酸锌应除去锌,应加入稀硫酸,所以在加入适量B时反应的化学方程式为:Zn+H2SO4═ZnSO4+H2↑。
③操作Ⅱ是蒸发,玻璃棒的作用是搅拌使液体均匀受热,防止液体飞溅。
(2)由于镁的活动性大于铁,铁不能与硫酸镁反应;铁的活动性大于铜,铁能将铜从其溶液中置换出来,由题意可知,实验后把两试管中的物质倒人烧杯中(如图乙)发现烧杯内的红色固体明显增多,说明了乙中的铁完全反应了,甲中的铁又与硫酸铜发生了反应。若硫酸铜完全反应了,溶液中的阳离子是:Mg2+和Fe2+;若硫酸铜没有完全反应,溶液中的阳离子是:Mg2+、Fe2+和Cu2+.由以上分析可知,BE正确。
故答为:(1)①铜、锌,漏斗;②Zn+H2SO4═ZnSO4+H2↑;③搅拌使液体均匀受热,防止液体飞溅。(2)BE。


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】根据金属活动性表回答下列问题。
(1)铁比锡的金属活动性_____ (填写“强”或“弱”);
(2)工业炼铁过程中发生 C+CO2 ![]() 2CO 反应,其中碳发生了_____反应(填“氧化”或“还原”);
2CO 反应,其中碳发生了_____反应(填“氧化”或“还原”);
(3)向 AgNO3、Cu(NO3)2 和 KNO3 混合溶液中加入铝粉和铁粉,充分反应后过滤, 得到无色滤液, 则滤渣中一定含有的金属是_____, 滤液中一定含有的溶质是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】钋广泛用于抗静电刷。钋元素的信息如图所示,下列说法错误的是

A. 属于金属元素 B. 质子数为84
C. 核外电子数为84 D. 相对原子质量为209g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据如图所示制取气体的装置,回答下列问题(装置选择用序号填写):
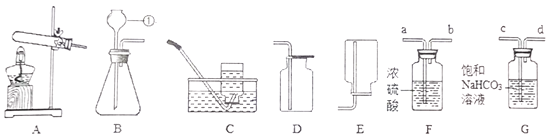
(1)实验仪器①的名称是_____________
(2)用高锰酸钾制取氧气时,选择的发生装置为_____,排空气法收集氧气,应选用的装置是____,验满的方法是__________________________________________________
(3)用大理石和稀盐酸制取二氧化碳时,反应的化学方程式为________________________________
若装置B中反应剧烈,从实验可行性和安全角度考虑,可采取的措施有_________(填序号)。
①用容积较小的锥形瓶 ②将大理石进一步粉碎 ③加热反应物
④降低液体反应物的浓度 ⑤用稀硫酸代替稀盐酸
(4)采用上述方法制取的二氧化碳中常含有氯化氢气体和水蒸气,为获得纯净、干燥的二氧化碳气体,可选用如图所示的F装置和G装置进行除杂和干燥,导管囗连接的正确顺序是:
气体→_____→______→______→______→D(填小写字母),除杂过程中发生反应的化学方程式是________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】a、b、c三种不含结晶水的固体物质的溶解度曲线如图,下列说法正确的是( )
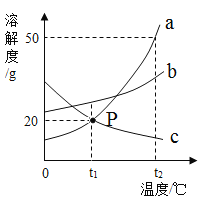
A.![]() 时,a、c饱和溶液中溶质质量相等
时,a、c饱和溶液中溶质质量相等
B.![]() 时,将30ga物质加入到50g水中充分搅拌,得到80ga的饱和溶液
时,将30ga物质加入到50g水中充分搅拌,得到80ga的饱和溶液
C.![]() 时等质量的三种饱和溶液降温至
时等质量的三种饱和溶液降温至![]() ,所得溶液中溶剂质量
,所得溶液中溶剂质量![]()
D.将![]() 时a、b、c三种物质的溶液分别升温至
时a、b、c三种物质的溶液分别升温至![]() ,其溶质质量分数都不可能发生变化
,其溶质质量分数都不可能发生变化
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列四个图像分别对应四个变化过程,其中错误的是( )
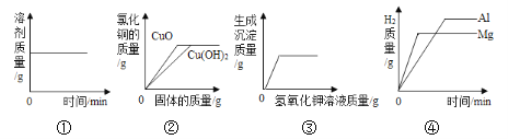
A. ①表示将一定量的 60℃硝酸钾饱和溶液冷却至室温
B. ②表示向相同质量和相同质量分数的稀盐酸中,分别加入过量 Cu(OH)2和 CuO 固体
C. ③表示向一定量的氯化铁和盐酸的混合溶液中,逐滴加入过量的氢氧化钾溶液
D. ④表示向相同质量和相同质量分数的稀硫酸中,分别加入过量的镁粉和铝粉
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】据科技部2月15日公布的消息,法匹拉韦(化学式为C5H4FN3O2)是继磷酸氯喹和瑞德西韦之后第三个获准用于治疗新冠肺炎的西药,该药对新冠肺炎的治疗显示出较明显的疗效和较低的不良反应。下列有关法匹拉韦的说法正确的是( )
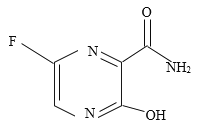
A.法匹拉韦中含有氧分子
B.法匹拉韦的相对分子质量为157g
C.1个法匹拉韦分子由15个原子构成
D.法匹拉韦中氮、氧元素的质量比是3:2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学反应的微观过程如下图(其中“![]() ”代表氢原子,“
”代表氢原子,“![]() ”代表氮原子,“
”代表氮原子,“![]() ”代表氧原子),下列叙述中,正确的是
”代表氧原子),下列叙述中,正确的是
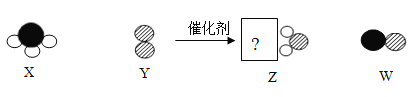
A.该反应类型为置换反应
B.该反应中氧元素的化合价发生了变化
C.所得生成物Z和W的质量比为9:15
D.该反应中原子、分子种类都未发生变化
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“配制一定质量分数的溶液”和“粗盐中难溶性杂质的去除”是初中化学的基础实验,请回答下列问题:
(1)“粗盐中难溶性杂质的去除”实验步骤:
①溶解称取5.0g粗盐,逐渐加入10mL水中,直到不再溶解,剩余粗盐1.2g。
②过滤。
③蒸发,请从溶解度的角度分析,实验中不采用降低溶液温度的方法得到精盐的依据是________。
④计算产率得到精盐3.2g,则精盐的产率为__________(计算结果保留一位小数)。
(2)整个实验中至少要进行__________次称量。
(3)从海水中获胜得的粗盐,经过上述实验得到精盐属于__________(填“混合物”或“纯净物”)。
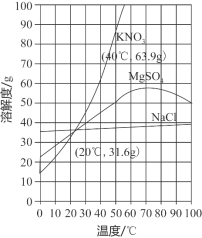
(4)根据如图所示溶解度曲线,40℃时,向装有50g水的烧杯中加入25gKNO3固体,充分搅拌后,所得溶液的溶质质量分数为_____%(精确到0.1%),将该溶液降温至20℃时,析出KNO3晶体的质量为____g。
(5)若用溶质质量分数为16%的KNO3溶液和蒸馏水配制100g溶质质量分数为10%的KNO3溶液,则需要取蒸馏水的体积为__________ml。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com