

分析 根据A、B、C、D、E 初中化学常见的物质,B是一种氧化物,相对分子质量为44,B中两元素质量比为3:8,所以B是二氧化碳,人体胃酸中含有D,可帮助消化,所以D是盐酸,生活中F是一种最常见的溶剂,所以F是水,F和G的组成元素相同,G会转化成F,所以G是双氧水;双氧水分解可以生成水和氧气,所以C是氧气,A和E都是由三种元素组成的化合物,E和二氧化碳可以互相转化,所以E可以是碳酸钠,A和碳酸钠也可以相互转化,所以A是氢氧化钠,然后将推出的物质进行验证即可.
解答 解:(1)A、B、C、D、E 初中化学常见的物质,B是一种氧化物,相对分子质量为44,B中两元素质量比为3:8,所以B是二氧化碳,人体胃酸中含有D,可帮助消化,所以D是盐酸,生活中F是一种最常见的溶剂,所以F是水,F和G的组成元素相同,G会转化成F,所以G是双氧水;双氧水分解可以生成水和氧气,所以C是氧气,A和E都是由三种元素组成的化合物,E和二氧化碳可以互相转化,所以E可以是碳酸钠,A和碳酸钠也可以相互转化,所以A是氢氧化钠,经过验证,推导正确,所以D是HCl,F是H2O;
(2)G→C的反应是过氧化氢在二氧化锰的催化作用下生成水和氧气,化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)A与D的反应是氢氧化钠和盐酸反应生成氯化钠和水,化学方程式为:HCl+NaOH=NaCl+H2O,该反应放出热量;
(4)C是氧气,能够支持燃烧和呼吸,常用于医疗急救、炼钢等.
故答案为:(1)HCl,H2O;
(2)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)HCl+NaOH=NaCl+H2O,放出;
(4)医疗急救、炼钢等.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:推断题
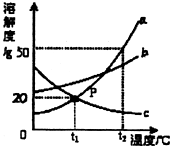 根据图中a、b、c三种物质的溶解度曲线,回答下列问题:
根据图中a、b、c三种物质的溶解度曲线,回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
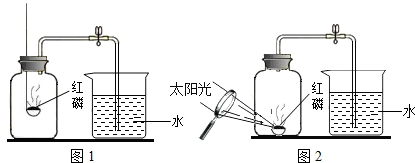
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 某实验小组欲证明氧化铜能加快氯酸钾的分解,他们进行了如下实验:
某实验小组欲证明氧化铜能加快氯酸钾的分解,他们进行了如下实验:| 编号 | KClO3质量(g) | 其他物质质量(g) | 待测数据 |
| 1 | 2.0 | ||
| 2 | 2.0 | CuO 0.5 | |
| 3 | 2.0 | MnO2 0.5 |
| 实验步骤 | 设计这一步骤的目的 |
| 以上实验表明,加入CuO后产生O2的速率比未加入时快得多 | CuO能加快KClO3的分解 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 手持试管,应垂直拿稳 | |
| B. | 手拿试剂瓶,标签向外,以防腐蚀标签 | |
| C. | 试剂瓶口不要紧贴试管口,以防污染 | |
| D. | 把试剂瓶塞拿下,倒放在桌面,用完立即将瓶塞盖上 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 组别 | 药品 | 实验现象 |
| ① | 块状石灰石和稀盐酸 | 产生气泡速率适中 |
| ② | 块状石灰石和稀硫酸 | 产生气泡速率缓慢并逐渐停止 |
| ③ | 碳酸钠粉末和稀盐酸 | 产生气泡速率很快 |

查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com