
【题目】(4分)下图为A、B、C三种物质的溶解度曲线,据图回答:
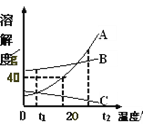
(1)200C时,A的饱和溶液中溶质的质量分数是 。
(2)20℃时,将25g A物质放入50g水中,充分搅拌,所得溶液的质量是 g。
(3)若将t10C三种物质的饱和溶液分别升温到t20C时,则三种溶液中溶质的质量分数由小到大的顺序是 。
(4)要从A物质中混有少量B物质得到A用 方法。
【答案】(1)28.6% (2)70克 (3)C A B (4)冷却热饱和溶液
【解析】试题分析:(1)根据溶解度曲线,200C时,A的溶解度为40g,故A的饱和溶液中溶质的质量分数=40g/140g×100%=28.6%
(2)根据溶解度曲线,200C时,A的溶解度为40g,说明在100g水中达到饱和状态溶解A的质量为40g,故50g水最多只能溶解20gA,将25g A物质放入50g水中,充分搅拌,所得溶液的质量是70克
(3)根据溶解度曲线,物质A、B的溶解度都随温度的升高而增大,故将t10CA、B两种物质的饱和溶液分别升温到t20C时,都由饱和溶液变为不饱和溶液,但溶液中的溶质和溶剂质量不变,即溶质质量分数也不变,所以只要比较它们在t10C 时的溶解度大小关系即可,在t10C 时:B的溶解度大于A,则溶质质量分数B也大于A ,而对于C而言,溶解度随温度的升高而降低,故t10C升温到t20C,由溶质析出,溶质质量分数减小,本在t10C时,物质C的溶解度就最小,溶质质量分数最小,故若将t10C三种物质的饱和溶液分别升温到t20C时,则三种溶液中溶质的质量分数由小到大的顺序是:C A B
(4) 根据溶解度曲线,物质A的溶解度都随温度的升高变化较大,而物质B的溶解度都随温度的升高变化不大,故要从A物质中混有少量B物质得到A用冷却热饱和溶液方法


科目:初中化学 来源: 题型:
【题目】某小组进行了如下实验,请回答下列问题
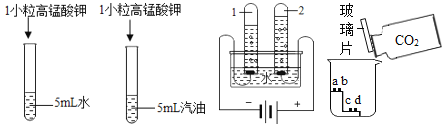
a、c为干燥的紫色石蕊试纸b、d为湿润的紫色石蕊试纸
(1)甲实验说明_____
(2)乙实验,若电解18g水,则试管2内得到的气体质量为_____g
(3)丙实验中,说明二氧化碳密度大于空气且能与水反应的现象是_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了测定某碳酸钠样品中杂质氯化钠的质量,李明同学进行了三次实验,反应的化学方程式为:Na2CO3+CaCl2===CaCO3↓+2NaCl。实验数据如下表:
编号 | 第1次 | 第2次 | 第3次 |
所取固体样品的质量/g | 7 | 5 | 5 |
加入氯化钙溶液的质量/g | 50 | 50 | 75 |
反应后生成沉淀的质量/g | 4 | 4 | 4 |
完成下列计算:
(1)碳酸钠样品中碳酸钠的质量是多少?
(2)第三次实验中充分反应后所得溶液中氯化钠的质量分数是多少?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室常用下图所示的装置制取并收集气体。请回答:
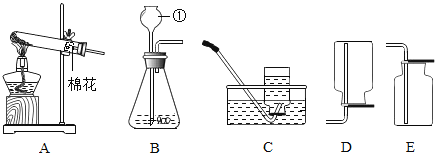
(1)仪器①的名称 。
(2)实验室若用A、C装置组合制取并收集氧气,其反应的原理为(用化学方程式表示)
,待收集完氧气后,应先从水槽中撤出玻璃管,再停止加热的原因是 。
(3)实验室制取并收集二氧化碳应选择的装置组合是 ,检验二氧化碳是否收集满的方法是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某兴趣小组向甲、乙试管中各加入2mL 10%的CuSO4溶液,再向两支试管中加入10%的NaOH溶液,甲试管中加入5mL、乙试管中加入2滴,振荡后观察到甲试管中有蓝色沉淀生成,乙试管中有浅绿色沉淀生成。
(实验讨论)得到的蓝色沉淀一定是氢氧化铜,写出反应的化学方程式:_____,那么浅绿色沉淀是什么呢?
(查阅资料)(1)NaOH溶液和CuSO4溶液反应可生成碱式硫酸铜,它是浅绿色固体,受热会分解;
(2)碱式硫酸铜有多种可能的组成,如Cu2(OH)2SO4、Cu3(OH)4SO4或Cu4(OH)6SO4;
(3)SO2气体能使酸性高锰酸钾溶液褪色。
(实验探究)该小组对碱式硫酸铜产生了兴趣,想探究碱式硫酸铜受热分解的产物。
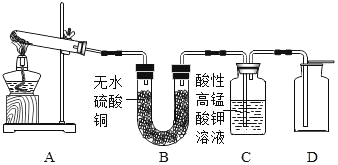
(实验设计)取少量碱式硫酸铜加入试管中并按以下流程进行实验:
实验结束后,试管A中残留有黑色固体,滴入稀硫酸后观察到_____的现象,证明该黑色固体是氧化铜;B中无水硫酸铜变为蓝色,证明有水生成;C中酸性高锰酸钾溶液褪色,证明生成_____;D中气体能使带火星木条复燃,证明有_____生成;
(实验反思)
(1)当NaOH溶液和CuSO4溶液反应时,只要CuSO4溶液的量一定,NaOH溶液_____(填“过量”或“不足”)时就能生成浅绿色沉淀;
(2)碱式硫酸铜可表示为:aCu(OH)2bCuSO4,如将Cu4(OH)6SO4改写该表示方式,则a与b的比值为_____;
(拓展延伸)当反应物的量不同,产物可能不同,试另举一个例子:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属在日常生活中有着广泛的用途。常见金属的活动性顺序如下:

请回答下面问题:
(1)金属活动性顺序表中的X是_____元素。(填元素符号)
(2)把一根用砂纸打磨过的铝丝浸入硫酸铜溶液中,该反应的化学方程式为_____。
(3)向一定质量AgNO3和Cu(NO3)2的混合溶液中加入过量的Zn粉,溶液质量随反应时间的变化情况如图2所示。图中B点溶液中含有的溶质有_____。
(4)非金属单质也具有类似金属与盐溶液之间发生置换反应的规律,即活动性较强的非金属可把活动性较弱的非金属从其盐酸溶液中置换出来,如在溶液中可发生下列反应:Cl2+2NaBr═2NaCl+Br2、I2+Na2S═2NaI+S↓、Br2+2KI═2KBr+I2由此判断S、Cl2、I2、Br2四种单质中非金属活动性最强的是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是“尾气催化转换器”将汽车尾气中有毒气体转变为无毒气体的微观示意图,其中不同的圆球代表不同原子。下列说法错误的是
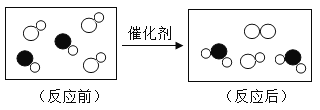
A. 此反应有单质生成
B. 原子在化学变化中是不可分的
C. 图中生成物全部是化合物
D. 参加反应的两种分子的个数比为1∶1
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、C、D、E、X、Y、Z都是初中化学中的常见物质,其中A是天然气的主要成分,X、Y、Z是单质,B、C、D、E是氧化物,常温下C是液体,Y是黑色固体,E是红棕色粉末。它们之间有如下反应关系:

请根据以上信息回答下列问题:
(1)有关物质的化学式:A为_____,C为_____。
(2)B与Y反应的化学方程式为_____,D与E反应的化学方程式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学研究性学习小组同学取 10g 石灰石样品,用足量的稀盐酸测定石灰石中碳酸钙的质量分数(假设石灰石中杂质不与盐酸反应)。测量 5 分钟内生成 CO2 质量的数据如表:
时间/分钟 | 1 | 2 | 3 | 4 | 5 |
生成 CO2 的质量/g | 1.5 | 2.5 | 3.0 | 3.3 | 3.3 |
请回答下列问题:
(1)石灰石中的 CaCO3 完全反应时,生成二氧化碳气体的物质的量为_____mol。
(2)该石灰石中 CaCO3 的质量分数是多少?(根据化学方程式列式计算)_____。
(3)请根据表中数据分析,你能发现数据背后的化学反应规律是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com