
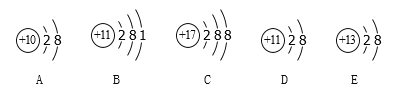
【题目】根据下列微粒的结构示意图,回答下列问题。
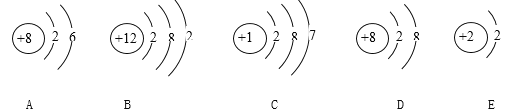
(1)图中共表示了____ 种元素的微粒,其中表示阴离子的是_______(填序号,下同),稀有气体原子的是_______。
(2)B微粒的质子数为_____,B是 _____元素(填“金属”“非金属”“稀有气体”),B原子在化学反应中形成离子的符号为_______。
(3)化学性质达到相对稳定的有_____填序号)。
【答案】4 D E 12 金属 Mg2+ DE
【解析】
在原子结构示意图中,小圆圈表示原子核,圆圈内的数字为质子数;弧线表示电子层,弧线上的数字为该层上的电子数。最外层电子数决定原子的化学性质,质子数决定元素的类别。
(1)图中共表示了4种元素的微粒,同一原子中,质子数=核外电子数=核电荷数=原子序数;在阳离子中:质子数>核外电子;在阴离子中:质子数<核外电子;其中表示阴离子的是D,原子核外只有一个电子层且电子数为2,或者最外层电子数为8的结构为稳定结构,有稳定结构的原子为稀有气体原子,E表示的微粒为稀有气体原子;
(2)B微粒的质子数为12,当原子的最外层电子数小于4时,反应中易失去电子成为阳离子,属于金属原子,统称金属元素,B是金属元素;离子是由原子的是电子形成的,失去电子时带正电荷,正电荷数等于失电子数,B原子在化学反应中形成离子的符号为Mg2+;
(3)原子核外只有一个电子层且电子数为2,或者最外层电子数为8的结构为稳定结构,微粒的化学性质稳定,所以化学性质达到相对稳定的有DE。


科目:初中化学 来源: 题型:
【题目】根据分子和原子的知识,下列叙述错误的是( )
A. 10mL酒精和10mL水混合,体积小于20mL,说明分子间有间隔
B. 夏天汽车轮胎容易膨胀,是温度升高,气体分子间隔变大
C. 墙内花开墙外香,是因为分子在不断运动
D. 分子的质量很小,一个水分子的质量约是![]()
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】草酸亚铁晶体(FeC2O42H2O)是一种浅黄色固体,难溶于水,受热易分解,是生产锂电池的原材料,某化学兴趣小组设计实验验证草酸亚铁晶体热分解的气体产物,并用热重法(TG)确定其分解后所得固体产物的组成,探究过程如下:
(查阅资料)
①硫酸铜晶体(CuSO45H2O)受热时会发生如下反应: CuSO45H2O![]() CuSO4+5H2O草酸亚铁晶体(FeC2O42H2O)也能发生类似的反应;
CuSO4+5H2O草酸亚铁晶体(FeC2O42H2O)也能发生类似的反应;
②草酸亚铁晶体热分解的气体产物是H2O,CO,CO2;
③白色的无水CuSO4遇水蒸气会变成蓝色;
④浓硫酸具有吸水性,是常用的气体干燥剂;
⑤浓的氢氧化钠溶液易吸收大量的二氧化碳气体,比石灰水吸收效果好。
(实验设计)
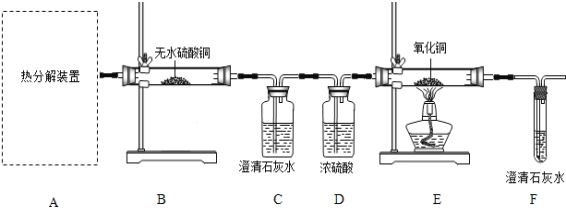
(1)从环保角度考虑,该套实验装置的明显缺陷是_______。
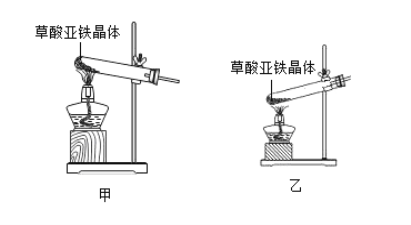
(2)可选择以下实验装置中的_____(选填“甲”或“乙”)作为虚线中的“热分解装置”。
(问题讨论)
(3)实验过程中如果观察到以下现象:B中白色无水CuSO4变成蓝色,___________,E中黑色粉末变成红色,则可证明草酸亚铁晶体热分解的气体产物是H2O,CO,CO2;写出F装置中所发生反应的化学方程式_________。
(4)该兴趣小组进行上述实验时,应先点燃__________处(填“A”或“E”)的酒精灯,原因是____________。
(5)若通过F装置中澄清石灰水变浑浊来证明草酸亚铁晶体热分解的气体产物中有CO,则需对实验设计方案进行改进,请说出你的改进措施________。
(数据分析)
(6)称取3.60g草酸亚铁晶体(FeC2O42H2O,相对分子质量是180)用热重法对其进行热分解,得到剩余固体的质量随温度变化的曲线如图所示,请分析该图回答下列问题:
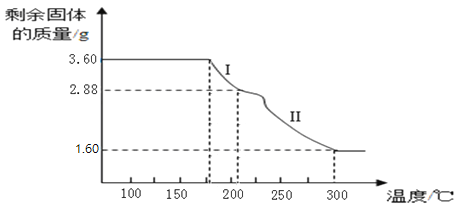
①过程Ⅰ发生反应的化学方程式为____________。
②已知:300℃时草酸亚铁晶体完全分解后剩余固体只有一种且是铁的氧化物。通过计算可确定该氧化物为_____________(填名称)。(请写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】通过化学学习我们认识了许多的物质,请回答以下问题
(1)在汽油中加入适量乙醇就得到乙醇汽油,使用乙醇汽油可节省石油资源,写出乙醇燃烧的化学方程式___________。
(2)很多天然矿石中含有碳元素,菱锰矿的主要成分是碳酸锰( MnCO3),其中锰元素的化合价________ 。
(3)炭雕是活性炭成型技术与传统雕刻工艺的完美结合,因为活性炭有疏松多孔的结构,具有_____能力,所以,炭雕既可以净化室内空气,又可以美化居住环境。

(4)钛及钛合金被称为“未来金属”,用其制造的潜艇、军舰没有磁性,不会被磁性水雷发现,这是利用钛的_________(填“物理”或“化学”)性质。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在今年五校“庆元旦 贺新年”联欢晚会上,戴校长给同学们表演了一个魔术:大烧杯中盛有一只燃着的蜡烛和一团包有过氧化钠(Na2O2)的棉花,将一瓶二氧化碳倒入烧杯中,蜡烛慢慢的熄灭,然后棉花突然剧烈的燃烧起来。这出乎意料的现象引起了同学们的极大兴趣,请你参与同学们的讨论和探究。
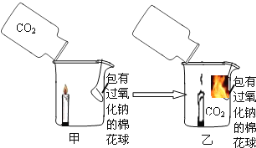
蜡烛熄灭的原因是__________。
(提出问题)棉花为什么会燃烧?
(提出猜想)
(1)可能是蜡烛燃烧引燃了棉花。
(2)_________________。
(3)可能是二氧化碳与过氧化钠反应生成了氧气。
(实验验证)
序号 | 实验操作 | 主要实验现象 | 实验结论及解释 |
① | 按下图装置进行实验
| 无现象 | 猜想﹙1﹚___ ﹙填成立或不成立﹚ |
② | 向盛满二氧化碳的集气瓶中加入适量的过氧化钠粉末,充分震荡,并___________________ | 感觉发烫 | 猜想﹙2﹚成立 |
③ | _____________ | _________ | 二氧化碳与过氧化钠反应生成了氧气,猜想﹙3﹚成立 |
(实验结论)
(1)CO2 与Na2O2反应生成了氧气与碳酸钠,化学方程式为__________。
(2)通常CO2可作灭火剂,但有些物质(如Na2O2)着火,不能用CO2熄灭。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】点燃两支蜡烛,分别放在白铁皮架的两个阶梯上,把白铁皮架放在烧杯里(如图所示)。沿烧杯内壁缓缓倾倒二氧化碳。
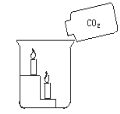
(1)向烧杯中倾倒二氧化碳时,观察到的现象是: ____________
(2)该实验说明:_____________________
(3)由上述结论可推断CO2的重要用途之一是 ___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】中兴缺“芯”事件震惊国人。芯片是电脑、智能家庭等的核心部件,芯片的主要成分是纯度极高的硅,其运算速率与硅的纯度有关。
(1)硅与金刚石结构相似,则构成硅的粒子是__________(填粒子名称)。
已知硅原子结构示意图为![]() 下面是四种粒子的结构示意图,其中与硅的化学性质相似的是_______(填序号)。
下面是四种粒子的结构示意图,其中与硅的化学性质相似的是_______(填序号)。
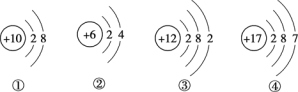
(2)光伏发电的太阳能电池板也需用高纯硅。在日光下高纯硅的作用主要是将光能转化为________能。
(3)自然界中的硅元素主要以二氧化硅的形式存在,请写出二氧化硅的化学式___。硅胶是常用的干燥剂,其主要成分可视作二氧化硅(如图),你认为硅胶可作干燥剂的原因可能是__________(一条即可)。

(4)高纯硅的制备以石英砂(主要成分是二氧化硅)为原料,生产过程示意图如下:

①上述四个步骤中属于物理变化的是_____________。
②物质M是该生产过程中可循环使用的物质,写出步骤4反应的化学方程式_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业上生产电石(CaC2)并制备重要工业原料乙炔(CxHy)流程如图1所示:
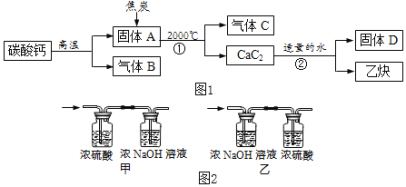
(资料)
(1)碳酸钙高温分解可得两种氧化物。
(2)浓硫酸具有强吸水性,NaOH溶液能吸收CO2。
(讨论)(1)C、B组成元素相同,C有毒,反应①化学方程式为_________。
(2)D微溶于水,溶解度随温度升高而减小,D的化学式是_________。
(测定乙炔组成)
资料:一个乙炔分子有四个原子构成。
(3)将一定量的乙炔(CxHy)完全燃烧,并将生成的气体缓缓通过如图2所示的____(选填“甲”或“乙”)装置,并再缓缓通一段时间的N2,并记录实验数据于如表中。
装置 | 反应前质量 | 反应后质量 |
浓硫酸 | 125.3g | 127.1g |
浓NaOH溶液 | 78.2g | 87.0g |
(4)实验中“缓缓通一段时间的N2”的目的是_________。
(5)计算:乙炔中碳元素质量为_____g,氢元素质量为_____g
(6)乙炔的化学式为______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请根据下列粒子的结构示意图。回答问题。
(1)属于同种元素的是____________。
(2)表示稀有气体元素原子的是__________。
(3)由C和E形成化合物的化学式为________。
(4)写出D所表示粒子的符号________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com