
【题目】氯化亚铜(CuCl)是一种白色粉末,不溶于水、乙醇(标准状况下沸点是78.2℃)及稀硫酸,熔点422℃,沸点1366℃,在空气中迅速被氧化成绿色,常用于有机合成工业中的催化剂。以粗盐水(含氯化钙、硫酸镁等杂质)、Cu、稀硫酸、SO2等为原料合成CuCl的工艺流程如下:
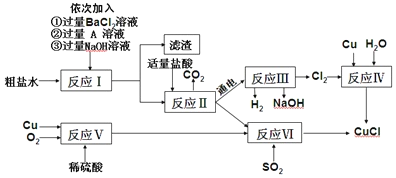
⑴A溶液中溶质的化学式是____________;
⑵写出反应III的化学方程式__________________________;
⑶反应VI的化学方程式是:2NaCl+2CuSO4+SO2+2H2O=2CuCl↓+2H2SO4+Na2SO4,反应中化合价升高的元素是_____________;
⑷本工艺中可循环利用的物质是NaOH和_____________;
⑸反应VI后,过滤得到的CuCl沉淀,用无水乙醇洗涤沉淀,在真空干燥机内于70℃干燥2小时,冷却密封包装即得产品。真空干燥的目的是_____________________。
【答案】 Na2CO3 2NaCl+2H2O ![]() 2NaOH+Cl2↑+H2↑ 硫 硫酸 防止氯化亚铜被氧化(加快乙醇和水的蒸发 ) 。
2NaOH+Cl2↑+H2↑ 硫 硫酸 防止氯化亚铜被氧化(加快乙醇和水的蒸发 ) 。
【解析】(1)加入氯化钡溶液可以除去硫酸根离子,加入碳酸钠溶液可以除去钙离子和过量的钡离子,加入氢氧化钠溶液可以除去镁离子,因此A溶液是碳酸钠溶液,碳酸钠的化学式是Na2CO3;(2)反应III中,电解饱和食盐水时,氯化钠和水反应生成氢氧化钠、氢气和氯气,反应的化学方程式为:2NaCl+2H2O ![]() 2NaOH+Cl2↑+H2↑;(3)反应2NaCl+2CuSO4+SO2+2H2O=2CuCl↓+2H2SO4+Na2SO4中,氯化钠中钠元素的化合价是+1,氯元素的化合价都是1,硫酸铜中铜元素的化合价是+2,硫元素的化合价是+6,氧元素的化合价是2,二氧化硫中硫元素化合价是+4,氧元素化合价是2,水中氢元素化合价是+1,氧元素化合价是2,氯化亚铜中铜元素的化合价是+1,氯元素化合价是1,硫酸中氢元素化合价是+1,硫元素的化合价是+6,氧元素的化合价是2,硫酸钠中钠元素化合价是+1,硫元素的化合价是+6,氧元素的化合价是2,因此反应中化合价升高的元素是硫元素,由+4变成+6;(4)本工艺中可循环利用的物质是NaOH、H2SO4,电解生成的氢氧化钠可应用于反应Ⅰ,反应VI中生成的硫酸可应用于反应Ⅴ; (5)70℃真空干燥的目的是加快乙醇和水的蒸发,防止CuCl被空气氧化。
2NaOH+Cl2↑+H2↑;(3)反应2NaCl+2CuSO4+SO2+2H2O=2CuCl↓+2H2SO4+Na2SO4中,氯化钠中钠元素的化合价是+1,氯元素的化合价都是1,硫酸铜中铜元素的化合价是+2,硫元素的化合价是+6,氧元素的化合价是2,二氧化硫中硫元素化合价是+4,氧元素化合价是2,水中氢元素化合价是+1,氧元素化合价是2,氯化亚铜中铜元素的化合价是+1,氯元素化合价是1,硫酸中氢元素化合价是+1,硫元素的化合价是+6,氧元素的化合价是2,硫酸钠中钠元素化合价是+1,硫元素的化合价是+6,氧元素的化合价是2,因此反应中化合价升高的元素是硫元素,由+4变成+6;(4)本工艺中可循环利用的物质是NaOH、H2SO4,电解生成的氢氧化钠可应用于反应Ⅰ,反应VI中生成的硫酸可应用于反应Ⅴ; (5)70℃真空干燥的目的是加快乙醇和水的蒸发,防止CuCl被空气氧化。


科目:初中化学 来源: 题型:
【题目】某种矿石由氧化镁、氧化铁、氧化铜和二氧化硅组成,用它制备氢氧化镁的流程示意图如图所示(已知:二氧化硅不溶于水也不与稀盐酸反应)。
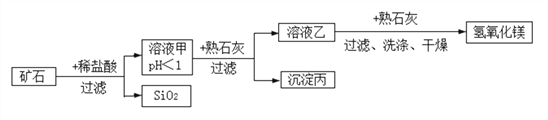
在溶液甲中加入熟石灰调节溶液的pH,可以使溶液中的金属阳离子逐步转化为沉淀。该实验条件下,使金属阳离子沉淀的相关pH数据见下表。为保证产品纯度、减少产品损失,并便于操作,所得溶液乙的pH的取值有一定的范围。
氢氧化物 | Fe(OH)3 | Cu(OH)2 | Mg(OH)2 |
开始沉淀的pH | 1.5 | 4.2 | 8.6 |
完全沉淀的pH | 3.2 | 6.7 | 11.1 |
下列说法错误的是
A. 溶液甲中共含有三种阳离子
B. 溶液乙的pH的范围是6.7<pH<8.6
C. 沉淀丙的成分是Fe(OH)3、Cu(OH)2、Mg(OH)2
D. 溶液乙中加入熟石灰发生的化学反应方程式:MgCl2+Ca(OH)2= Mg(OH)2↓+CaCl2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是某反应的微观示意图,下列有关说法正确的是( )

A. 反应前后分子的种类不变
B. 反应中生成的物质都是化合物
C. 该反应的基本类型属于复分解反应
D. 反应前后有三种元素的化合价均发生了变化
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】去年党的十九大会议使用了一种含碳酸钙的“石头纸”。为测定其中碳酸钙的含量,课外活动小组的同学共称取50g碎纸样品,分别放在5只烧杯中并编号,再分别向5只烧杯中加入浓度相同的稀盐酸进行实验。实验数据见下表(假设纸张中的其他成分既不溶于水,也不与盐酸反应):
烧杯① | 烧杯② | 烧杯③ | 烧杯④ | 烧杯⑤ | |
加入样品的质量/g | 10 | 10 | 10 | 10 | 10 |
加入稀盐酸的质量/g | 10 | 20 | 30 | 40 | 50 |
充分反应后生成气体的质量/g | 0.88 | 1.76 | 2.64 | m | 3.52 |
(1)表中m的值为___________。
(2)求样品中碳酸钙的质量分数___________。
(3)求样品中碳酸钙和盐酸刚好完全反应后得到溶液溶质的质量分数(结果保留到小数点后第二位)___
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】溶液在生活中应用非常广泛,因而了解溶液的有关知识非常必要。
(1)下图甲为X、Y、Z三种固体物质的溶解度曲线,根据曲线可知30oC时X的溶解度为_______g。小明同学欲在40oC时配制100g 25%的Y物质的溶液,他_______(填“能”或“不能”)达到目的。
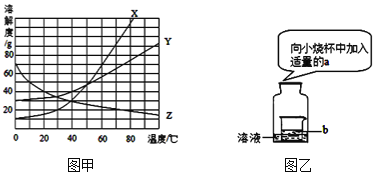
(2)小丽用图乙所示装置进行实验。
①若广口瓶内盛有70 g X物质的不饱和溶液, b是水,a是下列________(填字母)物质,有望变成饱和溶液。
A.浓硫酸 B.硝酸铵 C.氢氧化钠 D.氧化钙
②若广口瓶内盛有10gZ物质的饱和溶液,a、b分别是镁条和稀硫酸,观察到的现象是(Z与其他物质不反应)______________________________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图为A、B、C三种物质的溶解度曲线,下列说法正确的是
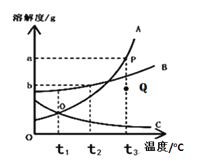
A. 在t1℃时饱和且质量相等的A、B、C三种溶液升温至t3℃时,所得溶液质量由大到小的顺序是A ![]() B
B ![]() C
C
B. 物质C的不饱和溶液可通过降温的方式变成饱和溶液
C. Q点可表示t3℃时A物质的饱和溶液
D. 将t3℃时饱和的A、B、C三种溶液降温至t1℃时,所得溶液溶质质量分数由大到小的顺序是 B![]() A
A ![]() C
C
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲、乙、丙三种物质的溶解度曲线,下列分析错误的是
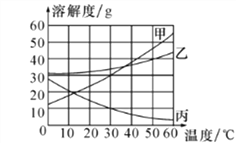
A. 30℃时,把10g丙溶解在50g水中,得到丙的饱和溶液
B. 50℃时,把甲、乙、丙三种溶液降温至10℃,析出晶体的质量由大到小的顺序为:甲>丙>乙
C. 将甲的饱和溶液变为不饱和溶液,可采用升高温度的方法
D. 30℃时,甲的饱和溶液的溶质质量分数约为23.1%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】能源利用和环境保护是人类共同关注的问题。
(1)石油是一种粘稠状液体,主要含有_____________两种元素
(2)页岩气是指蕴藏于页岩系统中的天然气,页岩气主要成分完全燃烧的化学方程式为___________。
(3)某电厂为防止环境污染,用石灰石粉浆来吸收煤燃烧时排放出的二氧化硫,其反应的化学方程式为:2CaCO3+2SO2+O2==2CaSO4+2X,则X的化学式为_________。
(4)以天然气为燃料的燃气灶,当其火焰呈现黄色或橙色,锅底出现黑色,这时就需要调节灶具的进风口,目的是_______________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】酸和碱是初中阶段两类非常重要的化合物。
(1)酸和碱之间能发生中和反应,该反应的实质是________________。
(2)实验考试时,需要用1%的氢氧化钠溶液100g,有关操作如图1所示:
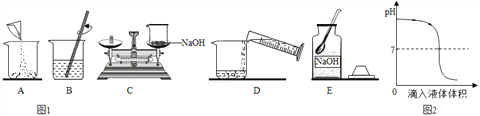
以上实验正确的操作顺序是_____(用字母代号表示);C操作中有明显的错误,正确的操作应该是______;量取一定体积的水时,需要选用的合适的仪器是_____。
(3)用pH试纸测定所配制的溶液的酸碱度,写出具体的操作方法。
(实验拓展)如图2是氢氧化钠溶液和盐酸用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线。滴加顺序有两种,a是将氢氧化钠溶液滴入盐酸中,b是将盐酸滴入氢氧化钠溶液中。
根据曲线判断,该反应的滴加顺序是_______(填“a“或“b“)。某同学在滴加过程中,意外发现了有气泡产生,请解释原因_____(写一个即可)。
(实验反思)某已变质的氢氧化钠溶液100g,向其中加入溶质质量分数为7.3%的稀盐酸100g,恰好完全反应得到中性溶液。则蒸干该中性溶液可得到固体的质量是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com