
【题目】小明家的“苏打粉”标示的主要成分为碳酸钠和氯化钠。为了测定其中碳酸钠的质量分数,小明取一定量的苏打粉样品于烧杯中并加入质量分数为12%的稀盐酸,当气泡完全放出后,称得反应后烧杯内溶液的质量如图所示。计算:
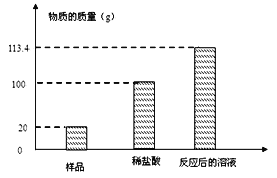
(1)生成的二氧化碳的质量为 .
(2)苏打粉中碳酸钠的质量分数为多少?
科目:初中化学 来源: 题型:
【题目】超细碳酸钙可用于生产钙片、牙膏等产品。利用碳化法生产超细碳酸钙的主要流程示意如下:
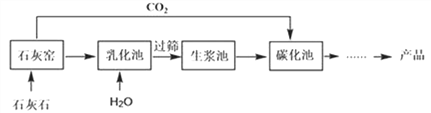
(1)石灰石的主要成分的化学式为__________。
(2)乳化池中,生石灰与水发生反应,其化学方程式为________________。
(3)过筛的目的是拦截_______(填“大于”或“小于”)筛孔直径的颗粒。
(4)碳化池中反应的化学方程式为__________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】1875年,法国化学家布瓦博德朗发现了一种新元素镓(其元素符号为Ga),它能与沸水剧烈反应生成氢气和氢氧化镓;镓的原子结构示意图如图所示。请回答下列问题:
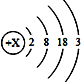
(1)镓元素原子的质子数为_______________;
(2)该元素在元素周期表中与铝元素在同一个_____________(填“横行”或“纵行”),其化学性质与铝元素相似,原因是_____________________________________;
(3)氢氧化镓与氢氧化钠都具有碱的性质,则氢氧化镓与稀硫酸反应的化学方程式为________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】粗盐中含有少量不溶性杂质(泥沙),还含有少量可溶性杂质(Na2SO4、CaCl2、MgCl2)。现以粗盐为原料制取精盐,生产过程如下图所示:
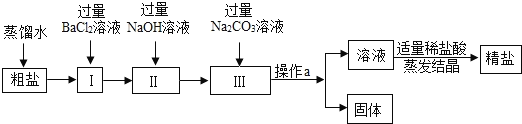
(1)操作a的名称是__________,该操作需要用到的玻璃仪器主要有:烧杯、_________、玻璃棒;
(2)写出I中发生反应的化学方程式_____________________;
(3)加入过量Na2CO3的作用是_________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是A、B、C三种物质的溶解度曲线,下列说法错误的是
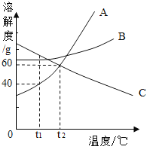
A.t1℃时,A、B、C三种物质的溶解度由大到小的顺序是C>B>A
B.当A中含有少量B时,可以通过冷却热饱和溶液的方法提纯A
C.升高温度可使接近饱和的C溶液变为饱和
D.将t2℃时A、B、C的饱和溶液同时降温至t1℃后,所得溶液中溶质的质量分数由大到小的顺序是C>B>A
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线。
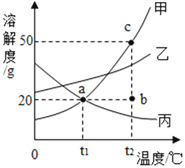
(1)t1℃时,甲、乙、丙三种物质的溶解度大小关系:_____。
(2)t1℃时,完全溶解5g丙物质至少需要水_____g。
(3)t2℃时,将20g甲加入到100g水中,充分搅拌后所得溶液是甲的_____溶液(填“饱和”或“不饱和”),可以用图中_____点(填“a”“b”或“c”)表示。
(4)将甲、丙的饱和溶液从t2℃降温到t1℃,对所得溶液的叙述不正确的是________。
A.都是饱和溶液 B.溶剂质量:甲<丙
C.析出固体质量:甲>丙 D.溶质质量分数:甲=丙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请根据下列实验装置回答问题:
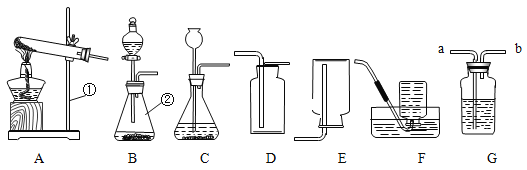
(1)写出仪器①②的名称:①__________________;②_____________________。
(2)用高锰酸钾制取氧气的化学方程式为________________________________;当用F装置收集满O2并取出集气瓶后,停止该实验的正确操作方法是________________。
(3)可用E装置收集的气体是________________(需答两种)。
(4)硫化氢(H2S)是有毒气体,实验室常用块状硫化亚铁(FeS)和稀硫酸在常温下反应制取硫化氢(H2S)气体,应选用的发生装置最好是_________________。
(5)检査C装置气密性的方法是:先用弹簧夹夹住导气管上的胶皮管,再向长颈漏斗中 加入水_______________________,静置,若观察到________________,说明气密性良好。
(6)G装置可用于气体的收集、检验、除杂和体积的测量等,用该装置不能完成的实验是______________(填序号)。
A.气体从a端通入,收集氢气。
B.瓶内装有澄清石灰水,气体从a端通入,检验氧气中中是否混有二氧化碳。
C.在b端连接量筒,瓶内装满水,氧气从a端通入,测量气体的体积。
D.瓶内装有氢氧化钠溶液,气体从a端通入,吸收一氧化碳中混有的二氧化碳。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】汽车轮胎是汽车的重要部件。市场上存在个别轮胎原料掺假问题:以返炼胶代替原片胶,严重影响轮胎的质量,给采用该轮胎的汽车带来了安全隐患。如图是汽车轮胎示意图,请回答下列问题:
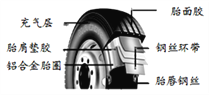
(1)在汽车轮胎组成中属于金属材料的是_______________;属于合成材料的是_____________。
(2)专家认为轮胎中充入稀有气体可较少胎体受热膨胀,减少爆胎机率,请写出一种稀有气体的化学式____________。
(3)轮胎的胎圈一般都用铝合金制成,用铝合金制作胎圈的优点是:______;铝合金属于________(填“纯净物”或“混合物”),请写出一种比较铁和铝活动性强弱的方法__________(用化学方程式表示)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碱式氯化镁【Mg(OH)Cl】受热能分解,它分解后产物是什么?小科进行了探究。
【猜想】Mg(OH)Cl分解后产物可能有:Mg、MgCl2、MgO、HCl气体、H2O、Cl2。
老师告诉他产物就是上述猪想中的其中几种,并提示Cl2是一种黄绿色有刺激性气味的气体。
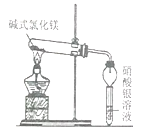
【实验一】取少量的Mg(OH)Cl放入大试管中,按如图所示装置进行实验。加热过程中观察到足量硝酸银溶液中有白色沉淀产生,一段时间后,沉淀不再产生,大试管口也没有液滴形成,管内有固体剩余,无其他现象。由此推知Mg(OH)Cl分解后产物中有_______气体,无其他气体。
【实验二】取少量实验一的剩刹余固体于试管中,加入足量稀盐酸,没有气泡产生。由此推知Mg(OH)Cl分解后产物中没有_______。
【实验三】再取少量实验一的剩余固体,加入足量稀硝酸,固体全部溶解,再滴入AgNO3溶液,无沉淀产生。由此推知Mg(OH)Cl分解后产物中没有________。
【结论】Mg(OH)Cl受热分解的化学反应方程式为____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com