
����Ŀ��ͼ1ΪNaCl��KNO3���ܽ�����ߡ�
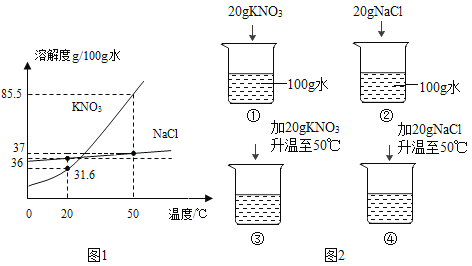
��1��20��ʱ��KNO3���ܽ����_______��
��2��50��ʱ����50gKNO3������뵽50gˮ�еõ�����KNO3��_______������͡������͡�����Һ����ʱ��Һ����������������_______��������0.1%��
��3����ȥNaCl��Һ�л���������KNO3���ᴿNaCl�ķ�����_______��
��4��20��ʱ��ijͬѧ������ͼ2ʵ�飬�õ���Ӧ��Һ��~�ܣ�˵����ȷ����______��
A�٢�����Һ�����������������
B�ۢ�����Һ�����������������
C���ۢܽ�����20�棬���о���������m(KNO3)��m(NaCl)
D���ۢܽ�����20�棬���ʵ������ۣ���
���𰸡�31.6g/100gˮ ���� 46.1% �����ᾧ AC
��������
��1�����ܽ������ͼ��֪20��ʱ��KNO3���ܽ����31.6g/100gˮ�����31.6g/100gˮ��
��2��50��ʱ��KNO3���ܽ����85.5g/100gˮ����50��ʱ100gˮ��������ܽ�85.5gKNO3����50gˮ��������ܽ�42.75g������50g����غ����γɱ�����Һ�����ʵ���������=![]() ��100%��46.1%��������ͣ�46.1%��
��100%��46.1%��������ͣ�46.1%��
��3������ص��ܽ�����¶�Ӱ��ϴ��Ȼ��Ƶ��ܽ�����¶�Ӱ���С���������������ᾧ�������з���õ�NaCl����������ᾧ��
��4��A����ͼ�п�֪20��ʱ�٢��м����20g���ʶ���ȫ�ܽ��ˣ��������ձ��е��ܼ�����100g�������������������ȣ���A��ȷ��
B��50��ʱNaCl���ܽ����37g/100gˮ�����Լ����40gNaCl��û��ȫ���ܽ⣬50��ʱKNO3���ܽ����85.5g/100gˮ�����Լ����40g KNO3ȫ���ܽ⣬�������ձ��е��ܼ�������ͬ�����Ԣۢ�����Һ������������������ȣ���B����
C��������20��ʱ���Ȼ��Ƶ��ܽ����36g/100gˮ������ص��ܽ����31.6g/100gˮ���ʢܻ�����4g���ۻ�����8.4g����m(KNO3)��m(NaCl)����C��ȷ��
D�����ۢܽ�����20��ʱ�����е�����������Ϊ36g�����е�����������Ϊ31.6g�������ʵ������ۣ��ܣ���D����
��ѡAC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ô����������������ԭ���ȵ�����ͭ���ⶨˮ����ɡ�ʵ��װ����A��B��C��D��ɣ���������װ��ʡ��δ���������ش��������⣺
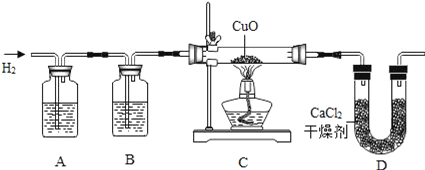
��1�����ijѧ����п�ͽ�Ũ��������ȡ����������װ��A��B��Ϊ�˵õ��������������������װ��A��ͨ����_____��Һ����������_____����װ��B��ͨ����_____��Һ����������_____��
��2����ʵ��ǰ����������£�װ����ͭ�IJ����ܵ���������6.4�ˣ�װ�Ȼ��Ƶ�U�ܵ�����������7.2�ˡ���������ʵ�����ݣ�д��ˮ���⡢������Ԫ�ص�����_____��
��3����װ��D�У���CaCl2�Ļ�Ϊ��ˮ����ͭ������Ϊ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A-F�����Ծ��꼶��ѧ���ʴ��ͥ�ij�Ա������A����Է�������Ϊ80�ĺ�ɫ�����B��Dͬ�����Σ�C��E��Ϊ�����ҷֱ���Aӵ�й�ͬ��Ԫ�ء�F�����������������ͬ�����죬����������Լ������������������ͼ��ʾ��ֻ�л����ܷ�����Ӧ�����ʷ��ܽӵ��Է�����ͬ���ڲ����������ش�

��1��A�Ļ�ѧʽΪ_ �� E������______��
��2�����α��������ǵĴ���˳��ΪA��F��______��E��
��3��A�����Fʱ�������Ļ�ѧ��Ӧ����ʽΪ______����Ӧ����Һ��___ɫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A~H�dz��л�ѧ���������ʣ�����AΪʯ��ʯ����Ҫ�ɷ֣�EΪ��ɫ���壬HΪ��ɫ��������Щ���ʵ��ת����ϵ��ͼ��ʾ�����в���������ͷ�Ӧ������ʡ�ԡ��ش��������⣺

��1��д���������ʵĻ�ѧʽ��A_____��E_____��H_____.
��2����ѧ��Ӧ�����������仯������B��ˮ��Ӧʱ��_____�������ա��ų�����������
��3��A��B+C�Ļ�ѧ��Ӧ����ʽΪ_____
��4��G+F��H�Ļ�ѧ��Ӧ����ʽΪ_____
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
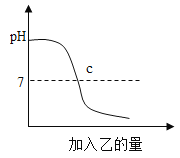
����Ŀ����������������κ�ˮ�ķ�Ӧ�����кͷ�Ӧ����֪�ס��ҷֱ���������Һ������������Һ�е�һ�֣���ͼ��ʾ����м�����ʱ��ҺpH�ı仯���ߣ���д���������ͼ������ȡ����Ϣ��
��1������_____��
��2������_____��
��3��_____��
��4��_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȡһ��ֽ�����ȼ�����10����ɫʯ����Һ��װ�벣�����У�Ȼ��Ӳ����ܵ�����ͬʱ����ֱ�պ��Ũ��ˮ��Ũ�����������Ѹ��������˹ܿڣ��ܿ�ɹ۲쵽�����а��̲�������������ʧ�����۲쵽����ͼ��ʾ������
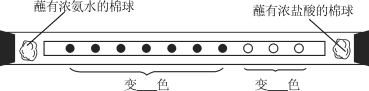
������˵������ȷ����
A����ˮ�����ᶼ�����ӷ�������
B���ù�����û�л�ѧ��Ӧ����
C������������ӵ��˶���������ͬ
D��ͼʾ�ڵ��ʾʯ����Һ��������ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ij��ɽ���Է�ˮ(��Ҫ�����ᡢ������������ͭ������п��)Ϊԭ����ͨ���������̿ɽ���ˮ�е�����ͭ��п�ֲ�������ʵ�ֻ������á�
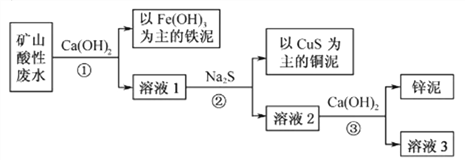
(1)�������������Ca(OH)2���������á�
һ���кͷ�ˮ�е��������÷�Ӧ�Ļ�ѧ����ʽΪ___________________________��
���ǽ�������ת��ΪFe(OH)3���÷�Ӧ����______________________(�������Ӧ����)��
(2)���������п��������Ҫ�ĺ�п������Ļ�ѧʽΪ___________________��
(3)Ϊ�ֲ���������ͭ��п�Ƚ�����Դ��ֱ�ӵõ�ͭ������ֻ��ı����������е�ij���������Լ����ɡ��ò����Ӧ������Լ��ֱ���____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ�ס��ҡ����������ʵ�ת����ϵ��

��1�����ס��ҡ���������������ˮ�����ᣮ
��д�������ҵĻ�ѧ����ʽ��__��
��������ʱ���������һ�ַ�Ӧ����һ������__Ԫ�أ�
��2����֪�������Եļ����ȷֽ�Ϊ�����������ˮ�������Ǻ�ɫ�Ľ���������ҵ���Һ����ɫ��
�ټ�����ʱ������Ҫ���Լ�������_____��
��д���������Ļ�ѧ����ʽ��_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ǻ�ѧ�г�����һ��ҩƷ������dz�ư�ɫ������ĩ���ڿ���������ˮ�ֺͶ�����̼��������ˮ����ˮ���ܷ�����Ӧ�����������ƺ������⣬����ʽ��Na2O2+2H2O=2NaOH+H2O2�������������ֽܷ�ų�������
��1������ˮ���������ʵ�鷽���ǣ�___________________________�������ķ�Ӧ����ʽ�ǣ�__________________________��
��2��ijͬѧΪ��֤���������Ƽ���ˮ���������������ƣ������ɵ���Һ�еμ��˼�����ɫ��̪��Һ���۲쵽����������Һ�ȱ�����Ϊ��ɫ������Դ��������̽����
������⣺ʲô������Һ�ȱ������ɫ��
��������裺
����1����ͬѧ����������ɫ��̪��Һ���ʵ�����Һ��ɫ����
����2����ͬѧ�����������ɵĹ�������ʹ��Һ��ɫ����
ʵ������ۣ�
a����ͬѧ����IJ��룬���������ͬѧ�ķ��ԣ���Ϊ______________________________��
b��Ϊ����֤�Լ��IJ��룬��ͬѧ��������·�����ʵ����֤��
ʵ�鲽�� | ʵ������ | ʵ����� |
ȡ����ϡ����������Һ���Թ��У��μ�1��2�η�̪��Һ������___________�۲����� | ��Һ��ȻΪ��ɫ | ____________________ |
���۽������㻹�������ͬ�IJ����������������µĺ����ļ���ͷ����㽫��ý�����4�֣�
����3��_____________
����3��
ʵ�鲽�� | ʵ������ | ʵ����� |
_________________ | _______________ | ______________ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com