
【题目】如图所示实验中,①、④为用紫色石蕊溶液润湿的棉球,②、③为用石蕊溶液染成紫色的干燥棉球。下列说法正确的是
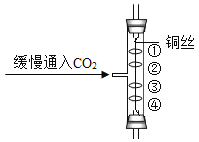
A.①、②、③、④都变红
B.③不变红、④变红,说明CO2密度较大
C.实验中的CO2可通过块状大理石和稀硫酸制取
D.①、④变红,②、③不变红,说明CO2与水反应生成酸
【答案】D
【解析】
二氧化碳能和水反应生成碳酸,碳酸显酸性,能使石蕊试液变红色。
A、将二氧化碳缓慢通入竖直放置的玻璃管中,①④为用紫色石蕊溶液润湿的棉球,②③为用石蕊溶液染成紫色的干燥棉球,二氧化碳不能使石蕊变色,二氧化碳和水发生了化学反应生成碳酸,碳酸显酸性,能使石蕊试液变红色,②③都不变色,①④都变红,故A不正确;
B、③为用石蕊溶液染成紫色的干燥棉球,④为用紫色石蕊溶液润湿的棉球,③不变红、④变红,说明CO2和水发生了化学反应生成碳酸,碳酸显酸性,能使石蕊试液变红色,故B不正确;
C、块状大理石和稀硫酸反应生成硫酸钙,硫酸钙的微溶物,覆盖在大理石表面,阻止反应的进行,则实验中的CO2不能通过块状大理石和稀硫酸制取,故C不正确;
D、①④为用紫色石蕊溶液润湿的棉球,②③为用石蕊溶液染成紫色的干燥棉球,①、④变红,②、③不变红,说明CO2与水反应生成酸,故D正确。故选D。


科目:初中化学 来源: 题型:
【题目】我市南部山区拥有丰富的石灰石矿产资源。有某一矿山上的石灰石样品,其中只含二氧化硅杂质(二氧化硅是一种既不溶于水也不与盐酸反应且耐高温的固体)。明水街道某学校的同学们想测定该样品中碳酸钙的质量分数,他们选取了一块石灰石样品,将其敲打粉碎后,称出16 g放入烧杯内(烧杯质量为10 g)。然后加入50 g某一定溶质质量分数的稀盐酸,用玻璃棒搅拌至不再产生气泡为止,剩余总质量为71.6g。请完成下列问题:
(1)将石灰石样品敲打粉碎的主要目的是:_____;
(2)实验结束时,理论上共放出二氧化碳的质量为多少_____;
(3)计算该石灰石样品中碳酸钙的质量分数。_____(保留小数点后一位小数)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】青岛有漫长的海岸线,蕴藏着丰富的海洋资源。

(一)粗盐提纯。
除去难溶性杂质后的食盐水中还含有Ca2+、Mg2+、SO42-等杂质离子,为得到较纯的氯化钠,进行如下的实验操作:
①加入过量的Na2CO3溶液;②加入过量的BaCl2溶液;③加入过量的NaOH溶液;④加入适量的盐酸调节溶液的pH等于7;⑤过滤;⑥蒸发。
(1)下列操作顺序正确的有______(填字母序号)。
A ②①③⑤④⑥ B ①②③⑤④⑥ C ③②①④⑤⑥ D ③②①⑤④⑥ E ②③①⑤④⑥
(2)其中操作①加入过量的Na2CO3溶液的作用为____。
(3)操作④加入适量的盐酸调节溶液的pH等于7的目的是____。
(4)操作⑤过滤后,所得的滤渣成分为____。
(二)海水资源综合利用的部分途径如上图。
(1)氨碱工业生产过程中,在加压并按先后顺序向饱和NaCl溶液中通入氨气、二氧化碳的条件下,使碳酸氢钠结晶析出,该反应的化学方程式是____。
(2)写出步骤Ⅰ电解饱和NaCl溶液的化学方程式是_____。
(3)海水制镁。实际生产中,步骤Ⅲ常选用______作为沉淀剂,从海水中提取MgCl2历经步骤Ⅱ、Ⅲ、Ⅳ三步转换的主要目的是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用适合的化学用语填空:
①2个氢原子______。
②能供给呼吸的气体______。
③食盐的主要成分______。
④氢氧根离子______。
⑤氧化钙中钙元素化合价为+2价______。
⑥地壳中最多的金属元素:______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下图所示实验,回答问题。
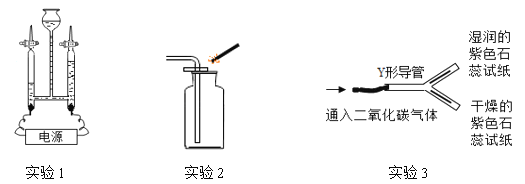
(1)实验1中,左侧玻璃管中产生气体的构成微粒是_____(填名称),电解水时发生反应的化学符号表达式为_____;
(2)实验2中盛放氧气的集气瓶正放,原因是_____,可用带火星的木条验满,利用了氧气的_____性;
(3)图中Y形导管平放于桌面,可观察到的现象是_____,用化学符号表达式解释结论:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请结合下图回答问题
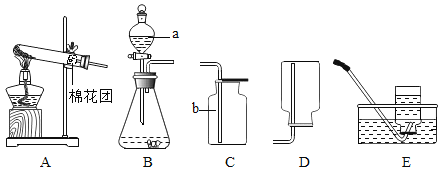
(1)写出图中有标号仪器的名称:a _______,b____________。
(2)用高锰酸钾制取一瓶氧气,可选用装置A和__________(选填序号)组合。装入药品前要先__________,棉花团的作用是____________,该反应的符号表达式____________。
(3)用双氧水和二氧化锰制氧气,二氧化锰的作用是_______,该反应的符号表达式_______。
(4)用如图装置制取CO2并验证相关性质。
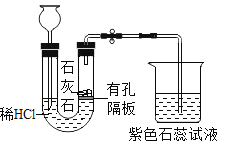
①生成CO2反应的符号表达式____________。
②相对于B装置,选择该发生装置的优点是__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用符号表示以下意义:
(1)2个镁原子________;
(2)氢氧根离子________;
(3)氯化亚铁________;
(4)正五价的氮元素形成的氧化物________;
(5)构成液氧的微粒________;
(6)金属铜中铜元素的化合价________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是实验室制备和收集氧气常用的几种装置,请回答下列问题。
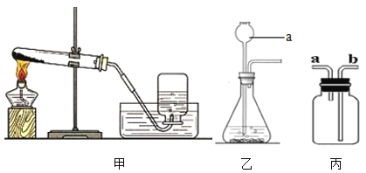
(1)若使用高锰酸钾制氧气,应选装置_____,指出装置的错误之处_____。此实验操作步骤有:①停止加热;②固定试管;③将导管从水槽中取出;④装药品;⑤加热;⑥收集氧气;⑦检查装置的气密性。请写出正确的操作顺序_____。
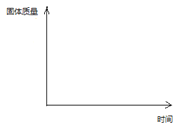
(2)若使用乙装置制氧气,a仪器名称为_____,锥形瓶内固体的化学式为_____,请在下图画出反应过程中,此固体的质量随时间的变化曲线_____。
(3)甲装置和乙装置都可以制氧气,两者相比计较,你认为装置_____操作更简便,请再写出所选装置的一处优点:_____。
(4)小冰同学用装置乙和装置丙收集了一瓶O2,装置连接正确
①乙中导管与_____相连(填“a”或“b”)
②用装置丙收集氢气,气流由_____进入(填“a”或“b)。
③装置丙充满水也可收集氧气,气流由_____进入(填“a”或“b)。
查看答案和解析>>
科目:初中化学 来源: 题型:
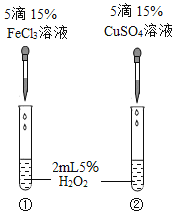
【题目】为比较Fe3+和Cu2+对过氧化氢分解反应的催化效果,某同学设计了如图所示的实验(FeCl3溶液、CuSO4溶液中都含有阴阳离子和水分子),有关实验有如下说法:
①过氧化氢中氧元素的化合价为-1价;
②若图1所示实验中反应速率为①>②,则一定说明Fe3+比Cu2+对H2O2分解催化效果好;
③实验中可通过观察产生气泡快慢来比较反应速率;
④滴加FeCl3或CuSO4溶液后过氧化氢分解速率加快,则FeCl3或CuSO4是过氧化氢催化剂
以上说法不正确的是( )
A.①②B.①④C.②④D.③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com