
【题目】如图为化学小组探究金属的化学性质所做的四个实验,回答下列问题:
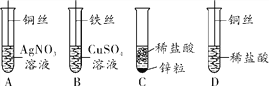
(1)写出溶液变蓝的反应的化学方程式______________________________。
(2)由上述实验能得出金属的活动性顺序是__________。
【答案】 Cu+2AgNO3=== Cu(NO3)2+2Ag Fe>Cu>Ag(或Zn>Cu>Ag)
【解析】A、铜比银活泼,铜可以把银从硝酸银溶液中置换出来,硝酸铜溶液呈蓝色,银是银白色;B、铁比铜活泼,铁可以把铜从硫酸铜溶液中置换出来,铜是红色;C、锌与稀硫酸发生置换反应,生成气体和硫酸锌,硫酸锌溶液无色;D、铜不能与稀盐酸反应。(1) 溶液变蓝的反应的化学方程式是Cu+2AgNO3=Cu(NO3)2+2Ag。(2)由上述实验能得出金属的活动性顺序是Fe>Cu>Ag(或Zn>Cu>Ag)。
点睛∶能与酸发生反应的金属比不与酸发生反应的金属活动性强,在金属活动顺序表中排在前面金属能把排在他后面的金属从其可溶性化合物溶液中置换出来。


 优百分课时互动系列答案
优百分课时互动系列答案 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案科目:初中化学 来源: 题型:
【题目】金属材料在国防建设中起着重要的作用。

①工业生产中常用稀盐酸除去铁制品表面的铁锈,该反应的化学方程式为___________________;
②小明为探究锌、铁、铜三种金属的活动性顺序,设计了如图2所示的两个实验:
Ⅰ.实验1中,小明以“金属表面产生气泡的快慢”为标准来判断锌、铁的活动性强弱,有同学认为不合理,理由是____________________________;
Ⅱ.通过实验2,可证明铁的活动性比铜强,反应的化学方程式是_____________________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学用语是学习化学的重要工具。
⑴写出下列微粒的化学符号
①硅原子___ ②2个氨分子____③氧化铝中铝元素的化合价___ ④硫酸根离子____
⑵现有H、O、C、Na四种元素,请选用其中的元素写出下列物质的化学式:
①用于人工降雨或灭火______; ②制肥皂的碱_______;
③最清洁的燃料_______; ④治疗胃酸过多的盐______。
(3)用化学方程式表示下列事实:
①常温下,铝具有很好的抗腐蚀性能,是因为铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜,反应的化学方程式是_______________;
②“冰洲石”(主要成分为CaCO3)制成的工艺品不能与盐酸接触,用化学方程式表示其原因:____;
③氯化铵与氢氧化钙混合加热____________________________ ;
④实验室用锌粒和稀硫酸反应制氢气________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有一包白色固体样品,可能由硫酸钠、氢氧化钠、碳酸钙、氯化钡、氯化镁中的一种或几种物质组成,为探究该样品的组成,某小组取适量样品按下列流程进行实验。下列说法正确的是

A. 滤渣a的成分一定是碳酸钙和硫酸钡
B. 滤液中溶质有氢氧化钠和氯化钡
C. 白色沉淀b的成分是碳酸钡和氢氧化镁
D. 样品中一定含有硫酸钠、氢氧化钠、碳酸钙、氯化钡,可能含有氯化镁
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图为KNO3的溶解度曲线,a、b在溶解度曲线上。

(1)a点对应的溶液是_____溶液。(填“饱和”或者“不饱和”)
(2)a点对应的溶液的质量分数是_________。(只列计算式)
(3)将a点对应的溶液升温到70 ℃,其质量分数_____。(填写“变大”、“变小”或“不变”)
(4)欲使KNO3溶液的状态从b点转化为c点,可采取的措施是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如下图所示,A-I是初中化学中常见的物质,A、C是两种常见液体且组成元素相同,B、F是黑色粉末,H是蓝色沉淀,E是含钠元素的化合物,部分反应物和生成物已略,“→”表示物质转化。
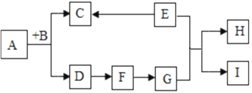
(1)物质F的化学式为_______;
(2)写出E物质在生活中的一种用途_______;
(3)写出反应E+G→H+I的化学方程式_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下图回答问题
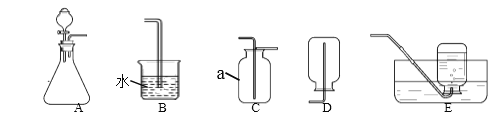
① 仪器a 的名称是______。
② 将A 装置和__装置连接(填编号)可组成实验室制取氧气装置,写出反应的 化学方程式是________________ 。
③ 锥形瓶中充满二氧化碳,分液漏斗中装有氢氧化钠溶液,将装置A 和B 连接,打开活塞滴入氢氧化钠溶液,关闭活塞后,看到的现象是_____。该现象不足以证明 二氧化碳与氢氧化钠发生了反应,理由是_________。(用化学方程式表示)
④ 为了实验更严谨,用图一装置进行对比实验,证明二氧化碳与氢氧化钠溶液确实发生了反应,由压强传感器采集的数据如图二,其中表示二氧化碳与氢氧化钠溶液反应的曲线 是__。(填“a”或“b”)
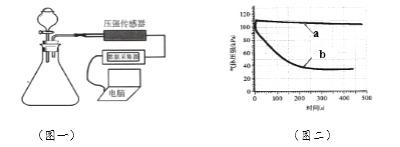
利用压强传感器证明CO2与NaOH溶液反应利用压强传感器证明CO2与NaOH溶液反应实验结果
⑤上述实验中4.4 克二氧化碳与40 克氢氧化钠溶液恰好完全反应。
I. 二氧化碳物质的量为______mol。
II. 氢氧化钠溶液的溶质质量分数(根据化学方程式计算)______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人类的生产生活离不开金属材料,请用学过的知识回答下列问题
(1)“湿法炼铜”的原理是硫酸铜溶液与铁反应,其反应的化学方程式为_____。图1铜制品的用途中,利用金属导电性的是_____(填字母)。
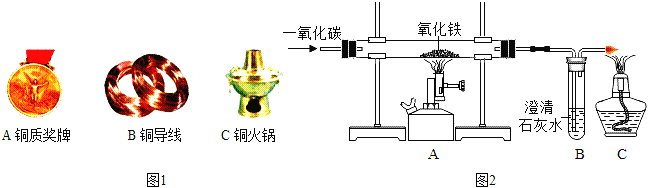
(2)工业上炼铁的原理是利用一氧化碳和氧化铁反应。某兴趣小组利用图2装置进行试验,请按要求填空:
①写出CO还原Fe2O3的化学方程式_____;实验过程中能观察到A装置中的现象为_____,右边导气管口放置点燃的酒精灯的目的是_____
②铁制品在一定条件下能生锈,疏松的铁锈不能阻碍里层的铁继续与_____反应生锈,因此铁制品可以进一步锈蚀。回收利用废旧金属制品的目的之一是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】鸡蛋主要由蛋壳、蛋壳膜、蛋白、蛋黄等几个部分组成,其中蛋壳的主要成分是CaCO3,里面覆盖一层蛋壳膜。化学活动兴趣小组的同学开展了以下探究活动:
【提出问题】蛋壳中的CaCO3含量是多少?

【查阅资料】
a、蛋壳经过科学检测其中含CaCO3的质量分数约为82%~85%,含蛋白质质量分数约14-17%。
b、蛋壳膜中蛋白质含量约为90%~93%。
c、Ba(OH)2是一种碱,化学性质与Ca(OH)2相似。
【设计方案】
方案一:用“灼烧法”,将该蛋壳放在空气中充分灼烧并采集相关数据进行测定。
方案二:用“酸处理法”,将蛋壳与稀盐酸反应后再进行吸收转变为碳酸钡进行测量处理。
【进行实验】
方案一:称取12.0 g蛋壳研磨成粉末置于通风橱中,灼烧至质量不再减少,再称量剩余固体的质量为7.16 g。
方案二:用下图所示的连接实验装置,称取12 g蛋壳样品进行实验(假设其他成分均不与HCl反应,装置内试剂均足量。)
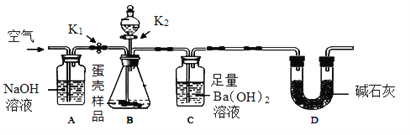
【实验步骤】
① 按上图连接好装置后,并检查装置的气密性;
② 向B装置中加入蛋壳样品后,先通入一会儿空气;
③ 关闭K1,打开K2,向蛋壳样品中滴入10%的盐酸,直到__________为止;
④ 关闭K2,打开K1,再缓缓通入空气一会儿,至装置C中不再产生沉淀为止;
⑤ 将装置C中的固液混合物进行过滤、__________、烘干后称量其质量;
⑥ 重复上述实验。
【数据处理】
方案一:产生的CO2质量__________g,蛋壳中的CaCO3的质量分数为__________%。(保留一位小数)
方案二:重复3次实验,记录数据如下:
实验次数 | 第1次 | 第2次 | 第3次 |
装置C中沉淀质量(/g) | 19.68 | 19.75 | 19.67 |
方案二:实验测得蛋壳中的CaCO3的质量分数__________(写出计算过程,)
(已知:Mr(CaCO3):100 Mr(BaCO3):197)
【评价反思】
(1)方案二中装置D的作用是__________。
(2)方案一测定值与科学检测的数据有较大误差,主要原因是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com