
过碳酸钠(2Na2CO3·3H2O2)广泛用于洗涤、纺织、医疗、造纸等。某兴趣小组展开了深入的学习:
【资料卡片】:
Ⅰ、制备研究:下图是制备过碳酸钠的工艺流程。
 |
请回答问题:
(1)反应器中发生反应的化学方程式为 ▲ ;
(2)生产中,反应及干燥均需在较低温度下进行,原因是 ▲ ;
(3)生产过程中,需加入较多的NaCl,以便过碳酸钠晶体析出,这是因为 ▲ 。
(4)操作A的名称是 ▲ ,若在实验室完成此操作,需要的玻璃仪器是烧杯、 ▲
和 ▲ ;
(5)洗涤过碳酸钠晶体最好选用 ▲ 。
A.蒸馏水 B.无水酒精 C.饱和碳酸钠溶液 D.饱和NaCl溶液
(6)母液可以循环使用,其中主要含有的溶质是 ▲ 和 ▲ ;
Ⅱ、纯度测定:测定过碳酸钠样品(杂质不溶于水)中2Na2CO3·3H2O2的质量分数。
小组同学设计了如下图所示实验装置(部分仪器略去),并进行实验。
 【实验步骤】:① ▲ ;②将过碳酸钠样品(2.20g)和少许黑色粉末均匀混合后置于装置A中,在量筒中加满水;③连接仪器,打开分液漏斗活塞,缓缓滴入水;④待装置A中 ▲ 时,停止滴加水,并关闭活塞;⑤待量筒中水面不再变化时,记录其中水面刻度;⑥根据数据进行计算。
【实验步骤】:① ▲ ;②将过碳酸钠样品(2.20g)和少许黑色粉末均匀混合后置于装置A中,在量筒中加满水;③连接仪器,打开分液漏斗活塞,缓缓滴入水;④待装置A中 ▲ 时,停止滴加水,并关闭活塞;⑤待量筒中水面不再变化时,记录其中水面刻度;⑥根据数据进行计算。
【实验分析及数据处理】:
(7)完善实验步骤的相关内容:① ▲ 、④ ▲ ;
(8)实验中,水的作用是 ▲ ;黑色粉末能加快过碳酸钠的分解速率,其自身质量和化学性质在反应前后均不变,可能是 ▲ (填化学式);
(9)实验中, ▲ ,则开始收集气体;(2分)
A.刚开始出现气泡时 B.当气泡均匀连续出现时
C.若用带火星木条放在导管口部,复燃时
(10)若量筒中收集到气体的体积是224mL(通常情况下,氧气的密度近似为1.43g·L—1。),计算过碳酸钠样品中2Na2CO3·3H2O2的质量分数[3分,Mr(2Na2CO3·3H2O2)=314、Mr(O2)=32] ▲ ;
【实验反思】:
(11)经过讨论,小组同学一致认为测定结果偏大,可能原因是 ▲ ;
(12)量筒中长导管的作用是 ▲ ;
(13)有同学提出,装置中原有空气会使测定结果偏大。这种说法是否正确,如不正确,请说明理由。 ▲ ;
(14)经过讨论,小组同学一致认为可用下述方案进行测定。方案:将装置A中剩余物过滤,洗涤滤渣,并将洗涤液并入滤液蒸发得无水固体1.39g。则样品中2Na2CO3·3H2O2的质量分数为 ▲ 。
(15)根据资料卡片,你还能设计出什么方案测定样品中2Na2CO3·3H2O2的质量分数? ▲ 。(只需给出简要的方案)
(1)2Na2CO3 + 3H2O2 == 2Na2CO3·3H2O2 (2)防止过碳酸钠分解,影响产量和产率
(3)过碳酸钠在NaCl溶液中溶解度较小,易析出晶体
(4)过滤 玻璃棒 漏斗 (5)B (6)NaCl Na2CO3(或H2O2)
(7)检查气密性 不再产生气体时 (8)溶解过碳酸钠,利于其分解 MnO2(或CuO)
(9)A(2分)
(10)过碳酸钠分解产生氧气质量为224mL ×10—3×1.43g·L—1 = 0.32g ……………… 1分
2(2Na2CO3·3H2O2) ~ 3O2↑
314×2 32×3
X 0.32g
解得X=2.09g ……………………………………………………………… 1分
则样品中,2Na2CO3·3H2O2的质量分数为: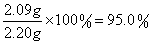 (或95.2%)… 1分
(或95.2%)… 1分
(11)滴入的水占据了锥形瓶内的体积,使得O2体积偏大
(12)起缓冲作用,防止温度降低至室温时,测量结果产生偏差(或防倒吸)
(13)不正确,装置中原有空气和生成的O2等体积代换 (注:理由叙述不正确不给分)
(14)93.6%(或93.5%)
(15)想方法测出过碳酸钠和酸反应生成CO2的体积或质量,进而进行计算(或过碳酸钠和氯化钙、氯化钡等溶液生成沉淀质量进行测定)(其他合理答案也可得分)


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
 生活中用到各种漂白剂.化学课上,老师带来一种常用作漂白剂的物质,可能是双氧水(H2O2)、过碳酸钠(2Na2CO3?3H2O2)和过氧化钙(CaO2)中的一种.同学们观察发现,该漂白剂为白色粉末(右图).
生活中用到各种漂白剂.化学课上,老师带来一种常用作漂白剂的物质,可能是双氧水(H2O2)、过碳酸钠(2Na2CO3?3H2O2)和过氧化钙(CaO2)中的一种.同学们观察发现,该漂白剂为白色粉末(右图).| 实验步骤 | 实验操作 | 实验现象 | 结论 |
| 步骤1 | 取2g白色固体放入试管中,加入5mL水,充分振荡. | 液体浑浊,有持续的细小气泡冒出. | |
| 步骤2 | 向步骤1的试管中继续滴加无色酚酞. | 无色酚酞变红. | |
| 步骤3 | 继续滴加 |
该漂白剂的成分不是过碳酸钠. |
查看答案和解析>>
科目:初中化学 来源: 题型:
 生活中用到各种漂白剂.化学课上,老师带来一种常用作氧系漂白剂的物质,可能是双氧水(H2O2)、过碳酸钠(2Na2CO3?3H2O2)和过氧化钙(CaO2)中的一种.同学们观察发现,该漂白剂为白色粉末(右图).
生活中用到各种漂白剂.化学课上,老师带来一种常用作氧系漂白剂的物质,可能是双氧水(H2O2)、过碳酸钠(2Na2CO3?3H2O2)和过氧化钙(CaO2)中的一种.同学们观察发现,该漂白剂为白色粉末(右图).| 实验步骤 | 实验操作 | 实验现象 | 结论 |
| 步骤1 | 取2g白色固体放入试管中,加入20mL水,充分振荡. | 液体浑浊, 有持续的细小气泡冒出. |
|
| 步骤2 | 静置,取步骤1的试管上层清液少许,滴加无色酚酞. | 无色酚酞变红. | |
| 步骤3 | 该消毒剂的成分不是过碳酸钠. |
查看答案和解析>>
科目:初中化学 来源: 题型:
 生活中用到各种漂白剂.化学课上,老师带来一种常用漂白剂的物质,可能是双氧水(H2O2)、过碳酸钠(2Na2CO3?3H2O2)和过氧化钙(CaO2)中的一种.同学们观察发现,该漂白剂为白色粉末(如图).
生活中用到各种漂白剂.化学课上,老师带来一种常用漂白剂的物质,可能是双氧水(H2O2)、过碳酸钠(2Na2CO3?3H2O2)和过氧化钙(CaO2)中的一种.同学们观察发现,该漂白剂为白色粉末(如图).| 实验步骤 | 实验操作 | 实验现象 | 结论 |
| 步骤1 | 取2g白色固体放入试管中,加入5ml水,充分振荡. | 液体浑浊, 有持续的细小气泡冒出. |
|
| 步骤2 | 向步骤1的试管中继续滴加无色酚酞. | 无色酚酞变红. | |
| 步骤3 | 该消毒剂的成分不是过碳酸钠. |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 1、过碳酸钠具有碳酸钠和过氧化氢的双重性质,不稳定,受热、遇水易分解; 2、过碳酸钠分解的化学方程式为2(2 Na2CO3?3 H2O2 )=4 Na2CO3+6 H2O+3O2↑ 3、H2O2分解放出热量,Na2CO3受热不分解;Ⅰ、制备研究:如图1是制备过碳酸钠的工艺流程.  请回答问题: (1)反应器中发生反应的化学方程式为 2Na2CO3+3H2O2═2Na2CO3?3H2O2 2Na2CO3+3H2O2═2Na2CO3?3H2O2 ;(2)生产中,反应及干燥均需在较低温度下进行,原因是 防止过碳酸钠分解,影响产量和产率 防止过碳酸钠分解,影响产量和产率 ;(3)生产过程中,需加入较多的NaCl,以便过碳酸钠晶体析出,这是因为 过碳酸钠在NaCl溶液中溶解度较小,易析出晶体 过碳酸钠在NaCl溶液中溶解度较小,易析出晶体 .(4)操作A的名称是 过滤 过滤 ,若在实验室完成此操作,需要的玻璃仪器是烧杯、玻璃棒 玻璃棒 和漏斗 漏斗 ;(5)洗涤过碳酸钠晶体最好选用 B B .A.蒸馏水 B.无水酒精 C.饱和碳酸钠溶液 D.饱和NaCl溶液 (6)母液可以循环使用,其中主要含有的溶质是 NaCl NaCl 和Na2CO3(或H2O2) Na2CO3(或H2O2) ;Ⅱ、纯度测定:测定过碳酸钠样品(杂质不溶于水)中2Na2CO3?3H2O2的质量分数. 小组同学设计了如图2所示实验装置(部分仪器略去),并进行实验. [实验步骤]:① 检查气密性 检查气密性 ;②将过碳酸钠样品(2.20g)和少许黑色粉末均匀混合后置于装置A中,在量筒中加满水;③连接仪器,打开分液漏斗活塞,缓缓滴入水;④待装置A中不再产生气体 不再产生气体 时,停止滴加水,并关闭活塞;⑤待量筒中水面不再变化时,记录其中水面刻度;⑥根据数据进行计算.[实验分析及数据处理]: (7)完善实验步骤的相关内容:① 检查气密性 检查气密性 、④不再产生气体 不再产生气体 ;(8)实验中,水的作用是 溶解过碳酸钠,利于其分解 溶解过碳酸钠,利于其分解 ;黑色粉末能加快过碳酸钠的分解速率,其自身质量和化学性质在反应前后均不变,可能是MnO2(或CuO) MnO2(或CuO) (填化学式);(9)实验中, A A ,则开始收集气体;A.刚开始出现气泡时 B.当气泡均匀连续出现时 C.若用带火星木条放在导管口部,复燃时 (10)若量筒中收集到气体的体积是224mL(通常情况下,氧气的密度近似为1.43g?L-1.),计算过碳酸钠样品中2Na2CO3?3H2O2的质量分数[Mr(2Na2CO3?3H2O2)=314、Mr(O2)=32] 95% 95% ;[实验反思]: (11)经过讨论,小组同学一致认为测定结果偏大,可能原因是 滴入的水占据了锥形瓶内的体积,使得O2体积偏大 滴入的水占据了锥形瓶内的体积,使得O2体积偏大 ;(12)量筒中长导管的作用是 起缓冲作用,防止温度降低至室温时,测量结果产生偏差(或防倒吸) 起缓冲作用,防止温度降低至室温时,测量结果产生偏差(或防倒吸) ;(13)有同学提出,装置中原有空气会使测定结果偏大.这种说法是否正确,如不正确,请说明理由. 不正确,装置中原有空气和生成的O2等体积代换 不正确,装置中原有空气和生成的O2等体积代换 ;(14)经过讨论,小组同学一致认为可用下述方案进行测定.方案:将装置A中剩余物过滤,洗涤滤渣,并将洗涤液并入滤液蒸发得无水固体1.39g.则样品中2Na2CO3?3H2O2的质量分数为 93.6% 93.6% .(15)根据资料卡片,你还能设计出什么方案测定样品中2Na2CO3?3H2O2的质量分数? 想方法测出过碳酸钠和酸反应生成CO2的体积或质量,进而进行计算(或过碳酸钠和氯化钙、氯化钡等溶液生成沉淀质量进行测定 想方法测出过碳酸钠和酸反应生成CO2的体积或质量,进而进行计算(或过碳酸钠和氯化钙、氯化钡等溶液生成沉淀质量进行测定 .(只需给出简要的方案)
查看答案和解析>> 科目:初中化学 来源: 题型:阅读理解 过碳酸钠(2Na2CO3?3H2O2)广泛用于洗涤、纺织、医疗、造纸等.某兴趣小组展开了深入的学习: 【资料卡片】:
|