
【题目】化学是一门以实验为基础的科学,请结合图表信息回答问题:
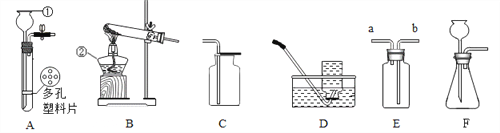
Ⅰ.写出图中①②仪器的名称:①__________________,②__________________。
Ⅱ.实验室用氯酸钾和二氧化锰的固体混合物制取氧气,反应的化学方程式为_____________,加热时试管口应略向下倾斜的原因是_______________。
Ⅲ.①为研究实验室制取二氧化碳的适宜条件(温度、浓度、固体的颗粒大小等因素会影响化学反应的快慢),进行了如下四组实验:
实验编号 药品 | 甲 | 乙 | 丙 | 丁 |
m g大理石 | 块状 | 块状 | 粉末状 | 粉末状 |
n g盐酸(过量) | 稀盐酸 | 浓盐酸 | 稀盐酸 | 浓盐酸 |
大理石与盐酸反应的化学方程式是__________________________;实验甲与_________ 对照(填编号),是为了研究固体反应物颗粒大小对反应快慢的影响;上述实验中,另一个影响反应快慢的因素是________________________。
实验室制取二氧化碳气体,可随时控制反应发生或停止的装置为_______(填序号),若
用E装置收集该气体,气体应从 _____(填“a”或“b”)端通入。若在收集得到二氧化碳的集气瓶中滴加紫色石蕊试液,稍作震荡,试液颜色变为______色,变色的原因是____________。
Ⅳ.甲烷是一种无色气体,密度比空气小,难溶于水的气体。实验室用无水醋酸钠(固体)与碱石灰(固体)混合加热制得,则可选择的发生装置为___________(填序号),选择装置D收集甲烷气体的理由是__________。
【答案】长颈漏斗酒精灯2KClO3 ![]() 2KCl+3O2↑防止冷凝水倒流使试管破裂CaCO3+2HCl→ CaCl2+H2O+CO2↑丙浓度Ab红CO2+H2O →H2CO3 碳酸使紫色石蕊试液变红B甲烷难溶于水
2KCl+3O2↑防止冷凝水倒流使试管破裂CaCO3+2HCl→ CaCl2+H2O+CO2↑丙浓度Ab红CO2+H2O →H2CO3 碳酸使紫色石蕊试液变红B甲烷难溶于水
【解析】(3)选择发生装置需考虑是因素是,反应物的状态和反应条件。加热固体制取气体,发生装置为B,固体和液体常温下反应制取气体应选用的发生装置为A。选择收集装置需考虑气体的密度,是否与空气的成分反应,气体在水中的溶解性。氧气的密度比空气的大,可以用向上排空气法收集,氧气难溶于水可以用排水法收集。验室用氯酸钾和二氧化锰的固体混合物制取氧气,反应的化学方程式为2KClO3 ![]() 2KCl+3O2↑,加热时试管口应略向下倾斜的原因是防止水倒流,使试管炸裂;丙对照,是为了研究固体反应物颗粒大小对反应快慢的影响,因两个方案中只有固体的颗粒大小不同;上述实验中,另一个影响反应快慢的因素是 浓度 (8). 实验室制取二氧化碳气体,可随时控制反应发生或停止的装置为A ,关闭弹簧夹,大试管内气体增多,压强变大,在压力的作用下,试管内液面下降,当液面下降到隔板下边时,固体反应物与液体分离,反应停止;反之,打开弹簧夹,反应开始。(9). 若用E装置收集该气体,二氧化碳的密度比空气的大,气体应从b端通入。(10)若在收集得到二氧化碳的集气瓶中滴加紫色石蕊试液,稍作震荡,试液颜色变为红色,反应方程式为 CO2+H2O →H2CO3 ,碳酸使紫色石蕊试液变红 (12) 用无水醋酸钠(固体)与碱石灰(固体)混合加热制得,则可选择的发生装置为B,选择装置D收集甲烷气体的理由是 甲烷难溶于水。
2KCl+3O2↑,加热时试管口应略向下倾斜的原因是防止水倒流,使试管炸裂;丙对照,是为了研究固体反应物颗粒大小对反应快慢的影响,因两个方案中只有固体的颗粒大小不同;上述实验中,另一个影响反应快慢的因素是 浓度 (8). 实验室制取二氧化碳气体,可随时控制反应发生或停止的装置为A ,关闭弹簧夹,大试管内气体增多,压强变大,在压力的作用下,试管内液面下降,当液面下降到隔板下边时,固体反应物与液体分离,反应停止;反之,打开弹簧夹,反应开始。(9). 若用E装置收集该气体,二氧化碳的密度比空气的大,气体应从b端通入。(10)若在收集得到二氧化碳的集气瓶中滴加紫色石蕊试液,稍作震荡,试液颜色变为红色,反应方程式为 CO2+H2O →H2CO3 ,碳酸使紫色石蕊试液变红 (12) 用无水醋酸钠(固体)与碱石灰(固体)混合加热制得,则可选择的发生装置为B,选择装置D收集甲烷气体的理由是 甲烷难溶于水。


科目:初中化学 来源: 题型:
【题目】完成下列变化的化学方程式,并按要求填空。
(1)红磷在空气中燃烧:____________ ;反应中____________(填“放热”或“吸热”)。
(2)实验室用高锰酸钾制取氧气:____________;试管口应放置____________。
(3)一氧化碳与三氧化二铁在高温条件下反应:____________;用____________检验气体产物。
(4)铁丝插入盛有硫酸铜溶液的试管中:__________;反应后溶液质量__________(填“增大”“减小”或“不变”)。
(5)熔融的金属钠与液氨(NH3)在加热条件下反应生成氨基钠(NaNH2)和氢气:_____________;反应类型为:_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是生命之源,保护水资源,防止水污染是每个公民和全社会的责任。下列做法有利于防止水资源污染的是
①农业生产中要合理使用农药和化肥
②工业废水和生活污水处理达标后再排放
③不用含磷洗衣粉
④将海水淡化
A.①②④ B.②③④ C.①②③ D.①②③④
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是人类宝贵的自然资源。对水的研究如下:
Ⅰ.电解水的实验装置如图所示,请回答:
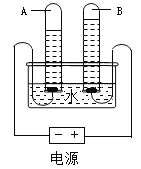
通电后,电极上出现气泡,一段时间后A试管和B试管中所收集的气体体积比约为______;实验室检验气体B的方法是______。
该实验可得出水是由__________________组成的结论;
写出电解水的化学方程式__________________________。
Ⅱ. 原水(未经过处理的水)中含有泥沙、悬浮物和细菌等杂质。在水中撒些明矾,可除去水中的泥沙、悬浮物,使水变澄清;通入适量氯气可生成盐酸和次氯酸,次氯酸(HClO)可杀死水中的细菌。某水厂生产自来水的步骤如下:
![]()
可以除去水中的泥沙和悬浮物杂质的步骤为_________________(填编号)。
② 能消毒杀菌的步骤为___________________(填编号)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】新型材料纳米铁粉具有广泛的用途,它比普通铁粉更易与氧气反应,工业上可以利用H2和FeCl2在高温反应器中制备,同时得到HCl。下列有关说法错误的是
A. 制备纳米级铁粉的反应属于置换反应
B. 纳米级铁粉与氧气反应,生成物是Fe3O4
C. 纳米级铁粉比普通铁粉更易与氧气反应是因为物质种类不同
D. 反应前需向反应器中通入氮气,目的是排除装置中的空气
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】目前使用的燃料大多来自化石燃料。
(1)化石燃料包括天然气、煤、______。
(2)天然气的主要成分是甲烷,甲烷燃烧的化学方程式为______。
(3)为解决化石燃料日益枯竭的问题,需要开发和使用新能源,如______(填一种即可)。
(4)越来越多的人选择拼车出行,拼车出行的好处有______(填序号)。
A. 降低出行成本 B. 减少汽车尾气排放
C. 减少使用汽油,节约能源 D. 降低交通压力,缓解拥堵
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】日常使用的干电池是一种锌锰电池,它的构造是:负极为锌做的圆筒,正极是一根碳棒,它的周围被二氧化锰,碳粉和氯化铵的混合剂所包围,总称为"碳包"。碳包和锌筒之间填充着氯化铵、氯化锌的水溶液和淀粉等组成的糊状物。废旧干电池随意丢弃会造成环境污染。学校兴趣小组同学准备对废旧的干电池进行探究。
(一)拆解干电池,得到铜帽、锌皮、碳棒、黑色粉末等物质。
(二)回收二氧化锰并测定碳粉与二氧化锰的质量比:
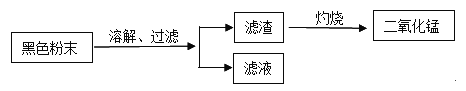
(1)干电池使用时将化学能转化成___________能。
(2)上述操作中灼烧的目的是___________;
(3)同学们将过滤后得到的滤渣干燥后称得质量为25克,充分灼烧后冷却称得剩余固体质量为20克,则滤渣中二氧化锰与碳粉的质量比为___________。经分析,此结果偏大,老师指出同学们在实验中缺少一步操作,该操作是___________。
(4)为验证二氧化锰,同学们用A、B两支洁净试管,分别取5毫升3%的过氧化氢溶液,往A试管中加入少量上述实验灼烧后得到的固体,如果出现___________的现象,说明为二氧化锰。反应的化学方程式为___________。
(三)用拆解得到的锌皮(含杂质)制取硫酸锌晶体。
实验步骤:①将剪碎后的锌皮放入烧杯中,加入足量的稀硫酸,充分反应;②将上述反应后的混合物过滤。③将滤液加热浓缩、_____、过滤,得到ZnSO4·7H2O晶体。
(5)步骤①中反应方程式为___________,将锌皮剪碎的目的是__________。
(6)步骤②需要的仪器有铁架台、烧杯、___________和玻璃棒,玻璃棒的作用是___________。
(7)步骤③缺少的操作是____________。
(四)测定锌皮中锌的质量分数。同学们设计了如下实验装置,取1克锌皮放于试管中,实验中将注射器内50毫升稀硫酸(足量)完全注入试管中。当试管中不再产生气泡时立刻读数得到量筒中水的体积为350毫升。已知实验条件下氢气的密度为0.09g/L。
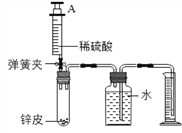
(8)计算该锌皮中锌的质量分数___________。(写出计算过程,结果保留两位小数)
(9)上述方法测得的锌的质量分数偏大,不可能的原因是____________
A.没等装置冷却就读数
B.锌皮中含有少量铁
C.试管中有气体没有排出
D. 将注射器中稀硫酸全部注入试管中后忘掉夹紧弹簧夹
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com