

 口算题天天练系列答案
口算题天天练系列答案科目:初中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 | 实验结论 |
| 抽取适量气体,注入 澄清石灰水中 | 有白色沉淀产生 | 玻璃罩内含有二氧化碳 |
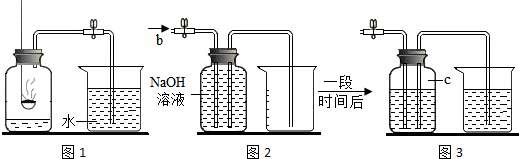
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 实验目的 | 实验方案 |
| A | 稀释浓硫酸 | 将浓硫酸沿器壁慢慢注入水里,并不断搅拌 |
| B | 鉴别氮气和氧气 | 将带火星的木条伸入集气瓶中,若 复燃是氧气 |
| C | 检测烧碱溶液、澄清石灰水的酸 碱度 | 滴到红色石蕊试纸上,观察颜色变化 |
| D | 除去NaCl固体中少量Na2CO3杂质 | 加足量稀盐酸后,蒸发结晶 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Na2SO4BaCl2 K2CO3 HCl | B. | NaClNa2CO3 KNO3 HCl | ||
| C. | FeCl3 NaOH KCl Ba(NO3)2 | D. | BaCl2 K2SO4 Na2SO4 NaCl |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
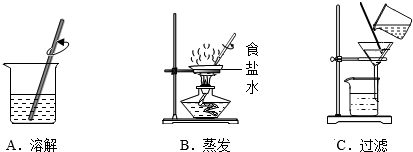
| 选项 | 实验目的 | 方案 |
| A | 鉴别稀盐酸和稀硫酸 | 取样,滴加紫色石蕊,观察现象 |
| B | 除去粗盐中的难溶性杂质 | 将粗盐研碎、溶解、过滤、蒸发 |
| C | 除去CaO中的CaCO3 | 高温加热到固体质量不变 |
| D | 探究Mg、Ag、Cu金属的 活动性顺序 | 将两根光亮的镁条分别伸入 硫酸铜溶液和硝酸银溶液中 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
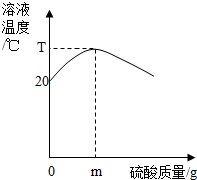 20℃时,在密闭(与外界不发生热交换)容器中,将400g 10%的氢氧化钠溶液和稀硫酸混合,反应过程中溶液温度与硫酸质量关系如图所示.下列说法不正确的是( )
20℃时,在密闭(与外界不发生热交换)容器中,将400g 10%的氢氧化钠溶液和稀硫酸混合,反应过程中溶液温度与硫酸质量关系如图所示.下列说法不正确的是( )| A. | 该反应是放热反应 | |
| B. | 恰好中和时溶液温度达到最高点 | |
| C. | 恰好中和时消耗硫酸的质量是m g | |
| D. | 若用浓硫酸代替稀硫酸,则恰好反应时溶液温度为T℃ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用火碱溶液吸收二氧化硫SO2+2NaOH═Na2SO3+H2O | |
| B. | 植物的光合作用C6H12O6+6O2 $→_{光照}^{叶绿素}$6CO2+6H2O | |
| C. | 碳酸饮料中碳酸的形成原理CO2+H2O═H2CO3 | |
| D. | 利用一氧化碳的还原性得到金属铁2Fe2O3+3CO═4Fe+3CO2↑ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
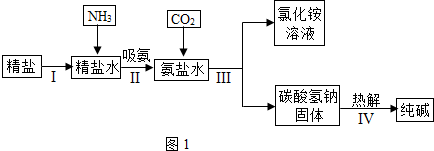
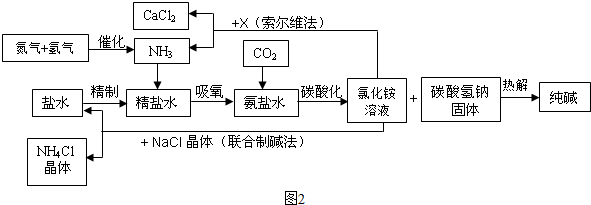
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com