
| A. | 21.2g | B. | 10.6g | C. | 12.6g | D. | 5.3g |
分析 根据样品中碳元素的质量分数即计算出碳元素的质量,进而计算出碳酸氢钠的质量,结合碳酸氢钠受热分解的方程式即可计算出碳酸钠的质量.
解答 解:碳元素的质量:20g×12%=2.4g;
碳酸氢钠的质量:2.4g÷$\frac{12}{23+1+12+16×3}×100%$=16.8g
设反应后生成的碳酸钠的质量为x,
2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑
168 106
16.8g x
$\frac{168}{16.8g}=\frac{106}{x}$
x=10.6g
答案:B.
点评 此题是对化学方程式计算的考查,解题的关键是找到已知量,此题则是利用碳的质量求出其它物质的质量.


 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案科目:初中化学 来源: 题型:选择题
| A. | 氢气+氧气$\stackrel{点燃}{→}$水 | |
| B. | 铁+硫酸铜→铜+硫酸亚铁 | |
| C. | 碱式碳酸铜$\stackrel{加热}{→}$ 氧化铜+二氧化碳+水 | |
| D. | 蔗糖水→蔗糖+水 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 缉毒犬能根据气味发现毒品,是由于分子在不断运动 | |
| B. | 変瘪的乒乓球放入热水中能鼓起来,是由于分子间隔变大 | |
| C. | 水降温会结冰,是因为结冰时水分子静止不动 | |
| D. | 将石块研磨成粉状,说明分子变小了 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
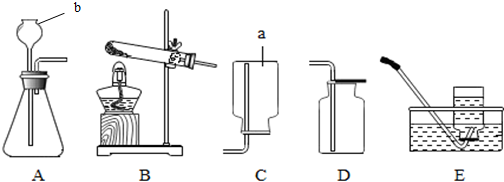
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
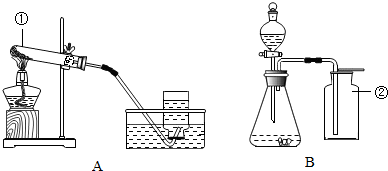
| 实验步骤 | 实验现象 |
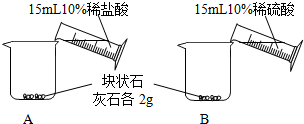 | A中不断产生气泡,固体逐渐减少,有少量固体剩余. B中开始有少量气泡产生,反应很快停止. |
| 实验步骤 | 实验现象 |
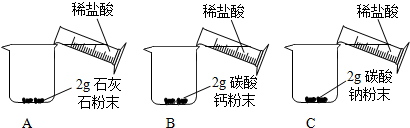 | A中迅速产生大量气泡,固体很快减少,有少量固体剩余. B、C中都迅速产生大量气泡,固体很快消失. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com