
【题目】硫酸钠是制造纸浆、燃料稀释剂、医药品等的重要原料.某硫酸钠粗品中含有少量CaCl2和MgCl2杂质,实验室进行提纯的流程如图1:
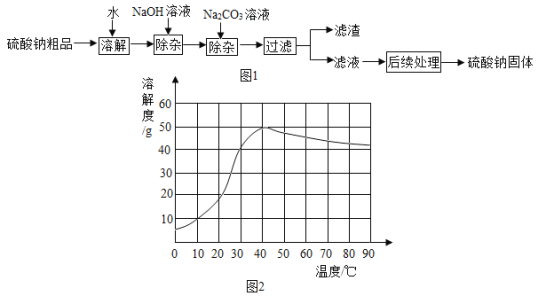
回答下列问题:
(1)用NaOH除杂时,反应的化学方程式为________,除杂、过滤后得到的滤渣成分的化学式是________.
(2)NaOH和Na2CO3如果添加过量了,最好加入适量________溶液除去.
(3)“后续处理”的主要操作是蒸发,为了获得较纯净的硫酸钠,应蒸发至_______(填序号).
A.完全蒸干时停止加热
B.快干时停止加热,利用余热蒸干
C.有大量固体析出时停止加热,过滤弃去剩余的少量溶液
(4)已知硫酸钠的溶解度随温度变化的曲线如图2所示.40℃时,100g蒸馏水中约溶解________g硫酸钠达到饱和.将该饱和溶液升高温度至90℃,观察到的现象是________.
【答案】2NaOH+MgCl2═2NaCl+Mg(OH)2↓;Mg(OH)2、CaCO3稀硫酸B50;析出固体
【解析】
(1)用NaOH除杂时,氢氧化钠和氯化镁反应生成氢氧化镁沉淀和氯化钠,反应的化学方程式为:2NaOH+MgCl2═2NaCl+Mg(OH)2↓;除杂、过滤后得到的滤渣成分的化学式是Mg(OH)2、CaCO3;
(2)氢氧化钠和稀硫酸反应生成硫酸钠和水,碳酸钠和稀硫酸反应生成硫酸钠、水和二氧化碳,因此NaOH和Na2CO3如果添加过量了,最好加入适量稀硫酸溶液除去;
(3)“后续处理”的主要操作是蒸发,为了获得较纯净的硫酸钠,应蒸发至快干时停止加热,利用余热蒸干;
(4)由硫酸钠的溶解度随温度变化的曲线可知,40℃时硫酸钠溶解度是50g,100g蒸馏水中约溶解50g硫酸钠达到饱和;将该饱和溶液升高温度至90℃时硫酸钠溶解度减小,观察到的现象是析出固体。


科目:初中化学 来源: 题型:
【题目】下图是证实植物进行光合作用的实验装置, 取一个大烧杯,装入大半杯水,烧杯内放入一些金鱼藻,并通入一定量的气体A。静置一段时问后,用漏斗罩住金鱼藻,然后将装满水的试管倒置于漏斗上,在阳光下放置一段时间,试管内有许多气泡产生,管内液面下降。根据这一实验,回答下列问题:

(1)通入气体A的目的是 ;
(2)试管内的气体可用 来检验;
(3)植物的光合作用的一种产物是葡萄糖,已知葡萄糖的化学式为C6H12O6,试计算出它的相对分子质量(写出计算过程,可能用到的相对原子质量:C-12、H-1、O-16,)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】MgSO4·7H2O是一种重要的化工原料,某工厂以一种镁矿石(主要成分为SiO2和MgCO3,还含有少量FeCO3)为原料制备MgSO4·7H2O的主要流程如下:
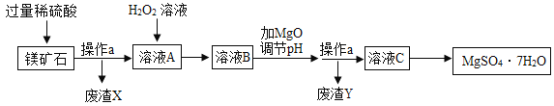
已知:SiO2既不溶于水也不溶于稀硫酸。请回答下列问题:
(1)“操作a”的名称是______。
(2)“废渣Y”中含有少量的FeOOH,其中铁元素的化合价是______。
(3)MgCO3溶于稀硫酸的化学方程式为______。
(4)“溶液A”中加入H2O2溶液会生成Fe2(SO4)3,该反应的化学方程式为______。
(5)选用MgO调节pH使Fe3+转化为沉淀,而不选用NaOH的原因是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某研究小组为探究“影响铁制品锈蚀快慢的因素”,取同浓度的稀氨水和稀醋酸,用右图装置完成表中实验,回答下列问题。
![]()
实验序号 | ① | ② | ③ | ④ |
实验温度/℃ | 25 | 25 | 70 | 70 |
试剂 | 稀氨水 | 稀醋酸 | 稀氨水 | 稀醋酸 |
出现铁锈 所需时间 | 1天 未见锈蚀 | 5分钟 | 1天 未见锈蚀 | 1分钟 |
(1)铁锈的主要成分是________(填化学式)。
(2)实验②和④可探究________因素对铁制品锈蚀快慢的影响;欲探究试剂酸碱性对铁制品锈蚀快慢的影响,应选择的实验是______________(填实验序号)。
(3)根据表中实验现象得出的结论是_________________(写出1点即可)。
(4)影响铁制品的锈蚀快慢除上述因素外,还有______________________(写出1点即可),请设计实验方案_________________________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】溶解是生活中常见的现象,不同物质在水中的溶解能力不同.
①下表是KNO3、NaCI在不同温度下的溶解度(单位:g/100g水).
温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 |
KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
NaCI | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
Ⅰ.上表中的两种物质在40℃时,________的溶解度较大;请用相应的数据列式表示该温度时KNO3饱和溶液的质量分数________ (不要求计算).
Ⅱ.请写出一种将KNO3的不饱和溶液转化为饱和溶液的方法________ .
Ⅲ.20℃时,将20g NaCl放入50g水中,所得溶液的质量是________ g.
Ⅳ.从NaCl溶液中得到NaCl晶体的方法是________ .
②用硫酸铜进行如图所示的实验,完成下列填空(用编号表示).
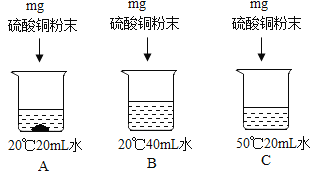
所得三个溶液中:一定属于饱和溶液的是________ ,溶液中溶剂质量的大小关系是________ .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】生活中处处有化学,化学与生活密切相关.
(1)某饼干包装袋中用干燥剂的是生石灰,请用化学方程式表示其原理________.
(2)森林火灾时,常砍伐处一条隔离带的目的是________.
(3)我们常用洗涤剂洗涤餐具上的油污,这是因为洗涤剂具有________功能,用汽油洗油污属________现象,
(4)雾霾是一种灾害性天气现象,由于人类生产、生活向大气中排放大量细颗粒物,如果超过大气的自净能力,就会出现雾霾现象.请分析下列污染物中,会导致雾霾的是(填序号)________。
A.二氧化碳 B.臭氧 C.一氧化碳 D.PM2.5
(5)厨房中的下列物品锁使用的主要材料属于金属材料的________。
A.不锈钢炊具 B.橡胶手套 C.纯棉围裙
(6)天然气作燃料________(用化学方程式表示).
(7)根据如图所提供的信息,写出在催化式排气净化器中发生的一个反应(用化学方程式表示)________.

(8)当汽车受撞击后,汽车安全气囊中的NH4NO3固体瞬间分散成N2O 和一种常温下的无色液体,反应方程式是________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某不纯的氯化钠样品中只含有一种杂质,取该样品11.7克,溶于适量水中,然后加入足量的硝酸银溶液,得到29.7克白色沉淀,则所含杂质不可能是( )
A. 氯化镁 B. 氯化钙 C. 氯化铝 D. 氯化钾
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属材料在人类社会中的使用历史悠久、领域广泛.
(1)通常情况下,不是固体的金属是________,合金中的所有成份________(填“是”或“不是”或“不一定”)都是金属.
(2)在金属活动性顺序中,________和________(填金属名称或符号)的活动性比Cu强、比Fe弱.
(3)等质量的两种金属(化学式分别为“X”和“Y”),分别与足量盐酸反应(除了金属种类不同,其它所有条件均相同;两种金属在化合物中均显+2价),生成的H2体积与反应时间的关系如图所示.
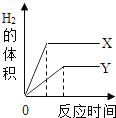
①这两种金属的活动性强弱顺序为X________Y(填“>”或“<”下同);
②这两种金属的相对原子质量大小关系为X________Y.
③将X金属条放入硫酸铜溶液中,X上可观察到的现象是________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】学校科学活动月,小明绘制了一幅简笔画-自然界中碳的循环。根据图示回答下列问题:
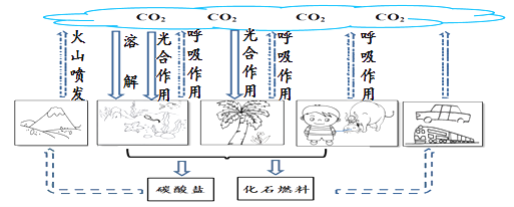
(1)自然界释放CO2的方式主要有火山喷发、________和化石燃料的燃烧。化石燃料是指天然气、煤和________。天然气燃烧的化学方程式为________。
(2)二氧化碳的过量排放会造成温室效应,依据图示分析,控制温室效应发生的有效措施有________、________。
(3)二氧化碳被碱性物质吸收可形成碳酸盐。澄清石灰水吸收CO2的化学方程式为________。CO2被氨水吸收转化为可作氮肥的NH4HCO3。NH4HCO3固体中氮元素的质量分数为________%(计算结果精确到0.1%)。
(4)CO2形成的超临界CO2流体可用于从香兰草豆荚粉中提取香兰素(C8H8O3)。
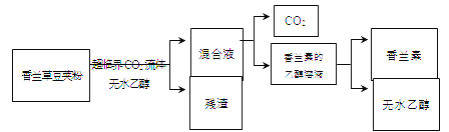
① 由香兰素的乙醇溶液得到香兰素的过程中,发生的变化是________。
② 以上提取香兰素的过程中,可循环使用的物质有________。
③ 在该生产流程中,你想进一步了解的问题是________。
(5)化学物质在生活中的应用方法都是由他们的性质决定的。
①稀有气体常用做焊接金属的保护气,是因为________。
②干冰可用于制做舞台云雾,利用了干冰________的性质。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com