
【题目】下列图象能正确反映其对应关系的是( )
A.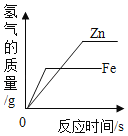 等质量的锌粉和铁粉分别与等质量分数的足量稀盐酸反应
等质量的锌粉和铁粉分别与等质量分数的足量稀盐酸反应
B.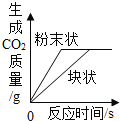 等质量,不同颗粒大小的碳酸钙分别与等质量分数的足量稀盐酸反应
等质量,不同颗粒大小的碳酸钙分别与等质量分数的足量稀盐酸反应
C.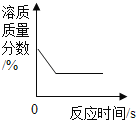 常温下,烧杯中的 KNO3的饱和溶液中,恒温蒸发一定质量的水
常温下,烧杯中的 KNO3的饱和溶液中,恒温蒸发一定质量的水
D.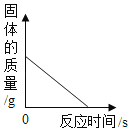 CO 还原一定质量的氧化铁,固体质量随反应时间的变化关系
CO 还原一定质量的氧化铁,固体质量随反应时间的变化关系
【答案】B
【解析】
A、等质量的锌粉和铁粉分别与等质量分数的足量稀盐酸反应,锌比铁活泼,反应需要时间短,最终铁和稀盐酸反应生成的氢气多,该选项对应关系不正确;
B、等质量,不同颗粒大小的碳酸钙分别与等质量分数的足量稀盐酸反应,粉末状碳酸钙和稀盐酸接触面积大,反应速率快,反应需要时间短,最终生成二氧化碳质量相等,该选项对应关系正确;
C、常温下,烧杯中的KNO3的饱和溶液中,恒温蒸发一定质量的水,部分硝酸钾析出,仍然是饱和溶液,温度不变,因此溶解度不变,溶质质量分数也不变,该选项对应关系不正确;
D、氧化铁和一氧化碳反应生成铁和二氧化碳,最终固体质量不能是0,该选项对应关系不正确。
故选:B。


 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:初中化学 来源: 题型:
【题目】某工厂产生的废渣主要成分是含钙的化合物(杂质为Fe2O3)。用该废渣制取CaCl2晶体(CaCl2·xH2O)并进行组成测定,其制取的流程如下图所示:
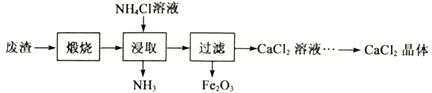
已知:NH4Cl溶液显酸性,且浓度越高酸性越强
(1)XRD图谱可用于判断某固态物质是否存在。右图为煅烧前后废渣的XRD图谱。写出煅烧时发生的化学反应方程式________________________________。
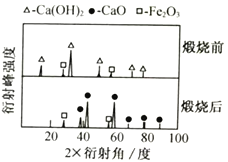
(2)浸取时需连续搅拌,其目的是_________________;生成的NH3能使湿润的红色石蕊试纸变____________色。
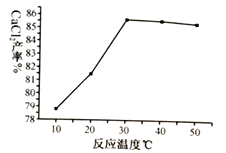
(3)在其它条件相同的情况下,CaCl2的产率随浸取温度的变化如下图所示。则宜选择的浸取温度为____________℃左右。
(4)若使用过量浓度较高的NH4Cl溶液,则所得CaCl2溶液中会含有NH4Cl、_______(填化学式)等杂质。
(5)过滤得到的Fe2O3在高温下可与CO反应,写出该反应的化学方程式____________。
(6)测定晶体(CaCl2·xH2O)的组成:
a.称取14.7000g CaCl2晶体于锥形瓶内,加入适量蒸馏水.使其全部溶解。
b.再向其中加入足量的Na2CO3溶液,静置。
C.过滤、洗涤、干燥、称量,得到10.0000g固体。
①通过计算,确定x的值(写出计算过程)。______________________。
②判断步骤b中沉淀完全的方法是:静置,向上层清液中滴加__________,则说明已沉淀完全;若沉淀不完全,则测得的x值比实际值______(填“偏大”、“偏小”或“ 不变”。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向硝酸亚铁、硝酸银、硝酸镁的混合溶液中加入一定量的锌粉,充分反应后过滤,得到滤液和滤渣。
(1)若向滤渣中加稀盐酸无气泡,则滤液中一定含有的金属离子为_____________(填符号)。要进一步确定可能含有的溶质,可在滤液中加入_____________溶液。
(2)若反应前后溶液的质量不变,则分别与硝酸亚铁、硝酸银反应的锌的质量比为______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属M与AgNO3溶液反应的化学方程式为:M+2AgNO3=M(NO3)2+2Ag。则下列说法错误的是( )
A.M的金属活动性比Ag强B.金属M可能是铝
C.该反应属于置换反应D.该反应前后M的化合价发生了改变
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属钛(Ti)因具有许多神奇的性能而越来越引起人们的关注,被誉为“未来金属“。常温下钛不和非金属、强酸反应,加热至红热时,能与常见的非金属反应。工业上由钛铁矿(主要成分为FeTiO3)制取金属钛的主要工艺过程如图:
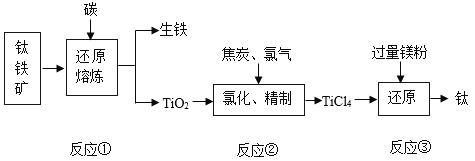
(1)反应前将钛酸亚铁和焦炭磨成粉末状的原因是_____。
(2)TiO2与C、Cl2在高温下反应,生成TiCl4和一种有毒气体,该气体是一种氧化物,其化学式为_____。
(3)写出步骤③中(Ar起保护气作用)在高温时生成金属钛的化学反应方程式_____,该反应的基本类型为_____。
(4)今年来,工业上用电解熔融的TiO2来制取金属钛获得成功,从能量的角度分析,工业利用该方法制备金属Ti的缺点是_____。
(5)如何从反应③后的固体中获得金属钛:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图象分别与选项中的操作相对应,其中不合理的是( )
A.  向一定量的稀醋酸中加入水
向一定量的稀醋酸中加入水
B.  向一定量的锌粉中加入盐酸
向一定量的锌粉中加入盐酸
C.  加热一定量的高锰酸钾固体
加热一定量的高锰酸钾固体
D.  一定温度时向一定量的石灰水中加入氧化钙
一定温度时向一定量的石灰水中加入氧化钙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】Na2CO3在工业和生活中有重要的作用。它的来源主要有以下两种途径:
I.将制碱与制氨结合起来的联合制碱法。这个方法是由我国的制碱工业先驱_发明的。
A 张青莲
B 道尔顿
C 侯德榜
D 华罗庚
Ⅱ.自然界有很多咸水湖,人们通过“冬天捞喊,夏天晒盐”的方式获得湖盐,其中就含有Na2CO3。
(1)小明同学想对某夏天制得的湖盐样品成分进行探究,查阅资料后他对样品成分做出了三种猜想。
猜想一:NaCl、Na2CO3
猜想二:NaCl、Na2SO4;
猜想三:NaCl、Na2CO3、Na2SO4请帮助他完成如下实验:
实验操作 | 实验现象 | 实验结论 | |
实验一 | 取少量样品于试管中,加适量水溶解后,加入过量稀HNO3 | 产生能使澄清石灰水变浑浊的气体 | 猜想___不成立 |
实验二 | 向实验一所得的溶液中加入适量的________ | __ | 猜想三成立 |
(2)小明同学为进一步确定上述湖盐样品中Na2CO3 的质量分数,取该湖盐样品10.0g做了如图所示的补充实验。(注:所用药品均足量)
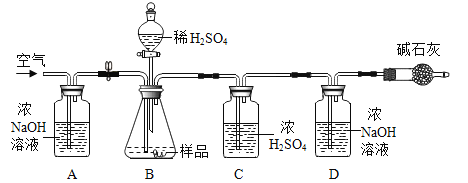
①反应结束之后打开止水夹并通入空气的目的是____。
②装置D中发生的反应为____(用化学方程式表示)。
③实验中碱石灰(含氧化钙和氢氧化钠)的作用是___。
④实验结束后,测得装置D增重0.33g,则该湖盐样品中Na2CO3的质量分数为多少___?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示,试管中盛有一段镁条,向试管中加入过量稀盐酸,观察到U形管中a处液面下降,b处液面上升。回答下列问题:
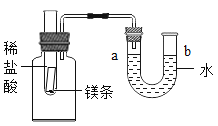
(1)镁条与稀盐酸反应的化学方程式为_____。
(2)U形管中液面发生变化的原因是_____。
(3)将试管中的物质换成水和另一种固体,可以让U型管内产生同样现象,则“另一种固体”是_____;若U型管内b处液面下降,a处液面上升,则“另一种固体”是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】建立宏观与微观之间的联系,是化学学科特有的思维方式。
(1)图中A、B、C、D是四种粒子的结构示意图,E是碘元素在元素周期表中的信息。回答下列问题:
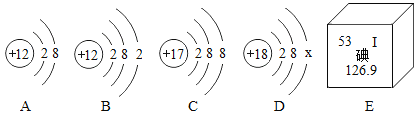
①A、B、C、D四种粒子共表示_______________种元素。
②构成氯化镁的微粒是________________(填字母序号)。
③E中碘元素原子的核内质子数为______________________。
(2)如图是某化学反应微观示意图。在点燃条件下,A和B反应生成C和D。
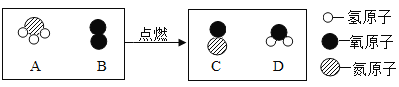
①1个A分子中含有__________个原子。
②A中氮元素和氢元素的质量比为____________________。
③A在B中充分燃烧的化学方程式为____________________。
④生成C与D的质量比是____________________。
(3)请你根据表中信息,类推出丙酸的化学式____________________。
物质名称 | 甲酸 | 乙酸 | 丙酸 | 丁酸 | 戊酸 |
化学式 | CH2O2 | C2H4O2 | ? | C4H8O2 | C5H10O2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com