


 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:初中化学 来源: 题型:阅读理解
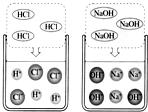 24、某化学兴趣小组利用“稀盐酸、硫酸铜、氢氧化钠、氯化钡”几种物质对复分解反应进行再探究.
24、某化学兴趣小组利用“稀盐酸、硫酸铜、氢氧化钠、氯化钡”几种物质对复分解反应进行再探究.| 实验步骤 | 实验现象 | 实验结论 |
| 编号 | 实验 | 现象 |
| 1 | 向盛有CuSO4溶液的试管里加入适量的 NaCl溶液. |
没有明显变化,溶液仍为蓝色 |
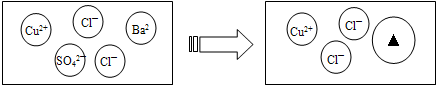
| 2 | 向盛有CuSO4溶液的试管里加入适量的 BaCl2溶液. |
有 白色沉淀 生成,滤液为蓝色 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解


查看答案和解析>>
科目:初中化学 来源: 题型:
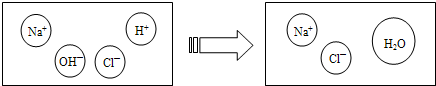
 17、已知M、N分别是稀盐酸、氢氧化钠溶液中的一种.某化学兴趣小组同学在一定量的M中不断滴加N,并测定所得溶液的pH值,如图所示.
17、已知M、N分别是稀盐酸、氢氧化钠溶液中的一种.某化学兴趣小组同学在一定量的M中不断滴加N,并测定所得溶液的pH值,如图所示.| 实验步骤 | 实验现象 | 结论 |
| 取少量该溶液,向其中滴加石蕊溶液(合理即可) | 溶液变红 | 为c处溶液,并推知溶液中的离子有 Na+、H+、SO42- (填写离子符号) |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验操作 | 实验现象 | 实验结论 | |
甲同学 |
取烧杯中溶液少许于试管中,向其中滴加 紫色石蕊试液 紫色石蕊试液 |
现象:溶液变为红色 | 溶液显酸性(含有H+);溶质中有氯化氢. |
乙同学 |
取烧杯中溶液少许于试管中,向其中加入少量锌粒 | 现象: 锌粒逐渐溶解,有气泡产生 锌粒逐渐溶解,有气泡产生 反应的化学方程式是: Zn+2HCl=ZnCl2+H2↑ Zn+2HCl=ZnCl2+H2↑ | |
丙同学 |
取烧杯中溶液少许于试管中,向其中加入少量石灰石 | 现象: 石灰石逐渐溶解,有气泡产生 石灰石逐渐溶解,有气泡产生 |
查看答案和解析>>
科目:初中化学 来源: 题型:
 铝、铁、铜是人类广泛使用的三种金属,与我们生活息息相关.图1是稀释浓硫酸实验的示意图.
铝、铁、铜是人类广泛使用的三种金属,与我们生活息息相关.图1是稀释浓硫酸实验的示意图.| 实验步骤 | 实验现象 | 结 论 |
取少量该溶液, 取少量该溶液, 向其中滴加 向其中滴加 石蕊 石蕊 溶液 溶液 |
溶液变红 溶液变红 |
为c处溶液,并推知溶液中的离子有 Na+、H+、SO42- Na+、H+、SO42- (填离子符号) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com