
分析 (1)物质的性质决定物质的用途,根据各种物质的性质分析解答;
(2)根据在原子中,质子数=原子序数=核电荷数=核外电子数,在阳离子中,质子数=原子序数=核电荷数>核外电子数;在阴离子中质子数=原子序数=核电荷数<核外电子数,据此解答.
(2)由题意知,质子数为10的分子,须为两种粒子化合而成.
解答 解:Ⅰ、(1)聚乙烯塑料可用于制食品包装袋,故填:B;
(2)碘酒中的溶剂是乙醇,故填:C;
(3)活性炭具有吸附性,能够吸附色素和异味,故填:A;
(4)葡萄糖可为人体提供营养,故选:D.
Ⅱ、在原子中,质子数=原子序数=核电荷数=核外电子数,在阳离子中,质子数=原子序数=核电荷数>核外电子数;在阴离子中质子数=原子序数=核电荷数<核外电子数.
(1)质子数为10的原子氖;
(2)质子数之和为10的不同的分子是水或氨气,其符号分别为:H2O、NH3;
(3)NH4+中N原子的质子数为7,H原子的质子数为1,所以NH4+的质子数为11,电子数=11-1=10.
(4)OH-中质子数为9,电子数=9+1=10,所以OH-是电子数为10的阴离子.
故答案为:(1)Ne;(2)H2O(或NH3);(3)NH4+;(4)OH-.
点评 本题考查的知识点多,而且有一定的难度.


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 滤渣中一定含Cu,可能含Zn | B. | 滤液中只有ZnSO4 | ||
| C. | 滤液中只有CuSO4 | D. | 向滤渣中滴加稀盐酸,无气泡产生 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 滤渣中只有Ag | B. | 滤渣中一定有Fe | ||
| C. | 滤渣中一定有Zn | D. | 滤渣中一定有Zn、Fe、Ag |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 ”均为铜片),只需完成实验B和D即可达到探究目的(填字母).
”均为铜片),只需完成实验B和D即可达到探究目的(填字母).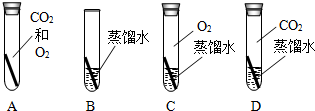
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 能使燃着的木条熄灭的气体可能是二氧化碳 | |
| B. | 化学变化的过程中常会伴随能量的变化 | |
| C. | 分子、原子、离子等都是构成物质的微粒 | |
| D. | 使无色酚酞试液变红色的溶液一定是碱溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 养成“周密设计、规范操作”的良好实验习惯,是完成化学实验的关键.在化学课上,同学们对蓝色沉淀Cu(OH)2产生了浓厚的兴趣.
养成“周密设计、规范操作”的良好实验习惯,是完成化学实验的关键.在化学课上,同学们对蓝色沉淀Cu(OH)2产生了浓厚的兴趣.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ③ | D. | ①③ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com