
实验室中有一瓶氢氧化钠固体,因不慎敞口放置了一段时间,已经部分变质。化学课外兴趣小组的同学决定测定该瓶试剂变质的程度,他们根据所学知识,依次进行了如下的实验操作:①取该瓶中的试剂30g加水配制成溶液A;②向溶液A中加入足量澄清的石灰水;③过滤、干燥、称量,得到4g白色沉淀。
试回答下列问题:
(1)叙述氢氧化钠固体敞口放置变质的原因是 。
(2)若向上述变质的氢氧化钠固体中加入足量的稀盐酸,能观察到的一个明显现象是
。
(3)写出溶液A中的溶质(填化学式) 。
(4)计算该30g试剂中含有杂质Na2CO3的质量分数(最终结果精确到0.1%)
 智能训练练测考系列答案
智能训练练测考系列答案科目:初中化学 来源: 题型:
 28、实验室中有一瓶无色液体,经测定其中只含氢、氧两种元素.请你对该无色液体进行如下探究活动,请回答下列问题:
28、实验室中有一瓶无色液体,经测定其中只含氢、氧两种元素.请你对该无色液体进行如下探究活动,请回答下列问题:| 实验步骤 | 实验现象 | 实验结论 |
| 取少量无色液体,加入盛有少量黑色二氧化锰的试管中 | 若有气泡 若无气泡 |
该液体是H2O2 该液体是H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:
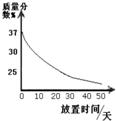


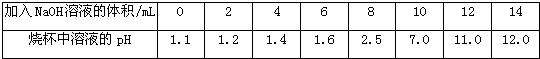
查看答案和解析>>
科目:初中化学 来源: 题型:
 实验室有一瓶氢氧化钾浓溶液,瓶上标签内容如图所示,请你根据签上提供的数据解答下列问题:
实验室有一瓶氢氧化钾浓溶液,瓶上标签内容如图所示,请你根据签上提供的数据解答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:




查看答案和解析>>
科目:初中化学 来源:北京模拟题 题型:填空题


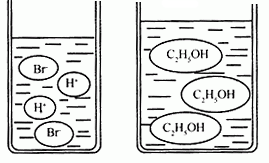
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com