
【题目】金属是重要的资源,与我们的生活息息相关。
(1)铜制插头是利用了金属铜的____性。选择锰钢而不用纯铁制造自行车车架的主要原因是_______。
(2)小明同学探究铝、铜、银三种金属的活动性顺序,设计了如图所示的方案。
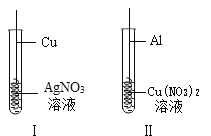
①I中发生反应的化学方程式为____________。一段时间后可观察到II中铝丝表面_________________。
②通过以上实验,______ (填“能”或“不能”)得出三种金属的金属活动性由强到弱的顺序为:Al>Cu>Ag
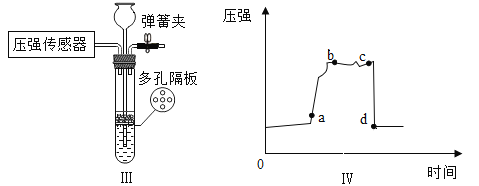
(3)实验室用锌粒和稀硫酸制取氢气的化学方程式为____________。Ⅲ可作为制取氢气的发生装置,为研宄该装置的工作原理,利用压强传感器测定制取氢气过程中的压强变化(如IV所示)。请描述ab时间段装置内出现的现象__________________。cd时间段对应的操作是_______
(4)己知碳在高温时与氧化锌完全反应得到锌和二氧化碳,要使81g氧化锌完全还原,需要碳的质量至少是多少?(写出计算过程)__________
【答案】导电 锰钢硬度大于纯铁 ![]() 逐渐生成一层红色固体 能
逐渐生成一层红色固体 能 ![]() 锌粒表面持续产生气泡,试管内液面逐渐下降至多孔隔板以 下 打开弹簧夹 6g
锌粒表面持续产生气泡,试管内液面逐渐下降至多孔隔板以 下 打开弹簧夹 6g
【解析】
(1)铜制插头是利用铜导电,故是利用了铜的导电性;
锰钢属于铁的合金,合金比组成它的纯金属的硬度大,抗腐蚀性好,选择锰钢而不用纯铁制造自行车车架的主要原因是:锰钢硬度大于纯铁;
(2)①I中发生反应为铜与硝酸银反应生成硝酸铜和银,该反应的化学方程式为:![]() ;
;
II中铝与硝酸铜反应生成硝酸铝和铜,故一段时间后,可观察到II中铝丝表面逐渐生成一层红色固体;
②铝能与硝酸铜反应生成硝酸铝和铜,说明在金属活动性顺序里,铝的金属活动性比铜强,铜能与硝酸银反应生成硝酸铜和银,说明在金属活动性顺序里,铜比银活泼,故通过以上实验,能得出三种金属的金属活动性由强到弱的顺序为:Al>Cu>Ag;
(3)实验室用锌粒和稀硫酸反应制取氢气,锌与稀硫酸反应生成硫酸锌和氢气,该反应的化学方程式为:![]() ;
;
ab段压强逐渐增大,说明锌与稀硫酸反应生成了氢气,气体增多,装置内压强增大,在压强差的作用下,试管里的液体被压入长颈漏斗中,故实验现象为:锌粒表面持续产生气泡,试管内液面逐渐下降至多孔隔板以下,反应停止没有气泡生成;
cd时间段压强逐渐减小至恢复原大小,故应该是打开了弹簧夹,试管内的气体逸出,压强减小,故填:打开弹簧夹;
(4)解:设需要碳的质量为x
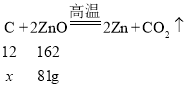
![]()
x=6g
答:需要碳的质量为6g。


科目:初中化学 来源: 题型:
【题目】如图所示为a、b、c三种物质的溶解度曲线。
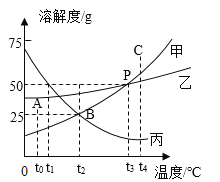
(1)B点表示:t2℃时,甲物质的溶解度是_____g。
(2)t2℃时,将15g甲物质加入到50g水中,充分溶解后所得溶液是______(填“饱和溶液”或“不饱和溶液”)。该溶液的溶质质量分数为______。
(3)若甲中混有少量的乙物质,提纯甲物质常采用的方法是______。
(4)将t3℃甲、乙、丙的饱和溶液降温至t2℃,溶液中溶质质量分数大小关系是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某班学生在老师指导下探究铁与水蒸气的反应,请帮助他完成下列实验报告。
(1)按图甲装好药品,连接装置(夹持仪器已略去)。其中A装置的作用是:_______
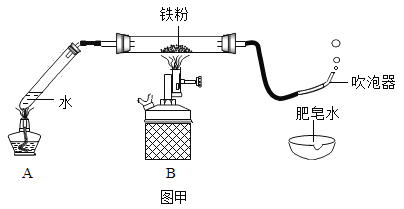
(2)加热一段时间后,灰色铁粉逐渐变黑,吹泡器连续吹出气泡,且气泡向上飞起;用燃着的木条靠近气泡,能产生爆鸣。
(3)同学们讨论后认为:铁与水蒸气反应生成的固体是“铁的一种氧化物”,玻璃管内的黑色固体中还可能含有“过量的铁”。
(查阅资料)铁有三种氧化物(FeO、Fe2O3、Fe3O4),其中FeO接触到空气会立即由黑色变为红棕色;铁的三种氧化物都不与硫酸铜溶液反应。
(实验探究)
实验步骤 | 实验现象 | 实验结论 |
倒出玻璃管中黑色固体,平铺于白纸上 | 黑色固体不变色 | 黑色固体中一定没 有_____(填物质名称) |
取上述黑色固体少许,装入试管,加入足量硫酸铜溶液 | _____ ,有红色固体出现 | 黑色固体中一定 含有_____。 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学课外小组对生活中另外一种常见金属铜在空气中能否生锈进行了以下探究:
[提出问题![]() 铜在空气中长期放置会生锈吗?生锈的条件是什么?
铜在空气中长期放置会生锈吗?生锈的条件是什么?
![]() 查阅资料
查阅资料![]() 铜在朝湿的空气中会慢慢生锈变绿,俗称铜绿,主要成分为碱式碳酸铜,化学式为Cu2(OH)2CO3
铜在朝湿的空气中会慢慢生锈变绿,俗称铜绿,主要成分为碱式碳酸铜,化学式为Cu2(OH)2CO3
![]() 作出猜想
作出猜想![]() (1)小组成员一致认为,铜生锈可能是铜与空气中的氧气、________共同作用的结果,他们猜想的依据是___________________。
(1)小组成员一致认为,铜生锈可能是铜与空气中的氧气、________共同作用的结果,他们猜想的依据是___________________。
![]() 设计实验
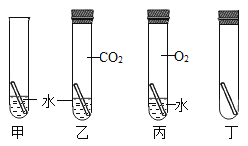
设计实验![]() 同学们设计如图实验,探究铜生锈条件:将完全相同的铜片放入不同环境中,观察生锈情况。
同学们设计如图实验,探究铜生锈条件:将完全相同的铜片放入不同环境中,观察生锈情况。
(2)小组同学讨论认为仅完成甲、乙、丙三个实验不能得出实验结论,于是又用丁试管补充了一个实验,装置中除了铜片外,还应该加入__________。
[观察现象]放置两周后,发现甲中的铜片变绿了,乙丙丁中的铜片没变化。
[得出结论]
(3)甲和乙对比,得出的结论是铜生锈需要与________接触。
(4)甲和丙对比,得出的结论是铜生锈需要与________接触。
(5)写出铜生锈生成碱式碳酸铜的的化学反应方程式是______________________。
[反思拓展]
(6)乙和丙中使用的是煮沸后迅速冷却的蒸馏水,目的是_______________________。
(7)小明发现从不同地点收集到的两个铜器(一个是纯铜做的,一个是青铜做的)中,纯铜器的铜绿比青铜器的少,他据此分析认为青铜比纯铜易锈蚀。小明的分析是否全面?请你说明理由:________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】镁条在空气中久置表面会变黑,对镁条变黑条件及黑色物质成分作如下探究。
(查阅)①氮化镁![]() 是黄色固体。②
是黄色固体。②![]() 可与
可与![]() 发生化合反应生成硫酸钠。③
发生化合反应生成硫酸钠。③![]() 溶液能吸收
溶液能吸收![]() 气体
气体
(猜测)镁条变黑可能原因:①空气中![]() 使镁条变黑;②空气中的
使镁条变黑;②空气中的![]() 使镁条变黑;③
使镁条变黑;③![]() ,猜想①、②均不合理,理由分别是______、______。
,猜想①、②均不合理,理由分别是______、______。
(实验)用图示装置![]() 镁条长度及试管容积均相同
镁条长度及试管容积均相同![]() ,分别进行下列实验。20天后,前3支试管中镁条始终无明显变化,仅试管D中线条表面全部变黑。
,分别进行下列实验。20天后,前3支试管中镁条始终无明显变化,仅试管D中线条表面全部变黑。
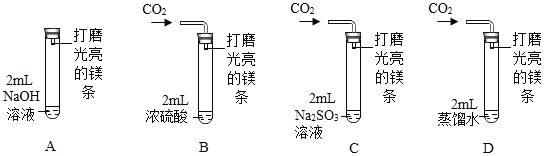
(结论)
![]() 试管C中,
试管C中,![]() 溶液的作用是______
溶液的作用是______![]() 用化学方程式表示
用化学方程式表示![]() 。
。
![]() 得出“镁条变黑一定与
得出“镁条变黑一定与![]() 有关”结论,依据的实验是______
有关”结论,依据的实验是______![]() 试管编号
试管编号![]() 与D对照。
与D对照。
![]() 由上述实验推知,镁条变黑与______
由上述实验推知,镁条变黑与______![]() 填序号
填序号![]() 有关。
有关。
![]() 和
和![]() 和
和 ![]() 和
和 ![]() 、
、![]() 和
和 ![]()
(反思与评价)
![]() 在猜想与假设时,同学们认为镁条变黑与N2无关,其理由是________________。
在猜想与假设时,同学们认为镁条变黑与N2无关,其理由是________________。
![]() 欲进一步证明镁条表面的黑色物质中含有碳酸盐,所需要的试剂是__________。
欲进一步证明镁条表面的黑色物质中含有碳酸盐,所需要的试剂是__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学实验中处处表现出颜色变化美。已知 A、B、F 均为黑色固体,C 为紫红色金属,D、E 是组成元素相同的无色气体;G 为红棕色固体,H 溶液呈蓝色。这些物质的相互转化关系如图所示,其中部分生成物已省略。
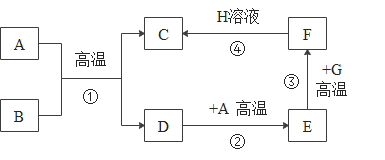
(1)写出下列物质的化学式:C_____________,E_____________。
(2)反应①的化学方程式为_____________________,属于____________反应(填基本 反应类型)。
(3)反应④中可观察到:溶液由蓝色变为________________色。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知 KNO3的溶解度如下表所示,下列说法不正确的是
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
溶解度/g | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
A.在 10℃-70℃之间,随着温度的升高,KNO3的溶解度增大
B.20℃时,向 100 g 水中加入 35 g KNO3,充分搅拌,所得溶液质量为 131.6 g
C.将 70℃时不饱和的 KNO3溶液降低温度,有可能转化为饱和溶液
D.50℃时,饱和 KNO3溶液中溶质的质量分数为 85.5%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某种催化剂可将汽车尾气中的一氧化碳、二氧化氮转化为两种空气中的无毒成分,反应的微观示意图如下。下列说法正确的是
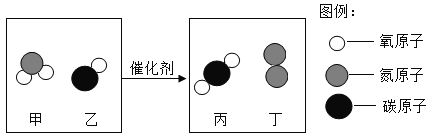
A.四种物质均属于化合物
B.物质丁由原子构成
C.参加反应的甲与生成的丁的分子个数比为2:1
D.参加反应的甲与乙的质量比为1:2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com