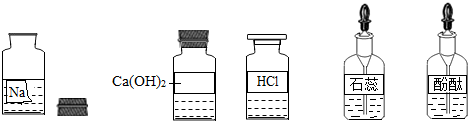
(2011?百色)某校兴趣小组同学准备进行常见酸、碱、盐的性质实验时,发现实验台上摆放的药品中(如图),有一装溶液的试剂瓶未盖瓶盖且标签破损,于是决定对这瓶溶液进行实验探究:

【提出问题】这瓶溶液是什么溶液?
【获得信息】酸、碱、盐的性质实验中用到含有钠元素的物质是氯化钠、氢氧化钠、碳酸钠
【提出猜想】这瓶溶液是:猜想一:氯化钠溶液;猜想二:氢氧化钠溶液;
猜想三:碳酸钠溶液.
【实验推断】
(1)小丽取样滴加无酚酞试液,溶液呈红色,得出结论:该溶液不可能是
氯化钠溶液
氯化钠溶液
溶液,理由是
氯化钠溶液呈中性,不能使酚酞试液变色
氯化钠溶液呈中性,不能使酚酞试液变色
;
(2)小刚另取样滴加稀盐酸有
气泡
气泡
产生,反应的化学方程式为
Na2CO3+2HCl=2NaCl+H2O+CO2↑
Na2CO3+2HCl=2NaCl+H2O+CO2↑
,小刚得出结论:该溶液是碳酸钠溶液.
(3)小青认为小刚的结论不完全正确,理由是
露置于空气中的NaOH溶液与空气中的CO2反应也生成碳酸钠
露置于空气中的NaOH溶液与空气中的CO2反应也生成碳酸钠
.小组同学讨论后一致认为还需要进行如下实验:
【继续探究】另取样加入过量的CaCl
2溶液,观察到有
白色沉淀
白色沉淀
产生,设计这一步骤的目的是
完全除去溶液中的CO32-,避免其对OH-检验造成干扰
完全除去溶液中的CO32-,避免其对OH-检验造成干扰
;静置后,取上层清液,滴入酚酞试液,溶液呈红色.

【实验结论】这瓶溶液是
NaOH溶液(填变质的NaOH溶液也可)
NaOH溶液(填变质的NaOH溶液也可)
.
【探究启示】实验取完药品后应
立即盖好瓶盖,重新贴上标签
立即盖好瓶盖,重新贴上标签
.
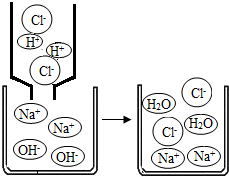
【拓展迁移】若该溶液与盐酸发生中和反应,恰好完全反应的微观过程如图所示,反应的实质表达式为:H
++OH
-=H
2O,则反应后溶液中存在的阴、阳离子是
Cl-、Na+
Cl-、Na+
(填符号);
【继续探究】实验中加CaCl
2溶液反应的实质表达式:
Ca2++CO32-=CaCO3↓
Ca2++CO32-=CaCO3↓
(用化学符号表示)



 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案