
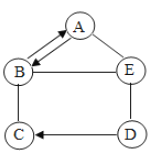
【题目】已知A、B、C、D、E分别为氧化铜、硫酸、氢氧化钠、硫酸铜和碳酸钠中的一种,它们之间的反应或转化关系如图(部分物质和反应条件已略去),已知C的溶液显蓝色,B属于碱。写出B转化为A的化学方程式:________;A和E反应的化学方程式:________;B和E反应从微观角度分析其实质是________。
【答案】CO2+2NaOH=Na2CO3+H2O Na2CO3+H2SO4=Na2SO4+H2O+CO2↑ 酸中的H+和碱中的OH-结合成H2O
【解析】
根据C是蓝色溶液可知,C为硫酸铜,B属于碱,则B为氢氧化钠;由于B(氢氧化钠)能与A相互转化,则A为碳酸钠,碳酸钠和氢氧化钙反应可以生成氢氧化钠,氢氧化钠和二氧化碳反应可以生成碳酸钠;而E即能与氢氧化钠反应,又能与碳酸钠反应,则E为硫酸,那么D则为氧化铜,氧化铜能和硫酸反应转化为硫酸铜;
根据分析知,B转化为A ,可以是二氧化碳和氢氧化钠的反应,方程式为:CO2+2NaOH=Na2CO3+H2O
A和E 的反应即碳酸钠和硫酸反应,方程式为: Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
B和E反应是酸和碱的反应,即中和反应,中和反应的实质是氢离子和氢氧根离子结合生成水。


 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案科目:初中化学 来源: 题型:
【题目】丁基锂(C4H9Li)是橡胶合成工业中一种常用的试剂。白色粉末,熔点﹣95℃,沸点80℃,遇水、空气均易自燃。下列关于丁基锂的说法正确的是( )
A.丁基锂是由4个碳原子、9个氢原子、1个锂原子构成的
B.丁基锂中碳元素质量分数为75%
C.丁基锂运输或使用过程中如果发生燃烧,可以用水浇灭
D.丁基锂相对分子量为64g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某纯碱样品中含有少量NaCl,小丽同学取该样品23g全部溶解于150g水中,再逐滴加入160g稀盐酸,反应中产生的气体的质量与盐酸的用量关系如图所示。(提示:相关反应为Na2CO3+2HCl=2NaCl+H2O+CO2↑)计算当恰好完全反应时:

(1)产生的二氧化碳的质量是 克。
(2)此时所得到的溶液中溶质的质量分数(写出必要的计算过程,结果保留到0.1%)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A~G是初中化学常见的7种物质,其中至少有一种物质是无色气体,且A与G含有相同的金属元素。它们在一定条件下转化关系如下图所示,其中部分反应物或生成物已略去。 请针对以下两种情况回答问题:
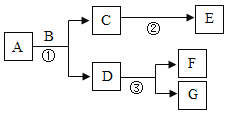
(1)若A中两种元素的质量比为7:3,F是一种红色金属,则F的化学式为________;写出反应①、③的化学方程式:①_____________ ; ③__________ 。
(2)若F与C常温下可以反应,②、③属于同一种基本反应类型,则A的化学式为______ ;写出反应①的化学方程式____________________ ;反应②的基本反应类型是_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是盐酸性质的知识归纳,下列说法不正确的是()
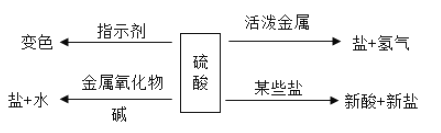
A.若盐为AgNO3溶液,则反应中有白色沉淀生成
B.若碱为NaOH溶液,则可以在溶液中滴加酚做溶液证明两者发生了中和反应
C.若金属氧化物为Fe2O3 , 盐酸与Fe2O3反应的化学方程式为Fe2O3+6HCl=2FeCl3+3H2O
D.若金属为Al和Fe,将质量相等且过量的两种金属与一定量的同种稀盐酸完全反应,Fe 产生的H2多
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学与生活息息相关,我们要正确认识和使用化学给我们带来的丰富的物质。
(1)人们常用铁锅炒菜,是因为人体血液中需要铁元素,人体缺乏它易患_____病。
(2)在新农村建设中,许多家庭兴建沼气池。沼气的主要成分燃烧的化学方程式是_____
(3)馒头为我们生活中的一种食品。但有些不法商贩为了美观和降低成本,一是添加了柠檬黄(PbCrO4)使馒头着色而美观,二是添加甜味剂代替蔗糖而降低成本,二者均会对人体造成危害。上述中蔗糖属于六大营养素中的_____;柠檬黄中Pb的化合价为+2价,则Cr的化合价为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是初中化学教材中的一些实验,按要求回答下列问题:
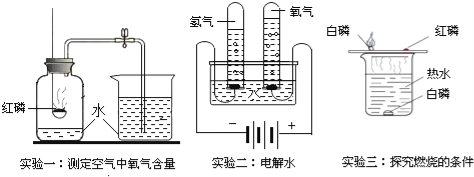
(1)为确保实验一测量结果的准确,需要注意的事项有_________ (写一条即可)
(2)通过水电解生成氢气和氧气的事实,得出的实验结论是_________ .
(3)实验三_________ 事实说明燃烧条件是温度达到着火点.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列化学方程式符合题意且书写正确的是( )
A.正常雨水呈弱酸性的原因:SO2+H2O=H2SO3
B.用稀硫酸可以除铁锈:3H2SO4+Fe2O3=2FeSO4+3H2O
C.用氢氧化铝治疗胃酸过多:Al(OH)3+3HCl=AlCl3+3H2O
D.乙醇可以用做燃料:C2H5OH+2O2=2CO2+2H2O
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】活动小组为测定由氧化铜和铜组成的混合物中氧化铜的质量分数,现取3份该固体混合物各20g,分别缓慢加入到50 g、100 g、150 g某稀硫酸中,测得三组实验数据如下表:
组别 | 第1组 | 第2组 | 第3组 |
稀硫酸质量/g | 50 | 100 | 150 |
剩余固体的质量/g | 10.0 | 4.0 | 4.0 |
根据实验及有关数据进行分析与计算:
(1)第1组实验中_____________(填“氧化铜”“稀硫酸”或“氧化铜与稀硫酸”)完全反应。
(2)样品中氧化铜的质量分数是__________g。
(3)根据第1组实验数据计算所用的稀硫酸溶质的质量分数__________(写出计算过程)。
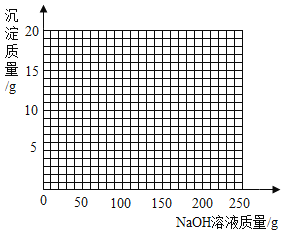
(4)若将第2组实验后的混合物过滤,在滤液中滴加10%的NaOH溶液,请画出在该混合溶液中加入10% NaOH溶液的质量与生成沉淀质量变化关系的曲线图__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com