
【题目】有一包固体,可能是Cu(NO3)2、K2SO4、KCl、K2CO3、KOH中的一种或几种组成。为了探究该固体的组成,某化学小组设计并开展以下实验:
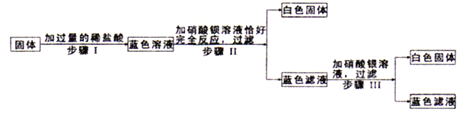
已知,步骤I中固体全部消失,溶液呈蓝色,无气泡产生,步骤II、III中均可观察到有白色沉淀生成。
请回答下列问题:
(1)经推论,原固体中一定不含K2CO3,理由是___________________
(2)原固体中一定含有的物质是________________。
(3)步骤II中产生白色沉淀的化学方程式是_______________。
(4)步骤III所得蓝色滤液中一定含有的阳离子是____________。
【答案】 向固体中加入过量的稀盐酸时,无气泡产生 Cu(NO3)2、K2SO4 Ba(NO3)2+K2SO4=BaSO4↓+2KNO3 Cu2+、K+、H+
【解析】本题是推断题。首先分析题中所给物质的性质和两两之间的反应,然后依据题中的现象判断各物质的存在性,最后进行验证即可。解题时注意加入试剂的量对反应后溶液成分的影响。
(1)碳酸钾与盐酸反应生成氯化钾、水和二氧化碳。原固体中一定不含K2CO3,理由是向固体中加入过量的稀盐酸时,无气泡产生;
(2)固体加过量稀盐酸,固体完全溶解且溶液呈蓝色,说明固体中一定有硝酸铜,硝酸铜与氢氧化钾能发生反应不能共存,则说明一定不存在氢氧化钾,根据题(1)的分析固体中一定不含K2CO3,在步骤Ⅰ得到的蓝色溶液中加入硝酸钡溶液有白色沉淀生成,硫酸钾与硝酸钡反应生成硫酸钡沉淀和硝酸钾,说明固体中一定有硫酸钾,在步骤Ⅱ得到的蓝色溶液中加入硝酸银溶液产生白色沉淀,含氯离子的溶液与硝酸银反应生成氯化银的沉淀,由于在步骤Ⅰ中加入了盐酸,不能说明固体中一定有氯化钾,所以原固体中一定含有的物质是Cu(NO3)2、K2SO4;
(3)步骤II中产生白色沉淀的反应是硫酸钾与硝酸钡反应生成硫酸钡沉淀和硝酸钾,化学方程式是Ba(NO3)2+K2SO4=BaSO4↓+2KNO3;
(4)根据题(2)中的分析可知,步骤III所得蓝色滤液中一定含有的阳离子是Cu2+、K+、H+。


科目:初中化学 来源: 题型:
【题目】如图是A、B、C三种固体物质的溶解度曲线,请回答下列问题:

(1)P点含义__________________;
(2)t2℃时,将15g A物质放入50g水中,充分溶解后,形成溶液的质量为____g;
(3)若A物质中含有少量的B物质,提纯A物质的方法是_____;(填“降温结晶”或“蒸发结晶”)
(4)t3℃时,将A、B、C三种物质的饱和溶液降温到t1℃,三种溶液中溶质的质量分数由大到小的顺序为___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】学习《海水“制碱”》的知识后,小明在实验室中进行了如下探究活动,请你和小明一起完成下面的实验探究活动。
(1)探究碳酸钠的溶解性:在编号为 A、B、C、D 的四个烧杯中各加入室温下的水 100g,并分别加入取自实验室的碳酸钠固体,搅拌至充分溶解,实验数据记录如下表:
烧杯编号 | A | B | C | D |
水的质量/g | 100 | 100 | 100 | 100 |
加入 Na2CO3 的质量/g | 30 | 35 | 40 | 50 |
溶液的质量/g | 130 | 135 | 140 | 140 |
分析上述数据,烧杯编号为_________中的溶液是饱和溶液。
(2)探究食用纯碱的纯度:小明把家中厨房里的食用纯碱(主要成分是Na2CO3)带到实验室,他称取食用纯碱12.0g放入烧杯中,加入200g水使其完全溶解。现将150g一定浓度的CaCl2溶液逐滴滴入烧杯中,测得滴加氯化钙溶液的质量与生成沉淀的质量关系如下表:
CaCl2 溶液的质量/g | 25 | 50 | 75 | 100 | 125 | 150 |
沉淀的质量/g | 2 | 4 | m | 8 | 10 | 10 |
①m 的数值是 ______。
②计算纯碱样品中碳酸钠的质量分数______(写出计算过程,计算结果保留一位小数)。
③滴加氯化钙溶液过量的目的是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某兴趣小组发现铁钉生锈需要几天的时间,询问老师如何加快铁钉生锈的速度。
老师说氯化物可能加快铁钉生锈的速度。
【提出问题】氯化物对铁钉生锈有怎样的影响?
【查阅资料】
ⅰ.NaCl、CaCl2、CuCl2等由氯离子与金属离子构成的盐属于氯化物。
ⅱ.铜能与氧气反应,生成黑色的CuO。
ⅲ.CuO能与稀硫酸发生反应:CuO + H2SO4 ==== CuSO4 + H2O。
【进行实验、分析解释、获得结论】
实验1:探究氯化物对铁钉生锈速度的影响。
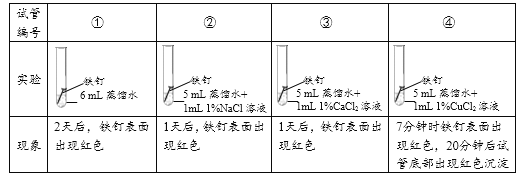
(1)对比实验①②③可以得到的结论是_________。
(2)小组同学认为,试管④中的红色沉淀可能是铁锈,也可能是铜。他们认为红色沉淀可能是铜的理由是__________(用化学方程式解释)。
实验2:探究试管④中红色沉淀的物质组成。
实验步骤 | 实验操作 | 实验现象 |
Ⅰ | 取出试管④中的铁钉,过滤剩余物,洗涤滤纸上的物质 | 固体为红色 |
Ⅱ | 将步骤Ⅰ所得红色固体加入试管中,再向试管中加入足量的___________ | 红色固体大部分溶解,溶液变为黄色 |
Ⅲ | 将步骤Ⅱ所得混合物过滤,洗涤、干燥滤纸上的固体后,置于石棉网上充分加热 | 红色固体变黑 |
Ⅳ | 向试管中加入步骤Ⅲ所得黑色固体,再加入足量稀硫酸 | 黑色固体全部溶解,溶液变为蓝色 |
(3)步骤Ⅱ中所加入的试剂是_________。
(4)步骤Ⅲ、Ⅳ的实验目的是_________。
(5)由实验2可得出结论:试管④中红色沉淀的物质组成是_________。
【反思与评价】
(6)结合实验1、2的结论,对于“氯化物对铁钉生锈速度的影响”,小组同学提出了进一步的假设:__。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学实验小组利用蜡烛进行了下列实验。
实验1:
序号 | 1-1 | 1-2 | 1-3 |
操作 |
|
|
|
现象 | 燃烧的蜡烛保持原状 | 燃烧的蜡烛熄灭 | 剧烈反应,有大量气泡和水雾生成,燃烧的蜡烛熄灭了 |
(1)实验1-2中,燃烧的蜡烛熄灭的原因是____。
(2)实验1-3中,反应生成氧气的化学方程式为___。
实验2:
(提出问题)实验1-3中燃烧的蜡烛为什么会熄灭?
(猜想与假设)
I.蜡烛燃烧生成的二氧化碳导致其熄灭。
II.过氧化氢分解时吸收热量,蜡烛周围的温度降低到着火点以下,导致其熄灭。
III.过氧化氢分解产生的水雾导致蜡烛熄灭。
(进行试验)
序号 | 2-1 | 2-2 | 2-3 |
操作 |
|
|
|
现象 | 有气泡产生,蜡烛火焰无明显变化,温度升高不明显 | 有较多气泡和少量水雾产生,蜡烛燃烧更旺。火焰明亮,温度升高较明显 | 剧烈反应,有大量气泡和水雾产生,燃烧的蜡烛熄灭,温度升高明显 |
(解释与结论)
(3)甲同学认为猜想I不成立,他的依据是____。
(4)通过实验验证,可以得出猜想____(填序号)成立。
(5)上述实验中,能证明氧气有助燃性的实验及现象是____。
(反思与评价)
(6)依据上述实验,若保持实验1-3中蜡烛不熄灭,可采用的方法有___。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】兴趣小组的利用提供的试剂:稀硫酸、澄清石灰水、氯化钠溶液、硫酸铜溶液和紫色石蕊溶液。探究酸碱盐的性质。小清同学将氯化钠溶液加入到稀硫酸中没有观察到明显现象,而将混合溶液加热一段时间后,意外地闻到刺激性气味。
[提出问题]刺激性气味的气体是什么?
[猜想与假设]猜想1.可能是二氧化硫 猜想2.可能是氯化氢
猜想3.可能是氨气
大家讨论后认为猜想3不合理,依据是_____________________。
[查阅资料] SO2和CO2的化学性质相似,都能使澄清灰水变浑浊。写出二氧化硫和氢氧化钙的反应的化学方程式:____________________________。
[实验探究]如图所示,小诚将产生的气体通入紫色石蕊溶液中,观察到_________,于是他认为猜想2正确。
[评价与改进]小煜认为小诚的结论不科学,于是他利用提供的试剂通过实验确认了猜想2正确。
实验操作 | 实验现象 |
如图所示,将产生的气体________________ | _____________________ |
[结论]加热氯化钠与硫酸的混合溶液得到的气体是氯化氢
[拓展应用]实验室可用氯化钠和硫酸反应制取氯化氢气体,已知氯化氢气体极易溶于水。请推测实验室制取氯化氢气体最适宜的方法为________________(填序号)。
A.加热氯化钠溶液和稀硫酸的混合物 B.加热氯化钠固体和稀硫酸的混合物
C.加热氯化钠固体和浓硫酸的混合物
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】a、b、c三种固体物质的溶解度曲线如图,下列说法错误的是( )
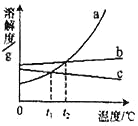
A. t1℃时等质量的a、c饱和溶液中,所含水的质量相等
B. t1℃时a、b、c饱和溶液升温至t2℃,所得溶液的溶质质量分数大小关系是a=b>c
C. 要从含有少量b的a饱和溶液中获得a,最好的方法是降温结晶
D. c物质可能是熟石灰
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向含有和Cu(N03)2和AgNO3的混合溶液中加入一定量的铁粉,并绘制参加反应的铁与溶液中溶质种类的关系图(如图)。下列说法正确的是
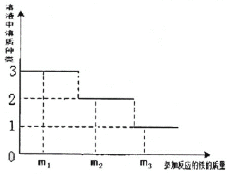
A.当参加反应的铁的质量为m1时,溶质的种类、析出的金属单质种类均为3种
B.当参加反应的铁的质量为m2时,加入盐酸,有白色沉淀生成
C.当参加反应的铁的质量为m3时,溶质为Fe(N03)2
D.当参加反应的铁的质量为m2时,加入稀盐酸,有气泡产生
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图四个图象的变化趋势,能正确描述对应操作的是( )
A. 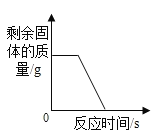 加热一定质量的高锰酸钾固体
加热一定质量的高锰酸钾固体
B. 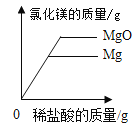 向等质量的镁和氧化镁中分别加入足量的稀盐酸
向等质量的镁和氧化镁中分别加入足量的稀盐酸
C. 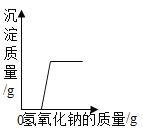 向一定质量的硫酸铜和稀硫酸的混合溶液中逐滴加入氢氧化钠溶液
向一定质量的硫酸铜和稀硫酸的混合溶液中逐滴加入氢氧化钠溶液
D. 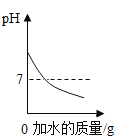 向一定量pH=13的氢氧化钠溶液中滴加大量的水
向一定量pH=13的氢氧化钠溶液中滴加大量的水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com