
【题目】烧杯中盛有CuSO4和H2SO4的混合溶液100.0g,向其中先后滴加BaCl2、NaOH溶液,烧杯中溶液的质量与滴加溶液的质量关系如图所示。

下列说法正确的是
A.ab 段不发生化学反应
B.c点溶液中只含2种溶质
C.该BaCl2溶液的溶质质量分数为41.6%
D.该混合溶液中CuSO4和H2SO4的质量比为80:49
【答案】CD
【解析】
烧杯中盛有CuSO4和H2SO4的混合溶液,向其中先滴加氯化钡溶液,![]() ,
,![]() ,后滴加氢氧化钠溶液,氢氧化钠溶液先和盐酸反应生成氯化钠和水,
,后滴加氢氧化钠溶液,氢氧化钠溶液先和盐酸反应生成氯化钠和水,![]() ,再和氯化铜反应生成氢氧化铜沉淀和氯化钠,
,再和氯化铜反应生成氢氧化铜沉淀和氯化钠,![]() 。
。
A、ab段为氢氧化钠和盐酸反应生成了氯化钠和水,发生了化学反应,不符合题意;
B、c点溶液中含有反应生成的氯化钠、过量的氯化钡、过量的氢氧化钠三种溶质,不符合题意;
C、生成硫酸钡沉淀的质量为:100g+100g-153.4g=46.6g,由化学方程式可知,氯化钡中的钡全部转化为了硫酸钡,故硫酸钡中钡元素的质量为:![]() ,故100g氯化钡溶液中氯化钡的质量为:
,故100g氯化钡溶液中氯化钡的质量为:![]() ,该BaCl2溶液的溶质质量分数为:
,该BaCl2溶液的溶质质量分数为:![]() ,符合题意;
,符合题意;
D、根据![]() ,
,![]() ,
,![]() ,
,![]() ,可得如下关系:CuSO4~CuCl2~2NaOH;H2SO4~2HCl~2NaOH
,可得如下关系:CuSO4~CuCl2~2NaOH;H2SO4~2HCl~2NaOH
设氢氧化钠溶液中溶质的质量分数为a,混合溶液中CuSO4中硫酸铜的质量为x,H2SO4的质量为y
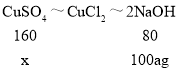
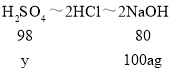
![]()
![]()
x=200ag y=122.5ag
该混合溶液中CuSO4和H2SO4的质量比为:200ag:122.5ag=80:49,符合题意。
故选CD。


 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案科目:初中化学 来源: 题型:
【题目】钛和钛合金被认为是21世纪的重要金属材料,他们具有很多优良的性能,如熔点高,密度小,可塑性好等。以钛铁矿(主要成分为FeTiO3,同时含有少量的Fe2O3、FeO等为原料制TiO2,再由TiO2制金属Ti的工艺流程如下:
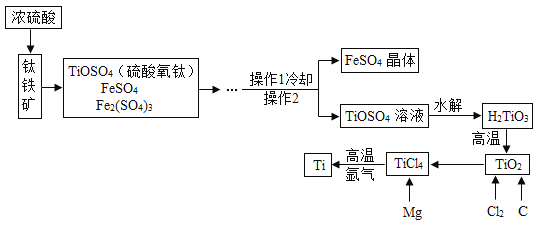
查阅资料:钛、镁在高温下能与空气中的氧气、二氧化碳等反应。
(1)硫酸氧钛(TiOSO4)中钛元素的化合价为_____。
(2)工艺流程中,水解属于_____变化(选填“物理”或“化学”)。
(3)工业上常在高温和氩气氛围中用TiCl4来制备金属Ti,其反应方程式为_____。其中氩气的作用是_____。
(4)TiO2 与焦炭、氯气在高温下反应制取TiCl4,该反应中氯气和碳的质量按71∶12 的比例恰好完全反应,反应的化学方程为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某物质在点燃的条件下发生反应,生成物和反应物共四种,它们的微观示意图和反应前后的质量如下表所示。
物质序号 | 甲 | 乙 | 丙 | 丁 |
|
微观示意图 |
|
|
|
| |
反应前质量/g | 68 | 100 | 1 | 0 | |
反应后质量/g | 0 | x | y | z |
(1)由![]() 构成的物质中
构成的物质中![]() 所代表的元素的化合价为______;
所代表的元素的化合价为______;
(2)表中的四种物质中,属于氧化物的是______ (填化学式);
(3)上述反应的化学方程式为______;
(4)一位同学在计算x、y和z数值的过程中,列出了以下等式,其中正确的是______(填字母序号)。
A.x + y +x = 169 B.y + z = 168 C.(100-x):z = 32:64 D.(l00-x):(y-1) = 8:3
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】改革开放40年来,潍坊大地经济、文化蓬勃发展,各项民生取得长足进步。
(1)诸城纺织,织染五洲。如图为某品牌服装标签,该服装里料属于_____(填“天然”、“合成”)纤维,鉴别涤纶与羊毛的简单方法是_____。
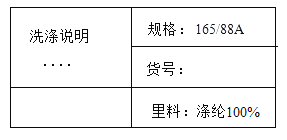
(2)寿光蔬菜,风光中外。从分子的角度看,能闻到果香的原因是_____。蔬莱在培育过程中要施加少量复合肥,下列属于复合肥的是_____(填序号)
A NH4Cl B NH4H2PO4 C CO(NH2)2 D K2SO4
(3)古城青州,历史璀璨。博物馆内斑驳铜绿的主要成分Cu2(OH)2CO3,由此可判断铜的生锈离不开O2、H2O和_____。“天下第一状元卷”历经百年不褪色的原因是_____。

(4)山水临胸,醉美沂山。沂山泉水甘冽,要鉴别泉水是硬水还是软水,需要用到_____,为了保护水资源,请写出一种防治水体污染的做法_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以甲为原料转化成丙的微观过程如下图。下列说法正确的是
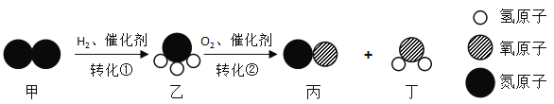
A.转化①中分子和原子的种类都发生改变
B.转化②中丙和丁的分子个数之比为1 :1
C.乙中氢元素的质量分数小于丁
D.转化①、②中氮元素的化合价都发生变化
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铁及其化合物在生活生产中应用非常广泛。
(一)铁材料的有关知识

(1)人类使用金属先后经历了“青铜”、“铁器”时代,直到近代才开始大量使用铝材料。这也反映出Cu、Fe、 Al三种金属的活动性由强到弱的顺序是_______________。
(2)磁铁矿是早期司南(如图)的材料,磁铁矿中所含铁的氧化物主要是________________。
(3)我国C919大型客机去年惊艳亮相,客机上大规模使用碳纤维复合材料、铝锂合金、铁钛合金、纳米陶瓷等先进材料,其中不涉及到的材料是_________(选填序号)。
A 合金
B 无机非金属材料
C 合成材料
D 复合材料
(4)铁矿石有赤铁矿、磁铁矿、黄铁矿(FeS2)等。工业上用黄铁矿制取硫酸而不用于炼铁,不用于炼铁原因是:①冶炼中产生SO2污染环境;②______________。
(二)制取碱式硫酸铁
碱式硫酸铁是-种废水处理剂,用硫酸厂的废渣(主要成分为铁的氧化物、少量FeS及SiO2)制备碱式硫酸铁晶体[Fe4(OH)2(SO4)5·6H2O]主要流程如下:

(1)废渣应研磨成粉末,目的是_____。
(2)“酸溶”过程中生成H2S气体的化学方程式为________
(3)过滤后洗涤,证明固体已洗净的方法是_______。
(4)“转化”发生反应的化学方程式为_______,该反应温度不宜过高的原因是________。
(三)碱式硫酸铁晶体的热分解实验
兴趣小组称取此晶体样品25.38g,在科研人员的指导下用下图装置进行热分解实验。
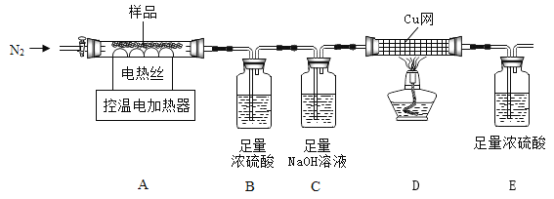
[查阅资料]①碱式硫酸铁晶体(相对分子质量为846)200°C完全分解生成Fe2O3、H2O和Fe2(SO4)3;
②Fe2(SO4)3在500°C完全分解为Fe2O3、SO2、SO3和O2;
③B装置中浓硫酸只能吸收SO3和H2O。.
(1)装配好实验装置后,先要_________。
(2)加热前后及过程中均通入N2,停止加热后继续通N2的目的是防止倒吸和______。
(3)控制不同的温度对A中固体加热,测得装置B、C和D中的质量变化如下表,测得剩余固体质量随温度的变化如图所示。

温度/C | 室温 | 220 | 520 |
B装置/g | 200.00 | 203.78 | 207.78 |
C装置/g | 200.00 | 200.00 | x |
D装置/g | 100.00 | 100.00 | 101.60 |
①如图中m1=____________。
②表格中x=_____________。
③将最终的剩余固体继续加热到更高的温度,发现固体减少0.32g后质量不再改变,写出此过程中发生反应的化学方程式____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】锂(Li)的元素信息图和氯(C1)元素的结构示意如图。下列描述正确的是( )
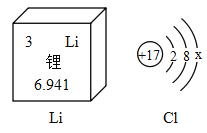
A.Li的相对原子质量为6.941g
B.Li、Cl元素形成的化合物为LiCl2
C.Cl-的结构:x=8,质子数=17
D.Li与O2反应生成氧化锂:![]()
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小丽来到实验室,看到实验桌上有一瓶敞口放置的氢氧化钠固体,于是她对这瓶氢氧化钠固体的成分展开探究。
[提出问题]这瓶氢氧化钠固体是否变质?
[猜想假设]猜想一:没有变质,固体物质是NaOH;
猜想二:部份变质,固体物质是NaOH和Na2CO3;
猜想三:完全变质,固体物质是_____。
[实验探究]为了探究固体成分,他们分别进行了如下实验:
(1)写出氢氧化钠变质的化学方程式_____。
(2)为了进一步确定这瓶固体的成分,丙同学设计了如下方案,请你完成下列实验报告:
实验方案 | 实验步骤 | 实验的现象 | 实验结论 |
实验方案Ⅰ | 取样于试管中 ,加入过量稀盐酸。 | 出现大量气泡 | 说明猜想一不成立 |
实验方案Ⅱ | ①取样于试管中,加水溶解,滴入酚酞溶液 | 溶液变红色 | 说明猜想二成立 |
②向①反应后溶液,滴入过量的Ca(OH)2溶液 | 产生白色沉淀,溶液显_____色 | ||
实验方案Ⅲ | ①取样于试管中,加水溶解,滴入酚酞溶液 | 溶液变红色 | 说明猜想三成立。 |
②向①反应后溶液,滴入过量的CaCl2溶液 | 产生_____,溶液由红色变成无色 |
[反思和评价]
1、在设计的实验方案中,其中有一种不合理的方案是_____。
2、在实验方案Ⅲ的探究中,能代替CaCl2溶液进行实验的是_____。 (填序号)
①稀硝酸;②Ba(OH)2溶液:③Ba(NO3)2溶液;④K2CO3溶液: ⑤Ca(NO3)2 溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】溶液与人们的生产生活密切相关。
(1)将少量下列物质分别放入水中,充分搅拌,可以得到溶液的是_____(填字母序号)。
A 高锰酸钾
B 汽油
C 面粉
D 白糖
(2)在盛有水的烧杯中加入以下某种物质,形成溶液过程中,温度有明显变化的是_____(填字母序号)。
A 烧碱
B 硝酸铵
C 氯化钠
D 浓硫酸
(3)如图为甲、乙两种固体物质的溶解度曲线。请回答下列问题
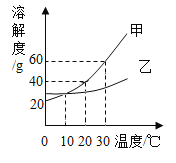
①甲中含少量的乙物质,提纯甲的方法是_____。
②若保持溶质的质量分数不变使乙的不饱和溶液变成饱和溶液采用的方法是_____。
③20℃时甲的溶解度为40g,这句话的含义是_____。
④30℃时,取等质量的甲乙两种物质的饱和溶液分别蒸发等量的水后,恢复到30℃.下列说法正确的是_____(填选项字母)。
A 恢复到原温度后,溶液中溶剂的质量:甲<乙
B 恢复到原温度后,析出晶体的质量:甲>乙
C 若再降温到10℃时,溶液的质量:甲<乙
D 若再降温到10℃时,溶液的溶质质量分数:甲=乙
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com