
【题目】某化学活动小组的同学做探究酸、碱、盐的某些化学性质的实验。如下图所示请回答下列问题:
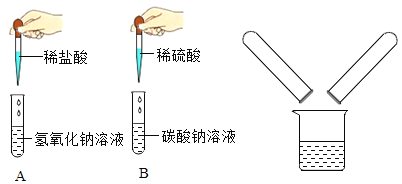
(1)何协同学进行的实验A中发生反应的化学方程式为________________________。
(2)实验结束后,他们将A、B试管中的废液分别倒在同一烧杯中,观察到溶液中有气泡冒出,则B试管中的溶质成分是___________________(填化学式),何协和岳娜两位同学想探究此烧杯中溶液溶质的成分,并进行如下探究活动:
(提出问题)烧杯中溶液的溶质成分是什么?
(猜想与假设)
何协同学猜想溶质成分是:NaCl、Na2SO4
岳娜同学猜想溶质成分是:NaCl、Na2SO4、Na2CO3
你的猜想是_______________(填化学式)
(实验验证)
(3)何协同学为了验证自己的猜想,取少量烧杯中的溶液于试管中,向其中滴加适量的氯化钡溶液,观察到无色溶液中产生白色沉淀,于是得出结论:自己的猜想正确,请对何协同学的推测及得出的结论进行评价_________________________。
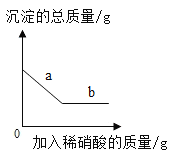
(4)岳娜同学将何协实验后的固液混合物过滤后,向滤渣中加入过量稀硝酸,并绘制出相关图像(如下图所示)。在滴加过量稀硝酸的过程中,下图中a发生反应的化学方程式为____________,通过对下图的分析,你认为烧杯中溶液的溶质成分是 ________________(填化学式)。
【答案】![]() Na2SO4、Na2CO3 NaCl、Na2SO4、HCl 不正确,因为硫酸钠、碳酸钠都能与氯化钡反应生成白色沉淀,其它猜想中的溶质成分都含硫酸钠,都能与氯化钡反应生成白色沉淀
Na2SO4、Na2CO3 NaCl、Na2SO4、HCl 不正确,因为硫酸钠、碳酸钠都能与氯化钡反应生成白色沉淀,其它猜想中的溶质成分都含硫酸钠,都能与氯化钡反应生成白色沉淀 ![]() NaCl、Na2SO4、Na2CO3
NaCl、Na2SO4、Na2CO3
【解析】
(1)氢氧化钠与稀盐酸反应生成氯化钠和水,该反应的化学方程式为:![]() ;
;
(2)A试管中氢氧化钠与稀盐酸反应生成氯化钠和水,氢氧化钠和稀盐酸可能恰好完全反应,也可能其中一个过量,B试管中碳酸钠与稀硫酸反应生成硫酸钠、二氧化碳和水,碳酸钠和稀硫酸可能恰好完全反应,也可能其中一个过量,将A、B试管中的废液分别倒在同一烧杯中,观察到溶液中有气泡冒出,说明A试管中盐酸过量,B试管中碳酸钠过量,因为碳酸钠与稀盐酸反应生成氯化钠、二氧化碳和水,故B试管中的溶质为Na2SO4、Na2CO3;
猜想与假设:氢氧化钠与稀盐酸反应生成氯化钠和水,碳酸钠和稀硫酸反应生成硫酸钠、二氧化碳和水,碳酸钠和稀盐酸反应生成氯化钠、二氧化碳和水,碳酸钠和稀盐酸可能恰好完全反应,这时溶质成分是氯化钠、硫酸钠,也可能碳酸钠过量,这时溶质成分是:碳酸钠、氯化钠、硫酸钠,还可能盐酸过量,这时溶质成分是:HCl、硫酸钠、氯化钠,故猜想是:NaCl、Na2SO4、HCl;
实验验证:(1)取少量烧杯中的溶液于试管中,向其中滴加适量的氯化钡溶液,观察到无色溶液中产生白色沉淀,不能证明何协同学猜想正确,因为硫酸钠、碳酸钠都能与氯化钡反应生成白色沉淀,其它猜想中的溶质成分都含硫酸钠,都能与氯化钡反应生成白色沉淀;
(4)由图可知,随着稀硝酸的加入,沉淀的质量逐渐减小,但是没有减小至零,说明沉淀部分溶于稀硝酸,该沉淀应是碳酸钡与硫酸钡的混合物,因为碳酸钡能与稀硝酸反应生成硝酸钡、二氧化碳和水,硫酸钡与稀硝酸不反应,碳酸钡与稀硝酸反应的化学方程式为:![]() ,沉淀是碳酸钡和硫酸钡的混合物,故溶质的成分一定含碳酸钠,由以上分析可知,烧杯中的溶质一定含氯化钠、硫酸钠,故烧杯中溶液的溶质成分是:NaCl、Na2SO4、Na2CO3。
,沉淀是碳酸钡和硫酸钡的混合物,故溶质的成分一定含碳酸钠,由以上分析可知,烧杯中的溶质一定含氯化钠、硫酸钠,故烧杯中溶液的溶质成分是:NaCl、Na2SO4、Na2CO3。


科目:初中化学 来源: 题型:
【题目】某种镀锡铜线表面锡的褪除及回收的工艺流程如图所示,请回答以下问题:
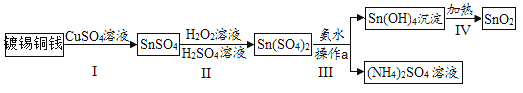
(1)Sn(OH)4中锡(Sn)的化合价为_________________。
(2)步骤Ⅲ中操作a的名称是_____________,该操作中用到的一种玻璃仪器的名称是______________。
(3)写出过程I中发生反应的化学方程式:_____________;过程IV发生的反应的基本反应类型是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】生铁用途十分广泛。工业上利用赤铁矿(主要成分是 Fe2O3,还含少量 SiO2 等杂质)冶炼生铁的过程如下:

回答下列问题:
(1)生铁属于_____材料(填“合成”或“金属”)。“高炉气体”中的_____(填化学式)会导致酸雨。
(2)“煅烧”时:
①生成 CO 的反应之一为 C + CO2 ![]() 2CO,该反应属于_____反应(填基本反应类型)。
2CO,该反应属于_____反应(填基本反应类型)。
②用化学方程式表示利用 CO 炼铁的原理_____。
③CaCO3 和 SiO2 固体在高温条件下发生反应,生成 CO2 气体和 CaSiO3,该反应的化学方程式为_____。
(3)生活中铁制品锈蚀的过程,实际上是 Fe 与空气中_____、_____等发生化学反应的过程。下列措施能防止铁制品锈蚀的是_____(填标号)。
A 涂油、喷漆 B 镀耐腐蚀的铬层
C 用盐水清洗 D .久置于酸性环境
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】探究铜生锈的条件
(提出猜想)根据铜锈的组成推测,铜生锈可能与CO2、H2O和O2有关。
(进行实验)实验小组同学取直径、长度均相同的铜丝,并打磨光亮。设计了如下图所示的5个实验并持续观察。
编号 | ① | ② | ③ | ④ | ⑤ |
实验 |
|
|
|
|
|
现象 | 无明显现象 | 无明显现象 | 铜丝表面有绿色物质 | 无明显现象 | 无明显现象 |
(解释与结论)
(1)实验中使用“经煮沸迅速冷却的蒸馏水”,其目的是_____。
(2)得出“铜生锈一定与O2有关”的结论,依据的两个实验是_____(填编号)。
(3)对比实验①和③,得出的结论是_____。
(4)为验证猜想,实验⑤广口瓶中除铜丝外,还应有的物质是_____。
(5)由上述实验可推知,铜生锈的条件是_____。
(反思与应用)
(6)结合上述实验,你对保存铜制品的建议是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】太阳能汽车利用太阳能来驱动,真正实现了零排放,有效地减少了对环境的污染,其产业的发展日益蓬勃。从某种意义上讲,太阳能汽车也是电动汽车的—种,所不同的是电动汽车的蓄电池靠工业电网充电,而太阳能汽车用的是太阳能电池。
(1)该太阳能汽车在白天给蓄电池充电的同时行驶,该行驶过程中首先____________能转化为化学能,然后转化为____________ 能,最终转化为机械能。
(2)该汽车车体主体材料是一种密度小、且抗腐蚀性好的一种合金,你认为下列材料中最合适的是___________( 填字母)
A 玻璃钢 B 锰钢 C 硬铝 D 生铁
(3)目前还有一种新能源汽车,氢燃料电池汽车,该种汽车的储氢材料是循环吸放氢过程中生成新的氢化物,其中一种为氢化铝锂(LiAlH4)的氢化物,在 125℃ 时分解为氢气和一种金属单质及氢化锂( LiH )。请你写出氢化铝锂分解反应的化学方程式______________。 反应前后铝元素的化合价分别为 ___________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】钼(元素符号是Mo)是一种重要的金属,用它制成的合金具有良好的机械性能,在工农业生产和国防上都有着广泛的应用。下图是利用钼矿石(主要成分为MoS2)制备金属钼的流程图,请据图回答下列问题:
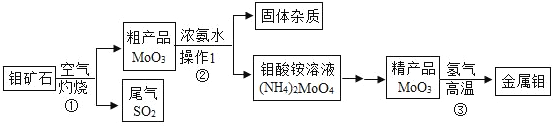
(1)反应①常将钼矿石粉碎,目的是_____。
(2)操作I的名称是_____,所需的玻璃仪器有烧杯、漏斗和_____。
(3)写出反应③的化学方程式:_____。
(4)尾气SO2会对空气造成污染,通常可以用浓氢氧化钠溶液吸收,请写出该反应的化学方程式:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知![]() 是初中化学常见的物质,B与人体血红蛋白结合会引起煤气中毒,C是赤铁矿的主要成分,H是胃酸的主要成分,它们之间的关系如下图所示。(图中“
是初中化学常见的物质,B与人体血红蛋白结合会引起煤气中毒,C是赤铁矿的主要成分,H是胃酸的主要成分,它们之间的关系如下图所示。(图中“![]() ”表示物质间转化关系,“—”两端物质间能相互反应。)请回答下列问题:
”表示物质间转化关系,“—”两端物质间能相互反应。)请回答下列问题:
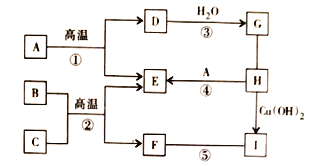
(1)写出I的化学式_____。
(2)判断⑤的反应类型_____。
(3)G的饱和溶液pH_____。
A 小于7 B 等于7 C 大于7 D 无法判断
(4)写出C与H反应的化学方程式_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】不同的交通工具使用着不同的材料,根据下列信息回答问题。
交通工具 |
共享单车 |
大飞机C919 |
共享汽车 |
用到的材料 | 轮胎:橡胶 | 机翼:铝锂合金 | 车身:钢 |
(1)上述材料中,含有的金属元素是_____,属于有机合成材料的是_____(写出一种即可)。
(2)大飞机C919大量使用铝锂合金,原因是_____。
(3)铝比铁活泼,为什么错的抗腐蚀性能更好?_____
(4)汽车车身表面的烤漆不仅美观,还能起到防锈的作用,防锈的原理是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】对下列化学用语中数字“2”含义的说法正确的是()
①2H ②2NH3 ③SO 2 ④![]() ⑤Mg2+ ⑥2OH- ⑦H2O
⑤Mg2+ ⑥2OH- ⑦H2O
A.表示离子个数的是⑤⑥
B.表示分子中原子个数的是③⑦
C.表示离子所带电荷数的是④⑤
D.表示分子个数的是①②
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com