
【题目】教材指出:H2O2分解的催化剂并非只有二氧化锰一种。实验证明FeCl3溶液、CuSO4溶液、红砖粉末都可以代替二氧化锰作H2O2分解的催化剂。针对上述结论,南开中学初三化学兴趣小组进行了如下探究:

探究一:比较同浓度FeCl3溶液、CuSO4溶液的催化效果
(1)请写出甲图左侧试管H2O2分解的化学方程式:_____。
(2)如用图甲装置进行实验,应观察同时滴入两种溶液后_____的现象。
(3)如用图乙装置进行实验,实验前检查该装置气密性良好。应测量生成等体积气体时所需的_____。
(4)已知过氧化氢分解是一个放热反应。用图乙装置进行实验时,细心的小丽同学观察到,锥形瓶中不再产生气泡后注射器的活塞向左移了一小段,请你推测出现该现象的原因_____。
探究二:证明红砖粉末可以作过氧化氢分解的催化剂
(5)小熊同学设计了如下实验:
她分别取2mL5%的H2O2溶液于两试管中,再称取0.5g红砖粉末倒入其中一支试管,发现加了红砖粉末的一支试管产生气泡速率较快。小熊认为,由此可证明红砖粉末可以作过氧化氢分解的催化剂。
小陈同学认为小熊的证明过程不够严密,需要补充下面两项实验。
实验结束后,小陈将试管内的剩余药品经①_____、洗涤、干燥后,称量得到固体质量仍为0.5g。
应补充的另一项实验为(填写实验操作)②_____。
【答案】2H2O2![]() 2H2O+O2↑ 产生气泡的快慢 时间 温度降低,装置内压强减小 过滤 将过滤、洗涤、干燥后的红砖粉放入一只盛有过氧化氢溶液的试管中,观察产生气泡的速率
2H2O+O2↑ 产生气泡的快慢 时间 温度降低,装置内压强减小 过滤 将过滤、洗涤、干燥后的红砖粉放入一只盛有过氧化氢溶液的试管中,观察产生气泡的速率
【解析】
探究一:
(1)甲图左侧试管H2O2分解的化学方程式:2H2O2![]() 2H2O+O2↑ ;
2H2O+O2↑ ;
(2)在过氧化氢分解的反应中,催化剂的作用是加快反应速率,如用图甲装置进行实验,应观察同时滴入两种溶液后产生气泡的快慢的现象,进而比较二者的催化效果;
(3)如用图乙装置进行实验,实验前检查该装置气密性良好。应测量生成等体积气体时所需的时间。时间越少,说明反应越快;
(4)已知过氧化氢分解是一个放热反应。用图乙装置进行实验时,细心的小丽同学观察到,锥形瓶中不再产生气泡后注射器的活塞向左移了一小段,出现该现象的原因反应中,由于反应放热,生成气体的温度高于室温,气体膨胀(压强增大),反应结束后,气体冷却,体积减小(压强变小);
探究二:
(5)红砖粉末是不溶固体,实验结束后,可用过滤的方法将红砖粉末分离出来,所以:将试管内的剩余药品经①过滤、洗涤、干燥后,称量得到固体质量仍为0.5g;
催化剂是能改变其他物质的反应速率而本身的质量和化学性质在反应前后都没有改变的物质,所以还应该证明红砖粉末在反应前后的化学性质没有改变。应补充的另一项实验为:将过滤、洗涤、干燥后的红砖粉放入一只盛有过氧化氢溶液的试管中,观察产生气泡的速率。如过氧化氢仍然快速分解,产生大量气泡,说明反应前后红砖粉末的化学性质没变。


科目:初中化学 来源: 题型:
【题目】小强同学在复习单质、氧化物、酸、碱、盐性质时,用铁、氧化铜、稀硫酸、氢氧化钙溶液、硫酸铜溶液五种物质,构建了如下图所示的知识网络图(图中短线“—”表示相连的两种物质能在一定条件下发生反应)。回答下列问题:
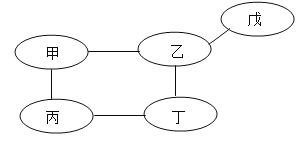
(1)戊物质是_________。
(2)丙物质属于______(填“酸”或“碱”或“盐”)。
(3)若丙和丁发生的反应属于置换反应,则此反应的化学方程式为:__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】推理是一种重要的思维方法,以下推理合理的是( )
A. 酸中一定含有氢元素,所以含有氢元素的物质一定是酸
B. 置换反应有单质生成,所以有单质生成的反应一定是置换反应
C. 中和反应有盐和水生成,因此有盐和水生成的反应一定是中和反应
D. 化学反应伴随能量变化,所以金属腐蚀过程中一定伴随能量变化
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】暖宝宝中的发热剂主要是铁粉、水和食盐等,在实验室发热剂能代替磷测定空气中氧气的体积含量(装置如图所示)。下列对此改进实验的叙述中,不正确的是
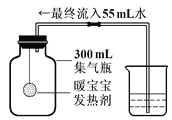
A.实验的原理是利用铁生锈消耗氧气
B.实验时,食盐可以加快铁粉的锈蚀
C.实验时,发热剂的多少不影响测量结果
D.实验测出空气中氧气的体积含量约是18.3%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人体无论缺碘元素(I)还是碘元素过量,都会引起甲状腺疾病。在食盐中按要求加入KIO3是我国政府给国人补碘的一种方法。请根据以下信息填空:
(1)碘元素在碘化物中化合价为﹣1,请你推测其最外层电子数为_____,它与元素周期表中第三周期的_____元素(填名称)具有相似的化学性质。
(2)加碘食盐最好在菜起锅前加入,据此推测,KIO3可能具有的化学性质是_____,如果加入过早,可能发生的一个化学反应的方程式为_____。
(3)小陈同学在硫化钠溶液中滴加碘(I2)的水溶液后发生置换反应产生淡黄色的固体单质。请结合(1)中知识信息写出该化学反应方程式_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】从不同角度认识物质,能帮助我们更全面了解物质世界。以氧气和二氧化碳为例,回答下列问题
(1)认识物质的组成和构成
①从宏观上看,氧气和二氧化碳都由________(填“元素”或“原子”或“分子”)组成。
②从微观上看,氧气和二氧化碳都由______(填“元素”或“原子”或“分子”)构成。
(2)认识物质的性质
①氧气的化学性质比较活泼。硫在氧气中燃烧观察到产生______火焰。
②在烧杯中有燃烧着的阶梯蜡烛,如图向烧杯中缓缓倾倒二氧化碳气体,观察到的现象是_____。
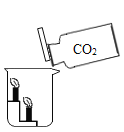
(3)认识物质的制法
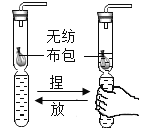
①某同学用软塑料瓶自制气体发生装置,通过捏放瓶身可随时控制反应发生和停止。若利用该装置制O2,反应的化学方程式为________。
③工业上常用液化空气制氧气,该过程发生______(填“物理变化”或“化学变化”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请根据下图中a、b、c三种物质的溶解度曲线,回答下列问题:
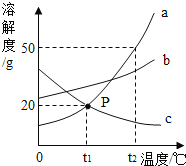
(1)P点的含义是__________。
(2)将t2℃时的a、b、c三种物质的饱和溶液降温到t1℃时,溶液中溶质的质量分数由大到小的顺序是______。
(3)适合采取冷却热饱和溶液析出晶体的是______。
(4)你还能获得哪些信息(只写一条)_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】生石灰常用作食品干燥剂,其包装袋上除了标明主要成分为生石灰外,还提醒人们注意:不可食用,不可浸水,不可开袋,儿童勿碰。
Ⅰ.小强同学通过探究发现,某食品包装袋中的生石灰干燥剂已经变质失效。他采用的探究方法是:取少量样品于试管中,加入少量水,用手触摸试管外壁,没有明显的放热现象。此实验中加入的水必须少量,理由是_____________。
Ⅱ.甲、乙同学想知道刚从食品袋中取出的生石灰干燥剂的成分,进行了如下探究:
(提出问题)生石灰干燥剂中含有哪些物质?
(查阅资料)工业上用高温煅烧石灰石的方法来制取生石灰。
(猜想与假设)猜想1:含有氧化钙、氢氧化钙
猜想2:含有氧化钙、碳酸钙
猜想3:含有氧化钙、氢氧化钙、碳酸钙
(活动与探究)甲、乙同学为了验证猜想,进行了如下实验:
甲同学实验:取少量样品于试管中,加入适量水充分反应后,再滴加几滴无色酚酞溶液,可观察到溶液呈红色。
乙同学实验:取少量样品于试管中,加入足量的稀盐酸,有无色无味的气体产生,该气体能使澄清的石灰水变浑浊。
(结论与反思)
(1)猜想_____错误(填“1”或“2”或“3”)。
(2)甲同学实验中,溶液呈红色的原因是__________。
(3)乙同学实验中产生的气体的是__________(填写化学式)。
(4)乙同学认为甲同学的实验是多余的,因为____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氢氧化钠如果保存不当容易吸收空气中的二氧化碳而变质[NaOH(Na2CO3)]。某化学课外活动小组的同学,为了测定实验室因部分变质的氢氧化钠中碳酸钠的质量分数,设计了如图所示的装置(图中铁架台已经略去),实验在27℃、101kPa下进行。
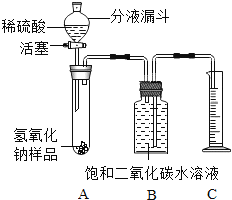
实验步骤如下:
①按图连接好装置;
②用天平准确称取氢氧化钠样品mg,放入A中试管内,向B中集气瓶内倒入饱和二氧化碳水溶液至瓶颈处;
③向分液漏斗中倒入稀硫酸,打开活塞,让稀硫酸滴入试管中至过量,关闭活塞。反应结束后,量筒中收集到饱和二氧化碳水溶液VmL;
④计算氢氧化钠样品中碳酸钠的质量分数。
请回答下列问题:
(1)氢氧化钠发生变质的化学方程式:________。
(2)在实验步骤①和②之间,还缺少一实验步骤,该实验步骤是_______。
(3)B中集气瓶盛装的饱和二氧化碳水溶液不能用水代替,其原因是_______。
(4)叙述检验氢氧化钠部分变质的方法:
实验步骤 | 实验现象 | 实验结论 |
①取样,溶于水,滴加过量的_______ | 产生白色沉淀 | 氢氧化钠部分变质 |
②静置,向上层清液中滴加________ | _____ |
(5)取10g变质的氢氧化钠于烧杯中,其中碳元素的质量分数为6%,向烧杯中加入100g一定质量分数的稀盐酸(足量),则反应结束后烧杯内物质的总质量是____g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com