

| A.步骤②中发生化合反应与置换反应 |
| B.“滤液1”中一定含FeCl2,可能含CuCl2 |
| C.步骤④反应为:2M+2FeCl2+ H2O2=2FeCl3+2H2O,M是HCl |
| D.若滤渣也为m1g,则废液中FeCl3与CuCl2的质量比为65∶54 |
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源:不详 题型:单选题
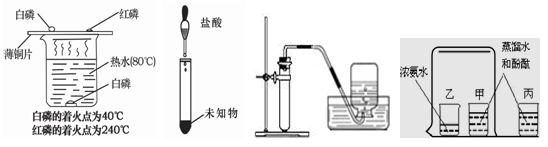
| A.①验证可燃物燃烧的条件 |
| B.②检验碳酸根离子的存在 |
| C.③实验室用过氧化氢溶液与二氧化锰制取氧气 |
| D.④探究分子在不断地运动 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
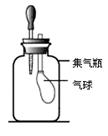
| 实验步骤 | 实验现象 | 实验结论 |
| 挤压滴管橡胶胶帽,使氢氧化钠溶液滴入集气瓶中。 | 气球逐渐变大 | 二氧化碳和氢氧化钠溶液确实发生了化学反应 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题

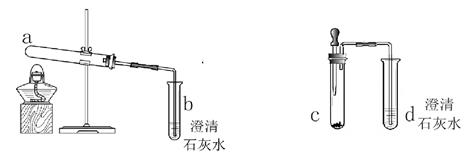
| 序号 | 实验方案 | 实验现象 | 实验结论 |
| Ⅰ | 在装置1的a试管中放入小苏打,加热 | a试管口内壁有无色液滴,_________。 | b试管中发生反应的化学方程式为______。 猜想1正确 |
| Ⅱ | 在装置1的a试管中放入酒石酸氢钾,加热 | a试管口内壁有无色液滴,石灰水不变浑浊 | ______________ |
| Ⅲ | 在装置2的c试管中放入小苏打和酒石酸氢钾的混合物,滴加________。 | , 石灰水变浑浊 | 猜想3正确 |
 Na2CO3 + H2O + CO2↑,根据以上实验结论和所学知识,小明对探究问题又提出了第4个猜想,并在以上实验的基础上,利用装置2完成实验验证,其实验方案为____。
Na2CO3 + H2O + CO2↑,根据以上实验结论和所学知识,小明对探究问题又提出了第4个猜想,并在以上实验的基础上,利用装置2完成实验验证,其实验方案为____。查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
| 实验序号 | 实验操作 | 实验现象 | 解释及结论 |
| 实验I | 用砂纸擦去镁条表面氧化膜,将其放入盛有适量饱和碳酸氢钠溶液的试管中 | 迅速反应,产生大量气泡和白色不溶物 |  |
| 实验Ⅱ | 将实验I中收集到的气体点燃,并在火焰上方罩一干、冷的小烧杯 | 气体安静燃烧、产生淡蓝色火焰,烧杯内壁有水雾出现。 | 该气体是 ,燃烧的化学方程式为 。 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
| 编号 | 维生素C溶液的处理方法 | 使40毫升高锰酸钾(KMnO4)溶液褪色的滴数 |
| 1 | 放置于室内暗处0.5小时 | 15 |
| 2 | 阳光强烈直射5小时后,放置于室内暗处0.5小时 | 22 |
| 3 | 煮沸10分钟后,放置于室内暗处0.5小时 | 21 |
查看答案和解析>>
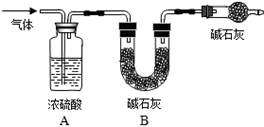
科目:初中化学 来源:不详 题型:实验题

| 装置 | B | C |
| 反应前质量 | 85.3g | 284.2g |
| 反应后质量 | 82.1g | 287.8g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com