
【题目】砷化镓(GaAs)是一种“LED”绿色节能光源材料,镓元素的相关信息如图。下列有关镓的说法正确的是

A. 属于非金属元素 B. 原子的核内质子数是31
C. 原子的核内中子数是31 D. 1个镓原子的质量为69.72g
【答案】B
【解析】A、根据元素周期表中的一格可知,中间的汉字表示元素名称,该元素的名称是镓,属于金属元素,错误;B、根据元素周期表中的一格可知,左上角的数字为31,表示原子序数为31;根据原子序数=核电荷数=质子数,则该元素的原子核内质子数为31,正确;C、根据元素周期表中的一格可知,左上角的数字为31,表示原子序数为31;根据原子序数=核电荷数=质子数=核外电子数,则该元素的原子核内质子数和核外电子数均为31,而不是中子数为31,错误;D、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为69.72,而不是1个镓原子的质量为69.72g,错误。故选B。


科目:初中化学 来源: 题型:
【题目】t1 ℃时,将等质量的硝酸钾和氯化钾分别加入到各盛有100 g水的两个烧杯中,充分搅拌后现象如图1所示,硝酸钾和氯化钾的溶解度曲线如图2所示。
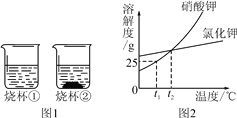
(1)烧杯②种的上层清液是否达到饱和状态?____(填“是”“否”或“无法判断”);
(2)烧杯①中溶解的溶质是____(写名称或化学式);
(3)将t1 ℃时50 g硝酸钾的饱和溶液稀释成10%的溶液,需加水____g;
(4)关于图1中烧杯内的物质,下列说法正确的是____。
A.烧杯①内溶液中溶质的质量分数>烧杯②内上层清液中溶质的质量分数
B.蒸发一定量的水,两烧杯中都一定有固体析出
C.将两个烧杯中的溶液混合,充分搅拌后,烧杯中一定还有剩余固体
D.将温度升高到t2 ℃,两烧杯内溶液中溶质的质量分数相等(不考虑水的蒸发)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是探究铁锈蚀条件的装置![]() 调节L端与R端的液面高度一致,塞紧木塞,一周后观察
调节L端与R端的液面高度一致,塞紧木塞,一周后观察![]() 下列推断正确的是
下列推断正确的是![]()
![]()
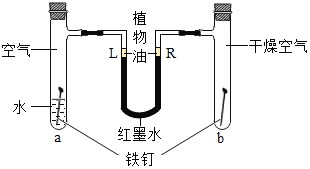
A. a,b管中铁钉都会生锈
B. 该实验证明铁锈蚀与空气无关
C. L端与R端液面高度最终不能保持一致
D. 将a管中的水改为食盐水能加快铁的锈蚀,L端与R端的液面高度差一定会加大
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】二氧化铈(CeO2)是一种重要的稀土氧化物。平板电视显示屏生产过程中产生大量的废玻璃粉末(含SiO2、Fe2O3、CeO2等物质),某课题组以此粉末为原料进行资源回收,其工艺流程如下:
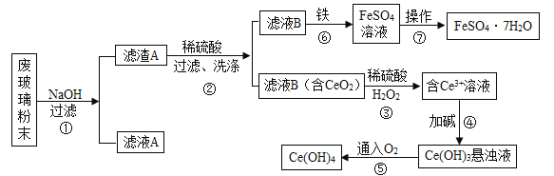
(1)写出第②步反应的化学方程式__________。
(2)洗涤滤渣B的目的是为了除去_____(填离子符号)。
(3)第③步反应中Ce元素由_______价变成+3价。
(4)第⑦步操作是把FeSO4溶液经蒸发浓缩、________、过滤、洗涤、干燥等步骤得到绿矾FeSO4·7H2O。
(5)若第④步加的碱为NaOH溶液,写出生成Ce(OH)3的反应方程式_________。
(6)请补充完整第⑤步反应的化学方程式:4Ce(OH)3+O2+_____=4Ce(OH)4。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】汽车尾气催化转换器可减少有害气体的排放,其中某一反应(在催化剂作用下)过程的微观变化如图所示,请回答下列问题。
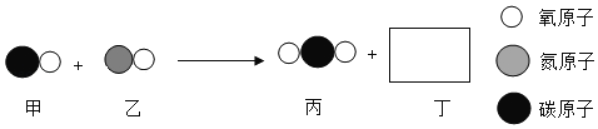
(1)结合上图分析,化学变化中最小的粒子是_____;
(2)丙微粒中碳元素的化合价为_____;
(3)已知丁是一种单质,则丁的化学式是_____;
(4)该反应的化学方程式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氯化亚铜(CuCl)广泛应用于冶金、电镀、医药等行业。已知CuCl难溶于水和乙醇,在潮湿空气中易变质。CuCl的制备流程如下:
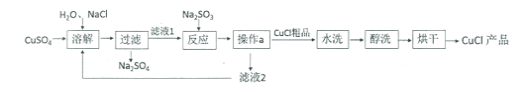
(1)“滤液1”中除了Na+、SO42-外,还存在较多的离子是______、_______(写离子符号)
(2)“反应”中发生的化学变化是2CuCl2+Na2SO3=2CuCl↓+2NaCl+SO3,产生的SO3迅速与水化合生成一种酸,该反应的化学方程式为___________。
(3)“操作a”的名称是__________。本流程中可以循环利用的物质(水除外)是__________。(写化学式)
(4)可用“水洗”的原因是__________,“醇洗”的目的是______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了研究质量守恒定律,某兴趣小组设计了如图1白磷燃烧前后质量测定”的实验,请分折有关问题。
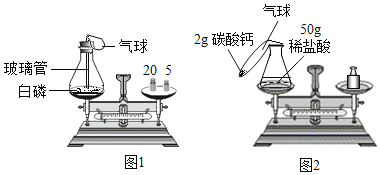
(1)装置:锥形瓶的底部铺有一层细沙,其作用是_____。
(2)燃烧前称量,锥形瓶的总质量为27.6g,则如图托盘天平中游码读数为_____g。
(3)白磷燃烧:白磷燃烧过程中看到的现象是_____,气球的变化是_____。
(4)燃烧后称量:发现托盘天平指针偏向右边,造成这种现象的原因可能是_____(只写一条)。
(5)反思:白磷燃烧_____(填“遵守”或“不遵守”)质量守恒定律,理由是_____。
考虑到白磷的危险性,老师改进了本实验,确定以“稀盐酸与碳酸钙反应“为研究对象,设计的实验装置如图所示。(方程式:CaCO3+2HCl=CaCl2+H2O+CO2↑)
(6)实验步骤如下:
①按如图2方式放好仪器,使天平平衡。
②将碳酸钙粉末全部倒入锥形瓶中,观察到锥形瓶中液体里出现的现象是_____。
③当反应结束时,气球已经完全鼓起,小明发现天平的指针已经向右偏了。他感到困惑:其他操作和仪器装置均正常。实验现象与数据与预测结果不符的原因是_____。
(7)本实验需要称量什么?_____,称量几次?_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】低钠盐适合患有高血压、肾病、心脏病的患者服用,苹果酸钠盐(C4H5O5Na)是低钠盐的一种.请回答:

(1)每个苹果酸钠盐分子中共有_______个原子.
(2)苹果酸钠盐碳、氧元素质量比为_______.
(3)若某病人每天食用 4.68g 苹果酸钠盐,则该病人每天最多吸收_______g 钠元素.
(4)药店销售一种苹果酸钠盐口服液,治疗效果非常好.该口服液的说明书如图,若某 病人每天食用 4.68g 苹果酸钠盐,试计算该口服液中苹果酸钠盐的质量分数_______.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com