烧碱(NaOH)是一种重要的化工原料,广泛应用于肥皂、造纸等工业.下面有一些关于烧碱的问题,请按要求解答:
(1)烧碱在工业上通常用电解饱和NaCl水溶液的方法制取,产物除烧碱外,还有H2和Cl2,请写出电解饱和NaCl水溶液的化学方程式______ 2NaOH+H2↑+Cl2↑
【答案】
分析:电解饱和食盐水能生成氢氧化钠、氢气和氯气,根据生成沉淀的质量可以确定混合物的组成,氢氧化钠和盐酸反应生成氯化钠和水,无明显现象,可以通过指示剂加以证明之间发生了化学反应,根据溶质质量分数的计算可以确定所需的配制方案,配制溶液时需要称量药品的质量和体积,导致溶质偏少或溶剂偏多的错误操作将会导致配制的结果偏低.
解答:解:(1)电解饱和食盐水能生成氢氧化钠、氢气和氯气,所以本题答案为:2NaCl+2H
2O

2NaOH+H
2↑+Cl
2↑;
(2)设生成10g沉淀需要碳酸钠的质量为x,
Na
2CO
3+Ca(OH)
2=CaCO
3↓+2NaOH
106 100
x 10g
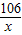
=

x=10.6g
所以含有氢氧化钠的质量为:14.6g-10.6g=4g,
所以本题答案为:D;
(3)可以借助指示剂证明氢氧化钠和盐酸发生了化学反应,,所以本题答案为:向滴有酚酞试液的氢氧化钠溶液中,逐滴加入盐酸,可以发现红色褪去;
(4)据题意可以发现,60g 10%的NaOH溶液需要氢氧化钠固体6g和水54g,配制方案中只要符合这个量就可以,40g5%的氢氧化钠溶液含有氢氧化钠2g,水38g,所以需要4g氢氧化钠固体和16g水,也可以加入20g20%的氢氧化钠溶液来配制,所以本题答案为:
| 序号 | 配制方案 |
| | |
| 方案1 | 40g5%的溶液,4g固体,16g水 |
| 方案2 | 20g20%的溶液和40g5%的溶液 |
(5)氢氧化钠具有腐蚀性,要放在玻璃器皿中称量,操作中导致溶质质量分数偏低的原因是水多固体少,砝码和氢氧化钠固体放错盘,会使固体质量减少,烧杯用水洗涤后未干燥就使用,导致水多,平视量筒凹液面最低处读数为50mL,则水的量正好,溶解时有少量水溅出导致水减少,所以本题答案为:①氢氧化钠直接放在纸上称量②AB.
点评:本题考查了氢氧化钠的制取依据有关的性质,溶液的配制和溶质质量分数的有关计算,完成此题,可以依据已有的知识及溶液配制的知识进行.

 2NaOH+H2↑+Cl2↑;
2NaOH+H2↑+Cl2↑;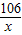 =
=




