烧碱(NaOH)是一种重要的化工原料,广泛
应用于肥皂、造纸等工业.下面有一些关于烧碱的问题,请按要求解答:
(1)烧碱在工业上通常用电解饱和NaCl水溶液的方法制取,产物除烧碱外,还有H2和Cl2,请写出电解饱和NaCl水溶液的化学方程式______ 2NaOH+H2↑+Cl2↑
【答案】
分析:(1)根据题目对反应的描述,确定反应的反应物与生成物,完成反应的化学方程式;
(2)根据碳酸钠与氢氧化钙生成碳酸钙沉淀和氢氧化钠的化学方程式,由生成沉淀碳酸钙的质量可计算14.6g固体中含有碳酸钠的质量,固体质量与碳酸钠质量差即为氢氧化钠的质量;
(3)借助酸碱指示剂遇酸碱呈现不同颜色的特点,可把滴有酚酞而呈红色的氢氧化钠溶液滴入稀盐酸中,通过红色消失以证实反应的发生;
(4)根据配制60g 10%的NaOH溶液,只需要取足氢氧化钠60g×10%=6g,然后加入适量水使得溶液质量达到60g即可完成所需要溶液的配制.
解答:解:(1)电解饱和NaCl水溶液的方法制取烧碱,还可以产生H
2和Cl
2,因此反应的化学方程式为2NaCl+2H
2O
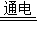
2NaOH+H
2↑+Cl
2↑;
(2)设样品中碳酸钠的质量为x
Ca(OH)
2+Na
2CO
3═CaCO
3↓+2NaOH
106 100
x 10g
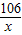
=
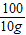
x=10.6g
样品中NaOH的质量=14.6g-10.6g=4g
故选D;
(3)滴有氢氧化钠的溶液呈红色,把这种呈红色的溶液滴入稀盐酸中,可观察到滴入的溶液红色立即消失,可说明氢氧化钠与盐酸发生了反应;
(4)配制60g 10%的NaOH溶液,需要氢氧化钠60g×10%=6g,因此可采取取30g 20%的NaOH溶液加入60g-30g=30g水、取40g 5%的NaOH溶液再加入6g-40g×5%=4g氢氧化钠固体和60g-40g-4g=16g水进行混合,都可得到60g 10%的NaOH溶液;
故答案为:
(1)2NaCl+2H
2O
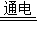
2NaOH+H
2↑+Cl
2↑
(2)D
(3)把加有酚酞的氢氧化钠溶液滴入稀盐酸,红色消失;(合理答案均可)
(4)
| 方案1 | 30g20%的NaOH溶液和30g水 |
| 方案2 | 40g 5%的NaOH溶液、4gNaOH固体和16g水 |
(合理答案均可)
点评:本题通过氢氧化钠这一物质综合考查了化学方程式的书写、化学方程式的计算、实验的设计及配制一定质量分数的溶液,在解答时要耐心思考.

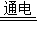 2NaOH+H2↑+Cl2↑;
2NaOH+H2↑+Cl2↑;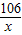 =
=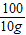 x=10.6g
x=10.6g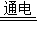 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑

 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案

