
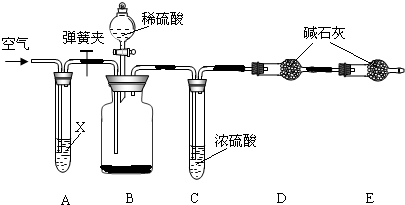
 实验室常用加热(85℃)NH4Cl和NaNO2两种饱和溶液的方法制取N2,如图是实验室用这种方法制N2,并测定生成N2体积的装置(部分装置略去),请回答相关问题:
实验室常用加热(85℃)NH4Cl和NaNO2两种饱和溶液的方法制取N2,如图是实验室用这种方法制N2,并测定生成N2体积的装置(部分装置略去),请回答相关问题:
| ||
| 37g |
| 100g+37g |
| ||
| 53.5 |
| 28 |
| 0.21g |
| x |
| 0.11g |
| 1.25g?L-1 |
| ||


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解

查看答案和解析>>
科目:初中化学 来源:2013-2014学年江苏省扬州市江都区九年级上期末考试化学试卷(解析版) 题型:探究题
实验室常用加热(85℃)NH4Cl和NaNO2两种饱和溶液的方法制取N2,下图是实验室用这种方法制N2,并测定生成N2体积的装置(部分装置略去),请回答相关问题:
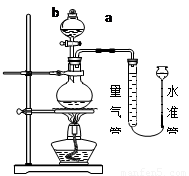
【查阅资料】:
1、NH4Cl和NaNO2反应生成NaCl、H2O及N2,并放出大量热量;
2、20℃时,NH4Cl的溶解度约为37g;
3、N2难溶于水,实验条件下,密度为1.25g·L—1。
【实验步骤】:
① ;
②20℃时,取0.78g饱和NH4Cl溶液放入烧瓶,连接装置;
③调节水准管,使其与量气管中液面相平,记录量气管中水面读数为12mL;
④打开分液漏斗活塞,逐滴滴入饱和NaNO2溶液,加热至反应发生,移走酒精灯;
⑤烧瓶中不再产生气泡时,关闭活塞;
⑥待冷却至室温,调节两边液面高度相平,记录量气管中水面读数为V mL;
⑦处理剩余药品,整理实验台。
【实验分析及数据处理】:
(1)写出装置中仪器的名称:a、 ;b、 ;
(2)反应的化学方程式为: ;
(3)完善实验步骤中的所缺部分:① ;
(4)步骤④中,移走酒精灯的目的是 ;
(5)NH4Cl是一种 (填“易溶”、“可溶”、“微溶”、“难溶”)物质。20℃时,其饱和溶液中溶质质量分数为 。根据实验数据计算,生成氮气约为多少毫升?(3分,计算过程中,中间数据保留2位小数,最终结果为整数;相对分子质量:Mr-NH4Cl:53.5、Mr-N2:28)
(6)根据计算结果,步骤⑥中V的数值为 ;
(7)实验中,实际测得氮气的体积偏大,可能原因是 。
A.实验中加入饱和NaNO2溶液的体积也被作为生成N2的体积
B.装置漏气
查看答案和解析>>
科目:初中化学 来源:2011年第二十一届“天原杯”全国初中学生化学素质和实验能力竞赛(广东赛区)初赛试卷(解析版) 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com