
【题目】自来水消毒过程中通常会发生如下化学反应,其反应的微观过程可用图表示:

(![]() 表示氯原子,
表示氯原子,![]() 表示氧原子,
表示氧原子,![]() 表示氢原子)
表示氢原子)
(1)请写出甲图所示反应的化学方程式 ;
(2)乙图所示反应的基本反应类型为 ;
(3)上述物质中,属于单质的有 (填化学式);
(4)D物质中氯元素的化合价为 ;
(5)以甲图为例分析,你能总结出的一条结论是 .
【答案】(1)H2O+Cl2═HCl+HCl(2)分解反应.(3)Cl2、O2(4)+1价 (5)化学反应前后原子的种类、数目不变(或化学反应前后元素的种类不变、化学反应的本质是原子的重新组合等合理说法均给分).
【解析】
试题(1)由图中可知,水和氯气反应生成次氯酸和盐酸,反应的化学方程式为:H2O+Cl2═HCl+HCl(2)反应物是一种,生成物是两种,属于分解反应.故填:分解反应.(3)氯气和氧气都是由同种元素组成的纯净物,属于单质.故填:Cl2、O2(4)氢元素是+1价,氧元素是﹣2价,可以求出氯元素的化合价是+1价.故填:+1价 (5)在化学变化中,原子是最小的微粒.故填:化学反应前后原子的种类、数目不变(或化学反应前后元素的种类不变、化学反应的本质是原子的重新组合等合理说法均给分).


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】碲(Te)被誉为“现代工业、国防与尖端技术的维生素,创造人间奇迹的桥梁”。实验室模拟提取碲的一个实验是:取某含碲溶液于烧瓶中,加入适量NaCl,加热到一定温度,持续通入SO2,待反应一段时间,过滤得到粗碲。
(1)反应的总化学方程式为: ![]() ,则X为______(填化学式);
,则X为______(填化学式);
(2)为探究获得较高粗碲沉淀率的反应条件,某研究小组在控制NaCl浓度和SO2流量不变的条件下,进行下述对比试验,数据如下:
实验 | 温度/℃ | 反应时间/h | 粗碲沉淀率/% |
a | 65 | 3.0 | 65.0 |
b | 80 | 3.0 | 98.9 |
c | 80 | 2.0 | 98.9 |
d | 90 | 2.0 | 97.0 |
①该小组研究的反应条件是______和______;
②实验a和b 的目的是______;
③为了提升设备利用效率和节约能源,可进一步优化反应条件测定粗碲沉淀率。若再设计对比实验,选择的反应条件还可以是______(填序号)。
A 80℃,1.5h B 80℃,2.5h C 70℃,2.0h D 95℃, 2.0h
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在相同质量、等质量分数的三份稀盐酸中,分别加入①MgO,②Mg(OH)2,③MgCO3三种物质,均能恰好完全反应,分别得到三份无色澄清溶液.则所得溶液中MgCl2的质量分数大小关系的比较,下列正确的是( )
A. ①=③>②B. ①>②>③C. ③>②>①D. ①=②=③
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人类发展的历史进程中人们不断研制出各种不同的用具,制造用具的材料也在不断地发生变化,金属制品因其美观、耐用、轻便易成型而被人们广泛利用,请根据所学知识及生活知识参与有关金属制品探究。
(一)以下工具的制作过程中没有发生化学变化的是_____。
A原始人制作石刀 B冶炼青铜 C炼铁
(二)请将以下金属材料的冶炼按年代的先后顺序排序_____(填序号)。
A铁 B青铜 C铝
从以上顺序可以看出,金属制品的出现顺序与_____有关,那么金属钾的制得应排在_____(填序号)之后。
(三)铜器是生活中常见物品,铜器保存不善,表面会生成一层绿色铜锈Cu2(OH) 2CO3.铜生锈的条件除了水和氧气外还需要_____(写化学式)。
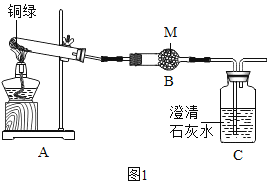
(四)为了探究碱式碳酸铜的化学性质和组成,该小组同学取少量铜绿(假设杂质不参与反应)按如图装置进行实验:
已知:I.铜绿的主要成分是碱式碳酸铜。
Ⅱ.铜器因所处环境不同,生成的铜绿中可能还含有CuSO4和CuCl2。
Ⅲ.硫酸铜、氯化铜的化学性质稳定,酒精灯加热条件下不分解。
(1)M药品的名称是_____。
(2)写出Cu2(OH)2CO3分解的化学方程式_____。
(3)实验过程中,发现A中绿色固体逐渐变为黑色,B中固体变蓝色,C中现象为_____,此处发生反应的化学方程式为_____。
(4)为了验证铜绿中是否有CuSO4和CuCl2,该小组同学进行了如下实验,请补充完成下列实验报告:
步骤 | 操作 | 现象及结论 |
① | 取少量铜绿溶于足量稀硝酸中,并将溶液分成甲、乙两份 | 产生气泡 |
② | 向甲中滴加硝酸钡溶液 | 若观察到_____,则铜绿中含有CuSO4 |
③ | 向乙中加入过量的硝酸钡溶液,振荡、静置,取上层清液于试管中,再滴加_____。 | 若观察到产生白色沉淀,则铜绿中含有CuCl2 |
(五)已知:
①铜矿矿石中含有Cu2(OH)2CO3及含铁元素的杂质;
②黄铵铁矾的化学式为 (NH4)xFey(SO4)m(OH)n,其中铁为+3价。
③在化学中Fe3O4可以表示为FeOFe2O3
某兴趣小组利用该铜矿石制黄铵铁矾的流程如图2:
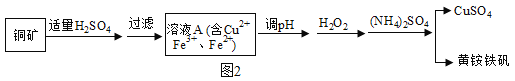
(1)以氧化物的形式表示Cu2(OH)2CO3的组成为_____,111gCu2 (OH)2CO3与稀H2SO4反应时消耗H2SO4的质量为_____g。
(2)该小组为测定黄铵铁矾的组成,进行了如下实验:
a.称取mg样品,加盐酸完全溶解后,将所得溶液分为两等份;
b.向一份中加入足量NaOH溶液并加热,收集到0.0425g的气体(假设气体全部逸出)。将所得沉淀过滤、洗涤、灼烧至恒重,得到红棕色粉末0.600g。
c.向另一份中加足量BaCl2溶液充分反应后,过滤、洗涤、干燥得沉淀1.165g。
①黄铵铁矾中NH4+与SO42﹣的个数比为_____。
②通过计算确定黄铵铁矾的化学式_____。(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】溶液与人们的生产、生活密切相关。
图1为甲、乙两种固体物质的溶解度曲线。
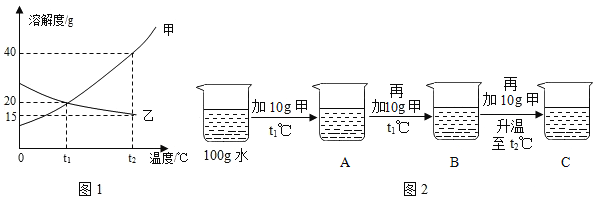
(1)溶解度随温度升高而增大的物质是_____ (填“甲”或“乙”)。
(2)某同学按图2所示进行实验,得到相应温度下的A、B、C三种溶液,在A、B、C三种溶液中属于饱和溶液的是_____(填字母)。 向C中再加入25g 甲,充分搅拌,恢复到t2℃时,所得溶液中溶质的质量分数为_____(结果精确到0.1%)。
(3)将t2℃时的甲、乙两种物质的饱和溶液降温至t1℃,所得溶液中溶质的质量分数:甲_____乙(填“<”“=”或“>”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列有关化学用语表示正确的是( )
A. 氯离子结构示意图: ![]()
B. 2个氢原子:2H+
C. 酒精的化学式:C2H4O2
D. 氧化钠中氧元素显-2价: ![]()
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氯化亚铜(CuCl)是一种难溶于水和乙醇,在潮湿空气中易变质,广泛应用于冶金、电镀、医药等行业的原料。CuCl的制备流程如下:
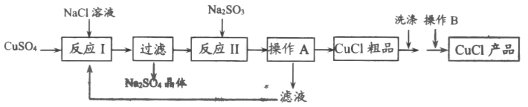
(1)“反应Ⅰ”中发生的化学方程式为_______。
(2)反应Ⅰ“过滤”后所得的滤液中,除了Cu2+, Na+, Cl-外,还存在较多的离子是_______(写离子符号)
(3)“反应Ⅱ”中发生的化学变化是2CuCl2+Na2SO3 +H2O =2CuCl↓+2NaCl+ H2SO4,其中化合价发生改变的元素有_______;反应过程中溶液的pH_______(选填“变大”、“变小”或“不变”)。
(4)本流程中可以循环利用的物质是_______。(写名称)
(5)在洗涤过程中用乙醇而不用水洗涤的原因是_______。
(6)“操作B”的名称是_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“三效催化转换器”可将汽车尾气中有毒气体处理为无毒气体.下图为该反应的微观示意图,其中不同的球代表不同种原子.下列说法中,不正确的是( )
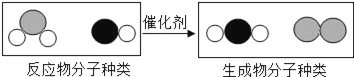
A. 分子在化学变化中可分
B. 此反应一定有单质生成
C. 原子在化学变化中不可分
D. 该反应属于置换反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下图装置,回答下列有关问题:
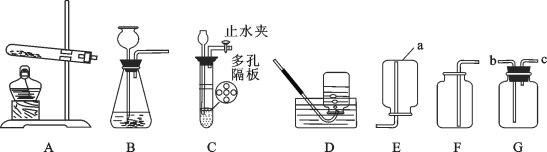
(1)装置图中仪器a的名称为_______。
(2)实验室用过氧化氢和二氧化锰制取氧气的化学方程式为_______,可选用的发生装置为_________,收集装置是____________。(填标号)
(3)若用G装置采用排空气法收集氢气,氢气应从_____________进。(选“b”或“c”)
(4)制取二氧化碳最好选用的发生装置是____________,该装置与另一个可选用的装置相比,其主要优点是_______。实验室制取二氧化碳的化学方程式为________,检验二氧化碳的原理为_________(用化学方程式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com