
����Ŀ�����չ����ʷ���������Dz������Ƴ����ֲ�ͬ���þߣ������þߵIJ���Ҳ�ڲ��ϵط����仯��������Ʒ�������ۡ����á�����׳��Ͷ������ǹ㷺���ã��������ѧ֪ʶ������֪ʶ�����йؽ�����Ʒ̽����
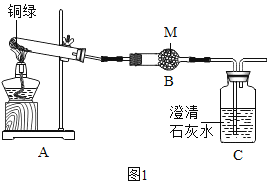
��һ�����¹��ߵ�����������û�з�����ѧ�仯����_____��
Aԭʼ������ʯ�� Bұ����ͭ C����
�������뽫���½������ϵ�ұ����������Ⱥ�˳������_____������ţ���
A�� B��ͭ C��
������˳����Կ�����������Ʒ�ij���˳����_____�йأ���ô�����ص��Ƶ�Ӧ����_____������ţ�֮��
������ͭ���������г�����Ʒ��ͭ�����治�ƣ����������һ����ɫͭ��Cu2��OH�� 2CO3��ͭ�������������ˮ���������Ҫ_____��д��ѧʽ����
���ģ�Ϊ��̽����ʽ̼��ͭ�Ļ�ѧ���ʺ���ɣ���С��ͬѧȡ����ͭ�̣��������ʲ����뷴Ӧ������ͼװ�ý���ʵ�飺
��֪��I��ͭ�̵���Ҫ�ɷ��Ǽ�ʽ̼��ͭ��
��ͭ��������������ͬ�����ɵ�ͭ���п��ܻ�����CuSO4��CuCl2��
������ͭ���Ȼ�ͭ�Ļ�ѧ�����ȶ����ƾ��Ƽ��������²��ֽ⡣
��1��MҩƷ��������_____��
��2��д��Cu2��OH��2CO3�ֽ�Ļ�ѧ����ʽ_____��
��3��ʵ������У�����A����ɫ������Ϊ��ɫ��B�й������ɫ��C������Ϊ_____���˴�������Ӧ�Ļ�ѧ����ʽΪ_____��
��4��Ϊ����֤ͭ�����Ƿ���CuSO4��CuCl2����С��ͬѧ����������ʵ�飬�벹���������ʵ�鱨�棺
���� | ���� | ������ |
�� | ȡ����ͭ����������ϡ�����У�������Һ�ֳɼס������� | �������� |
�� | ����еμ����ᱵ��Һ | ���۲쵽_____����ͭ���к���CuSO4 |
�� | �����м�����������ᱵ��Һ�������ã�ȡ�ϲ���Һ���Թ��У��ٵμ�_____�� | ���۲쵽������ɫ��������ͭ���к���CuCl2 |
���壩��֪��
��ͭ���ʯ�к���Cu2��OH��2CO3������Ԫ�ص����ʣ�
����������Ļ�ѧʽΪ ��NH4��xFey��SO4��m��OH��n��������Ϊ+3�ۡ�
���ڻ�ѧ��Fe3O4���Ա�ʾΪFeOFe2O3
ij��ȤС�����ø�ͭ��ʯ�ƻ��������������ͼ2��
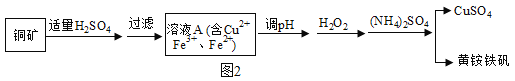
��1�������������ʽ��ʾCu2��OH��2CO3�����Ϊ_____��111gCu2 ��OH��2CO3��ϡH2SO4��Ӧʱ����H2SO4������Ϊ_____g��
��2����С��Ϊ�ⶨ�����������ɣ�����������ʵ�飺
a����ȡmg��Ʒ����������ȫ�ܽ��������Һ��Ϊ���ȷݣ�
b����һ���м�������NaOH��Һ�����ȣ��ռ���0.0425g�����壨��������ȫ���ݳ����������ó������ˡ�ϴ�ӡ����������أ��õ�����ɫ��ĩ0.600g��
c������һ���м�����BaCl2��Һ��ַ�Ӧ���ˡ�ϴ�ӡ�����ó���1.165g��
�����������NH4+��SO42���ĸ�����Ϊ_____��
��ͨ������ȷ����������Ļ�ѧʽ_____����д��������̣�
���𰸡�A B��A��C ���������� C CO2 ��ˮ����ͭ Cu2��OH��2CO3![]() 2CuO+H2O+CO2�� ����ʯ��ˮ����� Ca��OH��2+CO2�TCaCO3��+H2O ��ɫ���� ��������Һ 2CuOH2OCO2 98 1��2 NH4Fe3��SO4��2��OH��6
2CuO+H2O+CO2�� ����ʯ��ˮ����� Ca��OH��2+CO2�TCaCO3��+H2O ��ɫ���� ��������Һ 2CuOH2OCO2 98 1��2 NH4Fe3��SO4��2��OH��6
��������
��һ�����¹��ߵ�����������û�з�����ѧ�仯����ԭʼ������ʯ��������A��
���������½������ϵ�ұ����������Ⱥ�˳������ͭ��������������B��A��C��
������˳����Կ�����������Ʒ�ij���˳��������������йأ�������������ԣ�
�ɼ��ֽ���ʹ�õ�˳���֪�������Ļ��Խǿ����ʹ��˳����Խ������ô�����ر������ã������صĿ�ʼʹ��ʱ��Ӧ������֮����C��
������ͭ���������г�����Ʒ��ͭ�����治�ƣ����������һ����ɫͭ��Cu2��OH�� 2CO3���������غ㶨�ɿ�֪��ͭ�������������ˮ���������ҪCO2������CO2��
���ģ���1��MҩƷ����������ˮ����ͭ��������Ϊ��ˮ����ͭ��ˮ��Ӧ������ɫ������ˮ����ͭ�����Լ���ˮ�Ĵ��ڣ�������ˮ����ͭ��
��2��Cu2��OH��2CO3�ڼ��ȵ������·ֽ���������ͭ��ˮ�Ͷ�����̼���ʷ�Ӧ�Ļ�ѧ����ʽдΪ��Cu2��OH��2CO3![]() 2CuO+H2O+CO2����
2CuO+H2O+CO2����
��3��ʵ������У�����A����ɫ������Ϊ��ɫ��B�й������ɫ��C������Ϊ����ʯ��ˮ����ǣ��������ʯ��ˮ����ǣ�
C�еķ�Ӧ�Ƕ�����̼���������Ʒ�Ӧ���ɰ�ɫ����̼��ƺ�ˮ���ʷ�Ӧ�Ļ�ѧ����ʽдΪ��Ca��OH��2+CO2�TCaCO3��+H2O��
��4������������ͭ���ڣ�������ͭ���Ȼ�����Ӧ�����Ȼ�ͭ�����ᱵ�İ�ɫ�����������ɫ������
�ۼ����Ȼ�ͭ���ڿ�ͨ������Cl-����֤���������������ӽ�������Ȼ����İ�ɫ���������Կ��Լ�����������Һ��������������Һ��
���壩��1�������������ʽ��ʾCu2��OH��2CO3�����Ϊ2CuOH2OCO2������2CuOH2OCO2��
�⣺��������������Ϊx
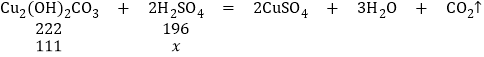
222��196=111��x
x��98g
����98��
��2���� �����Ӹ�����笠�������ȣ���������������ᱵ������ȣ����ɰ���������0.0425g���������ᱵ������1.165g�����������NH4+��SO42���ĸ�����Ϊ��![]() ��
��![]() ��1��2������1��2��
��1��2������1��2��
�� �õ�����ɫ��ĩ0.600g�����õ�0.600g��������������Ԫ������Ϊ��0.600g��![]() ��0.42g����������Ը�����
��0.42g����������Ը�����![]() ������������Ը�����
������������Ը�����![]() ��0.0025����������Ӹ�����
��0.0025����������Ӹ�����![]() ��0.005����������������Ը���Ϊa�����������У�0.0025����+1��+0.0075����+3��+0.005������2��+a������1����0����a��0.015������x��y��m��n��0.0025��0.0075��0.005��0.015��1��3��2��6����˻�������Ļ�ѧʽ NH4Fe3��SO4��2��/span>OH��6������NH4Fe3��SO4��2��OH��6��
��0.005����������������Ը���Ϊa�����������У�0.0025����+1��+0.0075����+3��+0.005������2��+a������1����0����a��0.015������x��y��m��n��0.0025��0.0075��0.005��0.015��1��3��2��6����˻�������Ļ�ѧʽ NH4Fe3��SO4��2��/span>OH��6������NH4Fe3��SO4��2��OH��6��


 Ӧ������ҵ��ϵ�д�
Ӧ������ҵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ӻ�ѧ��Ӧ����ʾ��ͼ�л�õĴ�����Ϣ�� ( )
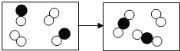
A. ��ͼ��ʾ����һ�����Ϸ�Ӧ
B. �û�ѧ��Ӧ�У�һ����Ԫ�صĻ��ϼ۷����ı�
C. ��ѧ��Ӧǰ��ԭ�����ࡢ��Ŀ���ֲ���
D. �÷�Ӧ�з�Ӧ��������ﶼ����ԭ��ֱ�ӹ��ɵ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʾ�Ϊ���г������ʣ�����A��ʹ������Сľ����ȼ��BΪ��ɫ���嵥�ʣ�CΪ��ɫ���������FΪ�Ϻ�ɫ���嵥�ʣ�EΪ�������Ҫ�ɷݣ�G��ʹ����ʯ��ˮ����ǣ��Իش��������⣺
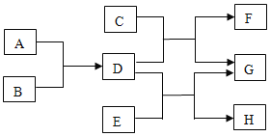
��1��D����Ϊ______���ѧʽ����
��2��д��D��C��Ӧ�Ļ�ѧ����ʽ��_______________��
��3��G���ʵ���;Ϊ��________��
��4��A��B��Ӧ�Ļ�ѧ����ʽ��________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й۵㶼�Ǵ���ģ������û�ѧ����ʽ����˵����
�۵� | ��ѧ����ʽ |
��������Ӧһ���ǻ��Ϸ�Ӧ | _____ |
�����κ�ˮ���ɷ�Ӧһ�����кͷ�Ӧ | _____ |
���û���Ӧһ���н������� | _____ |
������η�Ӧ������ͬʱ�������ֳ��� | _____ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ͼ��a��b��c�������ʵ��ܽ�����ߣ��ش��������⣺
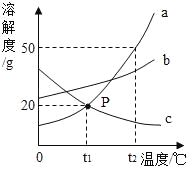
��1��P������_____��
��2��t2��ʱ��30g����a���뵽50gˮ�в��Ͻ��裬�õ�����a��_____����������������������������Һ����ʱ��Һ�����ʵ�����������_____����ȷ��0.1%����
��3����t2��ʱ��a��b��c�������ʵı�����Һ���µ�t1��ʱ��������Һ����������������С����_____��
��4������a�к�������������b���ɲ�ȡ_____�ķ����ᴿa���ʡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ��Ӧ���ڸ��ֽⷴӦ���ǣ�������
A. 3Fe+2O2![]() Fe3O4
Fe3O4
B. H2CO3��H2O+CO2��
C. Mg��OH��2+2HNO3��Mg��NO3��2+2H2O
D. 2C2H2+5O2![]() 2H2O+4CO2
2H2O+4CO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ˮ����������ͨ���ᷢ�����»�ѧ��Ӧ���䷴Ӧ���۹��̿���ͼ��ʾ��

��![]() ��ʾ��ԭ�ӣ�
��ʾ��ԭ�ӣ�![]() ��ʾ��ԭ�ӣ�
��ʾ��ԭ�ӣ�![]() ��ʾ��ԭ�ӣ�
��ʾ��ԭ�ӣ�
��1����д����ͼ��ʾ��Ӧ�Ļ�ѧ����ʽ�� ����
��2����ͼ��ʾ��Ӧ�Ļ�����Ӧ����Ϊ�� ����
��3�����������У����ڵ��ʵ����� �����ѧʽ����
��4��D��������Ԫ�صĻ��ϼ�Ϊ�� ����
��5���Լ�ͼΪ�������������ܽ����һ���������� ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��20��ʱ��NaCl�ܽ�������±������������ȷ����
ʵ�� ��� | ˮ�� ����(g) | ����NaCl ������(g) | ��Һ�� ����(g) |
�� | 10.0 | 1.5 | 11.5 |
�� | 10.0 | 3.0 | 13.0 |
�� | 10.0 | 4.5 | 13.6 |
�� | 10.0 | 6.0 | 13.6 |
A. ��������Һ��������������Ϊ15.0��
B. ����������Һ�DZ�����Һ
C. 20��ʱ��NaCl ���ܽ����45.0g��100g ˮ
D. �ۢ���Һ�����������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ������ʵ������֤ˮ���� �ɣ�

(1)ͼ 1 ��ʾʵ���У��۲쵽��������__________��
(2)ͼ 2 ��ʾʵ�飬��ֱͨ����Դһ��ʱ������� b �ڲ�����������_______________ ���ù��ڲ���Լ 10mL����ʱ�������� a �ڲ���Լ___________mL ���壮
(3)����ʵ��˵��ˮ����_______________ ��ɵģ�
(4)���ˮ��ʵ���У��ڵ������������������з�̪����������Һ(������ֻ��ǿ�����ԣ���������Ӧ)����ʵ������У��۲쵽�� b �缫��������ҺѸ�ٱ�죬��ô���Һ ��_____(��ᡱ������С�)�ԡ�������Һ��Ͼ��Ⱥ�����Һ�� pH=7��˵�����ʱ�� a �缫��������Һ��______(��ᡱ������С�)�ԣ�
(5)��ȡ 36g ��������Ϊ 1%����������Һ���е�⣬��������������Һ�����ʵ��� ��������Ϊ 1.8%����������________g ˮ��
(6)Ϊ��ȥˮ�е���ɫ����ζ��ˮ�м���______�� �ù�������______(��� ������ѧ��)�仯��
(7)�����п���ͨ����з���������ˮ��Ӳ�ȣ�Ӳˮ����й����з����Ļ�ѧ��Ӧ֮һ �ǣ�̼����ơ�̼���+������̼+ˮ���÷�Ӧ���ڷ�Ӧ�����е�______(�Ӧ�� ��)�������п���______����Ӳˮ����ˮ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com