
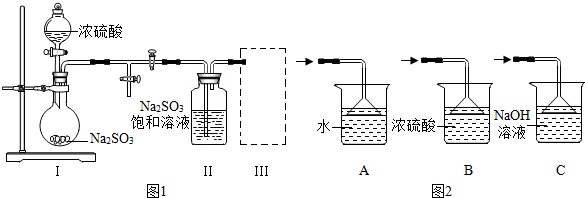
分析 本题属于物质的制备,由题目的信息可知:Na2SO3和硫酸反应生成硫酸钠和水和二氧化硫,配平即可;将装置Ⅱ中析出的晶体从溶液中分离出来的操作名称是过滤,装置Ⅲ用于处理尾气SO2,可选用图2中最合理装置为C,因为氢氧化钠溶液能吸收二氧化硫,防止空气污染;证明NaHSO3溶液呈酸性,可采用的实验方法是测定溶液的pH,PH小于7就显酸性;(5)测定某葡萄酒中防腐剂的残留量(以SO2计算)的原理:I2+SO2+2H2O=H2SO4+2HI,利用消耗的I2量可求SO2量.在实验过程中,若有部分HI变为I2,则测定结果偏低,因为消耗原来的I2量较少了.
解答 解:(1)由题目的信息可知:Na2SO3和硫酸反应生成硫酸钠和水和二氧化硫,配平即可;故答案为:Na2SO3+H2SO4=Na2SO4+H2O+SO2↑
(2)将装置Ⅱ中析出的晶体从溶液中分离出来的操作名称是过滤,故答案为:过滤
(3)装置Ⅲ用于处理尾气SO2,可选用图2中最合理装置为C,因为氢氧化钠溶液能吸收二氧化硫,防止空气污染;故答案为:C
(4)证明NaHSO3溶液呈酸性,可采用的实验方法是测定溶液的pH,PH小于7就显酸性;故答案为:c
(5)在实验过程中,若有部分HI变为I2,则测定结果偏低,因为消耗原来的I2量较少了,故答案为:偏低
点评 本考点属于实验题中的物质的制备题,综合性比较强,需要掌握酸碱盐的性质,还要掌握相互之间的反应规律和反应的条件.要注意根据题目给出的信息判断生成物,各有什么注意事项等.本考点主要出现在实验题中.


 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案科目:初中化学 来源: 题型:选择题
| A. | 氧气具有助燃性,可用作燃料 | |
| B. | 干冰升华时吸热,可用于人工降雨 | |
| C. | 盐酸能与金属氧化物反应,可用于金属除锈 | |
| D. | 氢氧化钠固体易潮解,可用作某些气体的干燥剂 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

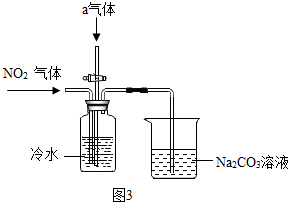
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 尿素[CO(NH2)2] | B. | 磷酸二氢铵(NH4H2PO4) | ||
| C. | 磷酸二氢钙[Ca(H2Po4)2] | D. | 硝酸钾(KNO3) |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com