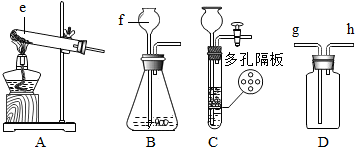
我校化学兴趣小组同学用加热高锰酸钾的方法制氧气,并做铁丝在氧气中燃烧的实验.请完成下列问题.
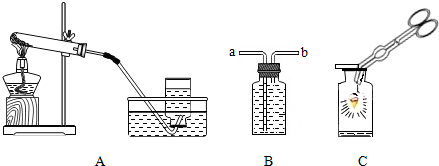
与氧气制取相关的问题:
(1)实验的主要步骤有:①加热 ②装药品并固定试管 ③检查装置的气密性 ④用排水法收集氧气 ⑤停止加热 ⑥将导管从水槽中取出.你认为正确的操作顺序是
;
(2)若用B装置来收集氧气,氧气应从
(填序号)端通入瓶内,若要测定收集氧气的体积,还需要
(仪器名称)来接排出的水.
(3)高锰酸钾受热分解的化学方程式是
;
与铁丝燃烧相关的问题:
(1)点燃铁丝前,将铁丝表面用砂纸打磨干净的目的是
;
(2)实验中为了防止集气瓶炸裂,必须
;
(3)写出铁丝在氧气中燃烧的化学方程式
.
如果你能完成下列2个问题,你可以得到4分的奖励分,化学满分不超过60分.
小亮对铁丝在氧气里燃烧时出现的红热球状物产生了兴趣,随后他进行了以下探究活动.
【问题1】铁燃烧后剩下来的球状物质中还有没有铁呢?
【收集资料】①铁粉和Fe
3O
4都黑色固体,都能被磁铁吸引;
②铁粉和Fe
3O
4都能和稀盐酸反应,铁与稀盐酸反应能生成氢气,而Fe
3O
4反应不能生成氢气.
【实验探究】将剩下来的球状物质碾碎,
,看到
,说明铁燃烧时溅落下来的黑色物质中还含有铁.
【问题2】铁燃烧的产物为什么不是Fe
2O
3呢?
【查阅资料】
(1)自然界中铁的氧化物主要是Fe
3O
4和Fe
2O
3两种(FeO极易被氧化为Fe
2O
3);
(2)Fe
3O
4和Fe
2O
3的分解温度、铁的熔点见表:
| Fe3O4 | Fe2O3 | 铁 |
| 分解温度/℃ | 1538 | 1400 | |
| 熔点/℃ | | | 1535 |
(3)Fe
2O
3高温时分解成Fe
3O
4和一种气体,据推测,这种气体应该是O
2,推测的依据是
.
【理论探究】实验测定铁在氧气里燃烧的产物是Fe
3O
4,结合表中数据,可推知铁在氧气里燃烧时产生的高温应在
℃之间,在此温度范围内 Fe
2O
3已分解.



 科学实验活动册系列答案
科学实验活动册系列答案