

| 假设和现象 | 判断和化学方程式 | |
| ① | 若现象a为白色沉淀 | 则猜想I不成立. |
| ② | 若现象a为产生白色沉淀, 现象b为无明显现象. | 则猜想Ⅲ成立.写出无色溶液B与硝酸中和反 应的化学方程式NaOH+HNO3=NaNO3+H2O. |
| ③ | 若现象a、b均 为:产生白色沉淀 | 则猜想Ⅱ成立.写出无色溶液B与硝酸钡溶液 反应的化学方程式Ba(NO3)2+Na2SO4=BaSO4↓+2NaNO3. |
分析 氯化钠溶于水时解离出的阴离子是氯离子,解离出的阳离子是钠离子,氯化钾溶于水时解离出的阴离子是氯离子,解离出的阳离子是钾离子,因此氯化钠和氯化钾溶于水时解离出的阴离子都是氯离子,每个氯离子带1个单位负电荷;
氯化钠、氯化钾不能和氢氧化钠反应,硫酸镁和氢氧化钠反应生成白色沉淀氢氧化镁和硫酸钠,氯化镁和氢氧化钠反应生成白色沉淀氢氧化镁和氯化钠;
氢氧化钠和稀硝酸发生中和反应生成硝酸钠和水,硫酸钠和硝酸钡反应生成不溶于稀硝酸的白色沉淀硫酸钡和硝酸钠.
解答 解:(1)样品中的NaCl和KCl溶于水时解离出的阴离子都是氯离子,可以表示为Cl-.
故填:Cl-.
(3)①若现象a为白色沉淀,说明样品b中添加有镁盐,同时说明猜想Ⅰ不成立;
②若现象a为产生白色沉淀,现象b为无明显现象,说明溶液B中不含有硫酸根离子,进一步说明样品b中不含有硫酸镁,即样品b中含有氯化镁,则则猜想Ⅲ成立,无色溶液B中氢氧化钠与硝酸中和反应生成硝酸钠和水,反应的化学方程式为:NaOH+HNO3=NaNO3+H2O;
③若现象a、b均为产生白色沉淀,说明溶液B中含有硫酸根离子,进一步说明样品b中含有硫酸镁,则猜想Ⅱ成立,无色溶液B中反应生成的硫酸钠与硝酸钡反应生成白色沉淀硫酸钡和硝酸钠,反应的化学方程式为:Ba(NO3)2+Na2SO4=BaSO4↓+2NaNO3;
填表如下所示:
| 假设和现象 | 判断和化学方程式 | |
| ① | 若现象a为白色沉淀 | 则猜想Ⅰ不成立. |
| ② | 若现象a为产生白色沉淀, 现象b为无明显现象. | 则猜想Ⅲ成立.写出无色溶液B与硝酸中和反 应的化学方程式为:NaOH+HNO3=NaNO3+H2O. |
| ③ | 若现象a、b均 为:产生白色沉淀 | 则猜想Ⅱ成立.写出无色溶液B与硝酸钡溶液 反应的化学方程式为:Ba(NO3)2+Na2SO4=BaSO4↓+2NaNO3. |
点评 向无色溶液B中加入稀硝酸中和氢氧化钠,说明向无色溶液A中加入的氢氧化钠是过量的,即无色溶液B中的硫酸盐是反应生成的硫酸钠,没有硫酸镁,因此和硝酸钡反应的是硫酸钠,要注意理解.


科目:初中化学 来源: 题型:选择题
| A. | 紫砂锅 | B. | 陶瓷碗 | C. | 不锈钢水瓢 | D. | 塑料盆 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 清洁剂名称 | 洁厕灵 | 活氧彩漂 | 漂白水 |
| 功能 | 有效清除污垢,除异味 | 漂洗衣物,使色彩鲜艳 | 快速漂除衣物污渍 |
| 有效成分 | 稀盐酸 | 双氧水 | 次氯酸钠(NaClO) |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验操作 | 实验现象 | 实验结论或化学方程式 |
| 将Mn片、Pd片 分别放入稀盐酸中 | Mn片表面有气泡产生,Pb片无明显现象 | 活动性:Mn>H>Pd |
| 实验操作 | 实验现象 | 化学方程式和实验结论 |
| 将Cu片浸入氯化钯(PdCl2)溶液中 | 铜丝表面覆盖一层银白色固体 | 化学方程式:Cu+PbCl2=Pb+CuCl2 |
| 将Ag片浸入PdCl2溶液中 | 无明显现象 | 实验结论:Ag的活动性比Pb弱 |
| 结论 | Pd、Cu、Ag金属活动性由强至弱:Cu、Pb、Ag | |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
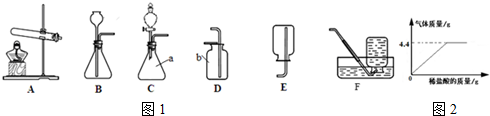
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 盛放氢氧化钠溶液的试剂瓶敞口放置 | |
| B. | 盛浓硫酸的试剂瓶敞口放置 | |
| C. | 生石灰放在敞口的小烧杯中 | |
| D. | 浓盐酸放置在密封的试剂瓶中 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
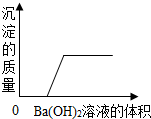 某溶液由盐酸、碳酸钠溶液、稀硫酸、氯化铜溶液四种物质中的一种或几种混合形成,现向该混合溶液中滴入氢氧化钡溶液,产生沉淀的质量与加入氢氧化钡溶液体积的关系如图所示.
某溶液由盐酸、碳酸钠溶液、稀硫酸、氯化铜溶液四种物质中的一种或几种混合形成,现向该混合溶液中滴入氢氧化钡溶液,产生沉淀的质量与加入氢氧化钡溶液体积的关系如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
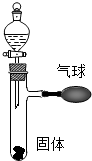 如图所示,打开分液漏斗,使其中的无色液体与试管中的固体接触反应,可观察到气球胀大现象,请分别写出3个符合图中现象,且分属不同反应类型的化学方程式:
如图所示,打开分液漏斗,使其中的无色液体与试管中的固体接触反应,可观察到气球胀大现象,请分别写出3个符合图中现象,且分属不同反应类型的化学方程式:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com