
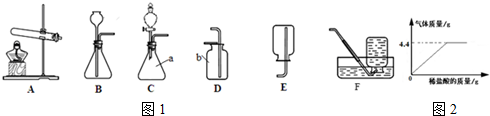
分析 (1)根据实验室常用仪器解答;
(2)装置A是用加热固体的方法制取氧气,且试管口无棉花,说明是用氯酸钾制取氧气,据此书写方程式;氧气不易溶于水,收集纯净的氧气用排水法;
(3)制取二氧化碳要用固体和液体在常温下反应,据此选择发生装置;然后利用二氧化碳不支持燃烧的特点来验满;
(4)实验室在常温下用块状电石与水反应制取微溶于水的乙炔气体,该反应必须严格控制加水速度,以免剧烈反应加热引起发生装置炸裂.能控制反应速率的为C装置.
(5)根据若选用E装置收集气体,气体应满足的条件是密度比空气小,且不与空气中的成分发生反应解答;
根据二氧化碳的质量可求出碳酸钙的质量,可求出石灰石样品中碳酸钙的质量分数
解答 解:
(1)根据实验室常用仪器可知:a锥形瓶;b集气瓶;
(2)装置A是用加热固体的方法制取氧气,且试管口无棉花,说明是用氯酸钾制取氧气,用氯酸钾和二氧化锰制取氧气,反应物是氯酸钾,生成物是氯化钾和氧气,方程式是2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;氧气不易溶于水,所以要收集纯度高、浓度大的氧气用排水法,排空气法收集的氧气可能混有少量空气;
(3)实验室制取二氧化碳是用固体石灰石与稀盐酸在常温下反应,又因二氧化碳不支持燃烧,可用燃着的木条放在瓶口,木条熄灭则说明已满.
(4)实验室在常温下用块状电石与水反应制取微溶于水的乙炔气体,该反应必须严格控制加水速度,以免剧烈反应加热引起发生装置炸裂.能控制反应速率的为C装置.
(5)若选用E装置收集气体,气体应满足的条件是密度比空气小,且不与空气中的成分发生反应;
(6)设大理石样品中碳酸钙的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 4.4g
$\frac{100}{x}=\frac{44}{4.4g}$
x=10g
大理石样品中碳酸钙的质量分数为$\frac{10g}{12g}$×100%≈83.3%
答案:
(1)锥形瓶; 集气瓶;
(2)2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;F;
(3)将燃着的木条放到集气瓶口,若立即熄灭则集满.
(4)C;
(5)密度比空气小,且不与空气中的成分发生反应.
(6)大理石样品中碳酸钙的质量分数为83.3%.
点评 了解实验室制取氧气的反应原理、并能结合装置图分析所用方法,收集气体的方法等,同时考查了学生依据实验现象分析解答问题的能力.


 教学练新同步练习系列答案
教学练新同步练习系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 钢铁生锈 | B. | 铁矿石炼成铁 | C. | 粉碎铁矿石 | D. | 酸洗铁锈 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 查阅初中化学课本上的金属活动顺序表 | |
| B. | 利用金属钛和FeCl2溶液进行实验 | |
| C. | 利用金属铁和TiSO4溶液进行实验 | |
| D. | 利用金属钛、金属铁与稀硫酸进行实验 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

| 假设和现象 | 判断和化学方程式 | |
| ① | 若现象a为白色沉淀 | 则猜想I不成立. |
| ② | 若现象a为产生白色沉淀, 现象b为无明显现象. | 则猜想Ⅲ成立.写出无色溶液B与硝酸中和反 应的化学方程式NaOH+HNO3=NaNO3+H2O. |
| ③ | 若现象a、b均 为:产生白色沉淀 | 则猜想Ⅱ成立.写出无色溶液B与硝酸钡溶液 反应的化学方程式Ba(NO3)2+Na2SO4=BaSO4↓+2NaNO3. |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 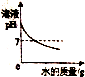 向一定量稀氢氧化钠溶液中滴入水 | |
| B. |  向一定量氯化铜溶液中加入一定量铝 | |
| C. |  向一定量硫酸和硫酸铜混合溶液中滴入氢氧化钠溶液 | |
| D. |  等质量的稀硫酸分别与足量的镁、铁、锌三种金属反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 多植树造林种草 | B. | 提倡绿色出行,发展公共交通 | ||
| C. | 大力发展火力发电 | D. | 开发太阳能、风能、地热能等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com