
【题目】取碳酸钠和氯化钠的混合物16g,加入150g水使其完全溶解,再加入100g氯化钡溶液恰好完全反应,过滤,得246.3g滤液(不考虑实验过程中质量损失)。计算(结果精确到0.1%):
(1)该混合物中碳酸钠的质量分数。
(2)反应后所得滤液中溶质的质量分数。
科目:初中化学 来源: 题型:
【题目】阅读下面科普短文。
葡萄的果肉和果皮中都含有丰富的营养物质,可生食、酿酒等。生食葡萄前要清洗干净。下图是一种清洗的方法:
葡萄酒是以鲜葡萄或葡萄汁为原料,经酿酒酵母菌株将葡萄汁中的糖转化为酒精,同时生成了高级醇、酯类、单萜等香气化合物。葡萄酒香气主要受酿造菌种、酿造工艺、发酵条件等因素的影响。研究人员以发酵汁中残糖量为指标,研究不同种类的酿酒酵母的发酵动力(即发酵过程的速率),其测定结果如图1所示。
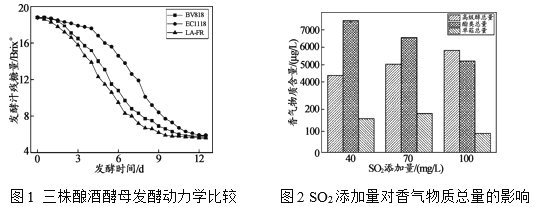
为防止葡萄酒在陈酿和贮藏过程中被氧化,抑制葡萄汁中微生物的活动,葡萄酒酿制中还会适量添加SO2,其添加量对主要香气物质总量影响如图2所示。
葡萄在栽种过程中容易产生病虫害,可通过定期施肥、中和酸性土壤、喷洒农药等方法来增强葡萄抗病能力。若发病,可用硫酸铜配制农药波尔多液进行喷洒。
依据文章内容回答下列问题。
(1)配制农药波尔多液时,不宜用铁制容器,其原因是_____(用化学方程式表示)。
(2)葡萄酒酿制过程中SO2的作用是_____。
(3)依据图1可获得的结论:在其他条件相同时,发酵动力最好的酿酒酵母菌株是_____。
A BV818 B EC1118 C LA-FR
(4)依据图2可知:SO2添加量在40~100 mg/L范围内,下列说法正确的是_____。
A SO2添加量在40 mg/L时,脂类总量最高
B 高级醇总量随着SO2添加量的增大而减小
C 单萜总量随着SO2添加量的增加,先增大后减小
(5)下列说法不正确的是_____。
A 面粉有利于去除葡萄皮上的脏东西
B 清洗干净后,建议吃葡萄不吐葡萄皮
C 葡萄富含糖类物质,糖尿病人不宜多食
D 可通过施加烧碱来中和酸性土壤
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学实验小组的同学在实验室里发现桌上有瓶敞口放置已久的NaOH溶液,他们对溶质的成分产生了探究的欲望。
[提出问题]这瓶NaOH溶液一定变质了,其变质程度如何呢?
[提出猜想]猜想一:NaOH溶液部分变质
猜想二:NaOH溶液完全变质
[实验探究]
(1)氢氧化钠溶液变质的原因为_____(用化学方程式表示)。
(2)小组的同学设计了如下实验进行探究,请根据表中内容填写:
实验步骤 | 现象 | 结论 | |
步骤一 | 取少量NaOH溶液样品于试管中,向其中滴加过量的CaCl2溶液 | 产生白色沉淀 | 猜想__成立 |
步骤二 | 过滤,向滤液中滴加酚酞试液 | 溶液变红色 | |
上述步骤一中,滴加过量CaCl2溶液的目的是____;步骤二中根据酚酞试液变红这一现象证明样品中含有___(填字母)。
A CaCl2
B Na2CO3
C NaOH
D Na2CO3和NaOH
[实验反思]
(1)下列物质中①BaCl2溶液、②Ca( NO3)2溶液、③Ca(OH)2溶液、④Ba(OH)2溶液,不能替代步骤一中CaCl2溶液的是____(填序号)。
(2)步骤二中用另外一种试剂代替酚酞试液也能得出同样的结论,发生反应的化学方程式为________。
(3)通过探究,实验室中的氢氧化钠应密封保存。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某氯化钠样品中含有少量的氯化钙,样品中钠元素和钙元素的质量比为23:20。取一定量的该样品,向其中加入适量的碳酸钠溶液(密度为1.1g/cm3)恰好完全反应,过滤,得到10g沉淀和112.8g滤液。请计算:
(1)原样品中氯化钙的质量
(2)所加入碳酸钠溶液的溶质质量分数。
(3)所加入碳酸钠溶液的体积。(计算结果精确到0.1)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】科技兴则国兴。嫦娥探月、蛟龙潜海、磁悬浮高铁纵横……,中国科技的迅猛发展让世界见证了“中国速度”!
(1)火箭、卫星、船舶等制造业常使用玻璃钢、塑料、钛合金等材料,其中塑料属于________(填字母)
A金属材料
B复合材料
C合成材料
(2)金属铝应用广泛。铝块制成铝丝,铝丝作室外高压线,铝合金制造的飞机外壳,具有轻量化、能抗击强大气流的冲击、耐受水雾和雨雪侵蚀等特点。据此可知铝具有_______性质(写出一种即可)。
(3)铝合金门窗变旧变暗后,尽量不用砂纸或钢丝球打磨,其原因用反应的化学方程式表示为_______。
(4)“愚人金”为铜锌合金,外观与黄金极为相似,纯铜的硬度比纯金硬度稍大。不法商贩常用“愚人金”冒充黄金牟取暴利。下列关于鉴别“愚人金”与黄金的实验方案,不合理的是______(填字母)。
A比较硬度,硬度大的是“愚人金”
B灼烧,表面变黑色的是“愚人金”
C浸没在稀硫酸中,表面有气泡产生的是“愚人金”
D浸没在硫酸镁溶液中,表面附着白色物质的“愚人金”
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】从某废旧电子产品中可以提炼贵重金属,并得到硫酸铜溶液。其工艺流程如图所示:
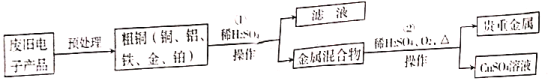
(1)图中“操作”的名称是_____ 。
(2)写出所得贵重金属中任意一种成分的化学式________。
(3)写出①中发生的化学反应方程式_______ ( 任写一种);该反应的基本类型为__ 。
(4)写出②中发生的化学反应方程式_______________ 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下表是几种物质在20℃的溶解度和相对分子质量。回答下列问题:
物质 | NaCl | NaHCO3 | NH4Cl | NH4HCO3 |
溶解度/g | 36.0 | 9.6 | 37.2 | 21.0 |
相对分子质量 | 58.5 | 84 | 53.5 | 79 |
(1)20℃时,用50g蒸馏水配制饱和NaHCO3溶液。
①计算需称量NaHCO3的质量是_____g。
②将称量的NaHCO3固体倒入盛有50g蒸馏水的烧杯中,然后用_____(填仪器名称)不断搅拌,直至_____。
③用配制所得的溶液可处理溶质的质量分数为1%的稀H2SO4_____g。
(2)相同温度下,不同溶质同时溶解在同一溶剂中,溶解度不变。在20℃时,将11.7gNaCl固体和15.8gNH4HCO3固体同时放入盛有100g水的烧杯中,充分搅拌,静置,观察到烧杯底部有晶体出现,该过程只发生复分解反应。杯底的晶体是_____,杯底晶体的质量是_____g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列说法中,正确的是
A.某碳酸钙和氧化钙组成的混合物中钙元素的质量分数为60%,将100g该混合物高温煅烧至固体质量不再改变,共生成16 g二氧化碳
B.某硝酸铵(NH4NO3)样品(杂质不含氮)中氮元素的质量分数为28%,则样品中硝酸铵的质量分数是40%
C.某种金属和铁的混合物5.6g与足量的稀硫酸充分反应,生成0.21 g氢气,则该种金属可能是镁
D.若SO2和SO3中氧元素的质量相等,则SO2和SO3两种物质的质量比一定为4 : 5
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室制取气体时需要的一些装置如下图所示,请回答下列问题。
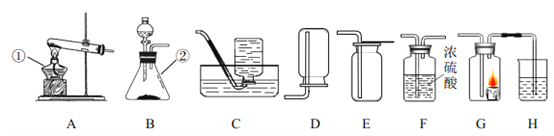
(1)写出标有序号的仪器名称:①______,②______。
(2)实验室制取氧气和二氧化碳的发生装置都可选用 B 装置的原因是______,装置中使用分液漏斗的优点是______。
(3)若要得到干燥的氧气,所选择装置的连接顺序为:B→______→______(填字母序号)。
(4)检验二氧化碳是否收集满的操作方法是______。
(5)某兴趣小组的同学连接 B、G、H 装置进行实验。若实验时 G 装置中蜡烛燃烧更剧烈,H 装置中溶液变浑浊,则 B 装置中反应的化学方程式为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com