
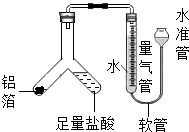
 梧州市某中学化学兴趣小组的同学到超市购买锡纸用于烧烤,同学们看见商品标签上标明锡纸的材质为“铝箔”.
梧州市某中学化学兴趣小组的同学到超市购买锡纸用于烧烤,同学们看见商品标签上标明锡纸的材质为“铝箔”.| 实验一:4mL 8% 的CuSO4溶液 | 实验二:4mL 8% 的CuCl2溶液 | |
| 实验现象 | 短时间内无变化,一段时间后铝片上才出现少量红色的铜. | 铝片上迅速有红色的铜出现. |
分析 根据金属的性质、检查装置气密性的方法、铝易被氧气氧化、金属与盐溶液反应的特点以及化学方程式的书写进行分析解答即可.
解答 解:【提出问题】由于锡和铝都能与盐酸反应生成氢气,故不能用加盐酸的方法鉴别锡和铝;利用熔点的不同可以采用加热的方法鉴别,故填:锡和铝都能与盐酸反应生成氢气;加热;
【探究活动一】(1)要检查该装置的气密性,可以从水准管一端注入水,待水准管和量气管出现较大高度差为止,静止几分钟,两侧高度差不缩小,证明装置气密性好,故填:从水准管一端注入水,待水准管和量气管出现较大高度差为止,静止几分钟,两侧高度差不缩小,证明装置气密性好;
(2)产生的氢气体积为100mL,即0.1L,氢气的密度为0.09g/L,故氢气的质量为:0.1L×0.09g/L=0.009g,设铝的质量为x,则有:
2Al+6HCl═2AlCl3+3H2↑
54 6
x 0.009g
$\frac{54}{x}$=$\frac{6}{0.009g}$
x=0.081g
故填:0.081;
【探究活动二】(1)铝的化学性质很活泼,易被氧气氧化生成致密的氧化铝保护膜,阻止反应的进行,故填:铝与氧气反应生成一层致密的氧化铝薄膜附在铝的表面,阻止反应的进行;
(2)要使铝箔燃烧,可以用火柴引燃,然后伸进盛有氧气的集气瓶中,故填:将铝箔卷曲,尖端夹一根火柴,将火柴引燃后,把火柴和铝箔一起伸入到盛有氧气的集气瓶中即可观察到铝箔燃烧并发出耀眼的白光;
【探究活动三】(1)铝与氯化铜反应生成氯化铝和铜,化学方程式为:2Al+3CuCl2═2AlCl3+3Cu;
(2)对比两个实验,氯化铜溶液中能快速出现红色的物质,说明对铝与铜盐溶液的反应可能有促进作用的离子是氯离子;可以才硫酸铜溶液中加入含有氯离子的氯化钠来进行实验,故填:Cl-;NaCl.
故答案为:【提出问题】锡和铝都能与盐酸反应生成氢气;加热;
【探究活动一】(1)从水准管一端注入水,待水准管和量气管出现较大高度差为止,静止几分钟,两侧高度差不缩小,证明装置气密性好;
(2)0.081;
【探究活动二】(1)铝与氧气反应生成一层致密的氧化铝薄膜附在铝的表面,阻止反应的进行;
(2)将铝箔卷曲,尖端夹一根火柴,将火柴引燃后,把火柴和铝箔一起伸入到盛有氧气的集气瓶中即可观察到铝箔燃烧并发出耀眼的白光;
【探究活动三】(1)2Al+3CuCl2═2AlCl3+3Cu;
(2)Cl-;NaCl.
点评 本题考查的是金属化学性质的实验探究,完成此题,可以依据已有的金属的性质结合物质间反应的实验现象进行.


科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | X | Y | Z | W |
| 反应前质量/g | 10 | 2.2 | 16.2 | 0.9 |
| 反应后质量/g | a | 4.4 | 8.1 | 1.8 |
| A. | a=15 | |
| B. | X、Z是反应物,Y、W是生成物 | |
| C. | Z为化合物 | |
| D. | 反应中Y、W两种物质变化的质量比为22:9 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质 | 所含杂质 | 除杂质的方法 |
| A | 氯化钙溶液 | 稀盐酸 | 加入过量的碳酸钙、过滤 |
| B | 硫酸钾溶液 | 氢氧化钾 | 适量的稀硫酸 |
| C | 二氧化碳 | 氯化氢 | 通过足量的碳酸氢钠溶液 |
| D | 二氧化锰 | 氯化钾 | 加水溶解、过滤、蒸发、结晶 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com