
| 实验操作 | 现象 | 结论 |
| 取少量该样品,滴入足量的 CaCl2溶液,充分反应后过滤. | 有白色沉淀生成 | 有关反应的化学方程式: CaCl2+Na2CO3═CaCO3↓+2NaCl |
| 在滤液中,滴入几滴 无色酚酞试液 | 溶液变红 | 样品未完全变质,仍含有氢氧化钠. |
分析 (1)A.根据酸和碱的组成特点分析;
B.中和反应特指酸与碱的反应;
C.根据酸碱的性质分析,多数酸和碱有腐蚀性;
D.根据复分解反应的特征分析判断;
(2)根据酸碱指示剂的变色规律和反应的化学方程式回答;
(3)根据氢氧化钠变质是与二氧化碳反应解答;验氢氧化钠部分变质的方法是先用氯化钙来检验是否含有碳酸根,然后用酚酞检验是否含有氢氧根离子.
解答 解:(1)A.酸和碱都含有氢元素,说法正确;B.中和反应是指酸碱中和,生成盐和水的反应不一定是中和反应,如酸性氧化物和碱反应也生成盐和水,但不是中和反应,故说法错误;C.多数酸和碱有腐蚀性,说法正确;D.复分解反应要想发生,生成物中必须有沉淀、水或气体生成,所以并不是酸和碱能与所有的盐发生复分解反应,故说法错误.故选BD;
(2)①溶液的红色消失一般是酸碱中和,结合题目中所提供的物质,该反应的化学方程式为2HCl+Ca(OH)2═CaCl2+2H2O 或 Ca(OH)2+H2SO4═CaSO4+2H2O.
②根据所提供的物质间的反应,蓝色溶液是硫酸铜溶液,生成的蓝色沉淀是氢氧化铜,说明硫酸和氢氧化钠反应时氢氧化钠过量,无色溶液中含有氢氧化钠,氢氧化钠和硫酸铜反应生成了蓝色的氢氧化铜沉淀.
(3)变质是生成了碳酸钠,若要证明碳酸钠,则根据碳酸钠和氢氧化钠的性质的不同,应选一种和碳酸钠溶液反应有白色沉淀生成但不能和氢氧化钠溶液反应的物质,故可选用氯化钙,然后检验滤液是否呈碱性.
故答案为:
(1)BD
(2)I 2HCl+Ca(OH)2═CaCl2+2H2O 或H2SO4+Ca(OH)2═CaSO4+2H2O
II 2NaOH+CuSO4═Cu(OH)2↓+Na2SO4(氧化铜和硫酸反应生成的硫酸铜和过量的氢氧化钠反应生成氢氧化铜蓝色沉淀)
(3)2NaOH+CO2═Na2CO3+H2O ①CaCl2/Ca(NO3)2/BaCl2/Ba(NO3)2溶液
②CaCl2+Na 2CO3═CaCO3↓+2NaCl ③溶液变红
点评 检验氢氧化钠与碳酸钠的混合物时,可先把碳酸钠变成沉淀并且不生成影响氢氧化钠检验的碱性物质,然后使用酚酞检验氢氧化钠.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
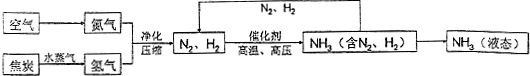
| 物质 | H2 | N2 | O2 | NH3 |
| 沸点 | -252℃ | -195.8℃ | -183℃ | -33.35℃ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 碱性溶液能使酚酞试液变红,所以能使酚酞试液变红的溶液一定呈碱性 | |
| B. | 酸碱中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 | |
| C. | 有一些金属与稀硫酸反应放出气体,所以与稀硫酸反应放出气体的物质是金属 | |
| D. | 碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
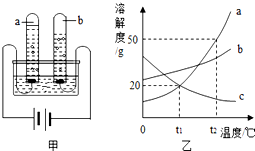 2014年3月22日是第二十二届“世界水日”,水与人类的生活和生产密切相关,请回答下列问题:
2014年3月22日是第二十二届“世界水日”,水与人类的生活和生产密切相关,请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
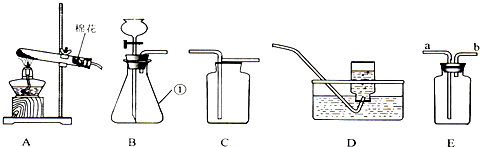
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Fe-----Fe3O4 | B. | Fe2O3--FeCl2 | C. | S--SO2 | D. | NaOH--Na2SO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com